| Эмбриональный эпидермальный лектин Xenopus | |||||||
|---|---|---|---|---|---|---|---|
 Мономерная структура XEEL-CRD со связанным D-глицерин-1-фосфатом. Белок окрашивается с помощью сине-красного градиента от N- к C-концу. Ионы кальция показаны зелеными сферами, а скоординированные молекулы воды показаны красными сферами. Мономерная структура XEEL-CRD со связанным D-глицерин-1-фосфатом. Белок окрашивается с помощью сине-красного градиента от N- к C-концу. Ионы кальция показаны зелеными сферами, а скоординированные молекулы воды показаны красными сферами. | |||||||
| Идентификаторы | |||||||
| Организм | Xenopus laevis | ||||||
| Symbol | itln1 | ||||||
| Entrez | 398574 | ||||||
| HomoloGene | 111044 | ||||||
| PDB | 4WN0 | ||||||
| RefSeq (мРНК) | NM_001089101.1 | ||||||
| RefSeq (Prot) | NP_001082570.1 | ||||||
| UniProt | Q800K0 | ||||||
| |||||||
| Интелектин-1 человека | |
|---|---|
 Мономерная структура интелектина человека со связанной аллил-бета-D-галактофуранозой. Белок окрашивается с помощью сине-красного градиента от N- к C-концу. Ионы кальция показаны зелеными сферами, а скоординированные молекулы воды показаны красными сферами. Мономерная структура интелектина человека со связанной аллил-бета-D-галактофуранозой. Белок окрашивается с помощью сине-красного градиента от N- к C-концу. Ионы кальция показаны зелеными сферами, а скоординированные молекулы воды показаны красными сферами. | |
| Идентификаторы | |
| Символ | ITLN1 |
| Alt. символы | hIntL-1 |
| ген NCBI | 55600 |
| HGNC | 18259 |
| OMIM | 609873 |
| PDB | 4WMY |
| RefSeq | NP_060095 |
| UniProt | Q8WWA0 |
| Прочие данные | |
| Locus | Chr. 1 q21.3 |
Интелектины представляют собой лектины (углеводсвязывающие белки), экспрессируемые в организме человека, и другие хордовые. Люди экспрессируют два типа интелектинов, кодируемых генами ITLN1 и ITLN2 соответственно. Некоторые интелектины связывают специфичные для микробов углеводные остатки. Таким образом, предполагается, что интелектины действуют как иммунные лектины. Несмотря на то, что интелектины содержат фибриноген-подобный домен, обнаруженный в семействе иммунных лектинов фиколинов, существует значительное структурное расхождение. Таким образом, интелектины могут не функционировать по тому же пути лектин-комплемент. Большинство интелектинов все еще плохо охарактеризовано, и они могут выполнять различные биологические роли. Также было показано, что человеческий интелектин-1 (hIntL-1) связывает лактоферрин, но его функциональные последствия еще предстоит выяснить. Кроме того, hIntL-1 является основным компонентом астматической слизи и также может участвовать в физиологии инсулина.
Первый интелектин был обнаружен в ооците Xenopus laevis и назван XL35 или XCGL-1. Ооцит X. laevis также содержит близкородственный XCGL-2. Кроме того, эмбрионы X. laevis выделяют лектин эпидермиса эмбриона Xenopus в воду из окружающей среды, предположительно для связывания микробов. XSL-1 и XSL-2 также экспрессируются в сыворотке X. laevis при стимуляции липополисахаридом. У X. laevis
обнаружены два дополнительных кишечных интелектина. Человек имеет два интелектина: hIntL-1 (оментин) и hIntL-2. У мыши также есть два интеллектина: mIntL-1 и mIntL-2.
Несколько линий доказательств предполагают, что интелектины распознают микробы и могут функционировать как защитный белок врожденного иммунитета. Оболочечный интелектин - это опсонин для фагоцитоза гемоцитами. Было показано, что интелектин амфиоксуса агглютинирует бактерии. У рыбок данио и радужной форели экспрессия интелектина стимулируется при воздействии микробов. Млекопитающие, такие как овцы и мыши, также повышают экспрессию интелектина при паразитарной инфекции. Повышение экспрессии интелектина при воздействии микробов подтверждает гипотезу о том, что интелектины играют роль в иммунной системе.
Хотя для функционирования интелектинам требуется ион кальция, последовательности не имеют ничего общего с лектинами C-типа. Кроме того, всего около 50 аминокислот (фиброноген-подобный домен) выравниваются с любым известным белком, в частности с семейством фиколина. Первые структурные детали интелектина происходят из кристаллической структуры домена распознавания углеводов XEEL, меченного селенометионином (Se-Met XEEL-CRD), решенного с помощью Se- SAD. XEEL-CRD экспрессировали и метили Se-Met в клетках насекомых High Five с использованием рекомбинантного бакуловируса. Фибриноген-подобная складка сохраняется, несмотря на дивергенцию аминокислотной последовательности. Однако в интелектине присутствуют обширные вставки по сравнению с фиколинами, что делает интелектин отдельным структурным классом лектинов. Затем структура Se-Met XEEL-CRD обеспечивает решение структуры путем молекулярной замены связанного с D-глицерин-1-фосфатом (GroP) XEEL-CRD, апо-человеческого интелектина-1 (hIntL-1), и hIntL-1, связанный с галактофуранозой.
Каждая полипептидная цепь XEEL и hIntL-1 содержит три связанных иона кальция: два в структурном сайте кальция и один в сайте связывания лиганда. Аминокислотные остатки в структурном сайте кальция консервативны среди интелектинов, поэтому вероятно, что большинство, если не все, интелектины имеют два структурных иона кальция.
В сайте связывания лиганда XEEL и hIntL-1, экзоциклический вицинальный диол углеводного лиганда непосредственно координируется с ионом кальция. Существуют большие вариации в остатках сайтов связывания лиганда среди гомологов интелектина, что позволяет предположить, что семейство интелектинов может иметь широкую лигандную специфичность и биологические функции. Поскольку в разных организмах нет соглашений о нумерации интектинов, не следует предполагать функциональную гомологию на основе числа интектинов. Например, hIntL-1 имеет остатки глутаминовой кислоты в сайте связывания лиганда для координации иона кальция, в то время как интелектин-1 рыбок данио лишен этих кислотных остатков. Остатки сайта связывания лиганда интелектина-2 рыбок данио аналогичны остаткам, присутствующим в hIntL-1.

Сайт связывания лиганда эмбрионального эпидермального лектина Xenopus (XEEL) со связанным D-глицерин-1-фосфатом. Ион кальция показан зеленой сферой, а упорядоченные молекулы воды показаны красными сферами.

Сайт связывания лиганда человеческого интелектина-1 (hIntL-1) со связанной аллил-бета-D-галактофуранозой. Ион кальция показан в виде зеленой сферы, а упорядоченные молекулы воды показаны в виде красных сфер.
hIntL-1 представляет собой тример с дисульфидной связью, как показано невосстанавливающим SDS-PAGE и Рентгеновская кристаллография. Несмотря на отсутствие межмолекулярных дисульфидных связей, XEEL-CRD является тримерным в растворе. N-концевой пептид полноразмерного XEEL отвечает за димеризацию тримерного XEEL-CRD в гексамерный полноразмерный XEEL с дисульфидной связью. Следовательно, N-концы интелектинов часто ответственны за образование олигомеров, связанных дисульфидной связью. В гомологах интелектина, где N-концевые цистеины отсутствуют, сам CRD может все еще образовывать нековалентный олигомер в растворе.

Дисульфидно-связанный тримерный человеческий интелектин-1.
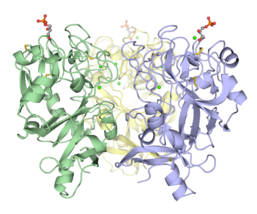
Тримерный домен распознавания углеводов эпидермального лектина эмбриона Xenopus (XEEL-CRD). Обширные биофизические исследования убедительно показывают, что XEEL-CRD является тримером в растворе, несмотря на отсутствие межмолекулярных дисульфидных связей, обнаруженных в hIntL-1.