 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Daurismo |
| Другие названия | PF- 04449913 |
| AHFS / Drugs.com | Монография |
| MedlinePlus | a619004 |
| Беременность. категория |
|
| Код АТС | |
| Правовой статус | |
| Правовой статус |
|
| Идентификаторы | |
Название IUPAC
| |
| Номер CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL |
|
| ECHA InfoCard | 100.244.738 |
| Химические и физические данные | |
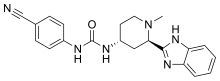
| Формула | C21H22N6O |
| Молярная масса | 374,448 г · моль |
| 3D-модель (JSmol ) | |
УЛЫБКИ
| |
InChI
| |
Glasdegib, продаваемый под торговой маркой Daurismo, представляет собой лекарство для лечения впервые диагностированного острого миелоидного лейкоза (AML) у взрослых старше 75 лет или те, у кого есть сопутствующие заболевания, исключающие использование интенсивной индукционной химиотерапии. Его принимают внутрь и используют в сочетании с низкой дозой цитарабина.
. Рекомендуемая доза гласдегиба составляет 100 мг перорально один раз в день с 1 по 28 дни в сочетании с 20 мг цитарабина подкожно два раза в день с 1 по 28 день. 10 из каждого 28-дневного цикла при отсутствии неприемлемой токсичности или потери контроля над заболеванием.
Наиболее частыми побочными реакциями являются анемия, утомляемость, кровоизлияние, фебрильная нейтропения, скелетно-мышечная боль, тошнота, отек, тромбоцитопения, одышка., снижение аппетита, дисгевзия, мукозит, запор и сыпь.
Это низкомолекулярный ингибитор sonic hedgehog, который является сверхэкспрессируемым белком при многих типах рака. Он подавляет рецептор sonic hedgehog сглаженный (SMO), как и большинство препаратов этого класса.
Гласдегиб был одобрен для медицинского применения в США в декабре 2018.
Одобрение FDA было основано на многоцентровом открытом рандомизированном исследовании (BRIGHT AML 1003, NCT01546038), в которое вошли 115 субъектов с впервые диагностированным AML, которые соответствовали хотя бы одному из следующих критериев: возраст 75 лет и старше, b) тяжелое сердечное заболевание, c) исходный статус работы Восточной кооперативной онкологической группы, равный 2, или d) исходный уровень креатинина сыворотки>1,3 мг / дл. Субъекты были рандомизированы в соотношении 2: 1 для получения гласдегиба, 100 мг в день, с LDAC 20 мг подкожно два раза в день в дни с 1 по 10 28-дневного цикла (N = 77) или только LDAC (N = 38) в 28-дневных циклах. до прогрессирования заболевания или неприемлемой токсичности. Испытание проводилось в США, Канаде и Европе.
Эффективность была установлена на основе улучшения общей выживаемости (дата рандомизации до смерти от любой причины). При среднем сроке наблюдения 20 месяцев, медиана выживаемости составила 8,3 месяца (95% ДИ: 4,4, 12,2) для группы гласдегиб + LDAC и 4,3 месяца (95% ДИ: 1,9, 5,7) для группы, получавшей только LDAC, и HR 0,46 (95% ДИ: 0,30, 0,71; p = 0,0002).
Гласдегиб получил приоритетный обзор и орфанный лекарственный препарат США Food and Управление лекарственных средств (FDA). В октябре 2017 года ему было присвоено звание орфанного препарата Европейским агентством по лекарственным средствам (EMA).
Гласдегиб был одобрен для медицинского применения в Европейском союзе в июне 2020 года.
.