эпигенетика шизофрении - это исследование того, как наследуются эпигенетические изменения. регулируется и модифицируется окружающей средой и внешними факторами, и как эти изменения формируют и влияют на возникновение, развитие и уязвимость шизофрении. Эпигенетика также изучает, как эти генетические модификации могут быть переданы будущим поколениям. Шизофрения - изнурительное и часто неправильно понимаемое заболевание, которым страдает до 1% населения мира. Хотя шизофрения - это хорошо изученное заболевание, оно остается в значительной степени непроницаемым для научного понимания, поэтому эпигенетика предлагает новый путь для исследований, понимания и лечения.
Исторически шизофрения изучалась и исследовалась с помощью различных парадигм или школ мысли. В конце 1870-х гг. Эмиль Крепелин задумал изучить это как болезнь. Другой парадигмой, предложенной Зубиным и Спрингом в 1977 году, была модель стресс-уязвимость, в которой индивидуум обладает уникальными характеристиками, которые придают ему или ей сильные стороны или уязвимые места, чтобы справиться со стрессом, предрасположенность к шизофрении. Совсем недавно, при расшифровке генома человека, основное внимание было уделено идентификации конкретных генов для изучения болезни. Однако парадигма генетики столкнулась с проблемами, связанными с противоречивыми, неубедительными и непостоянными результатами. Самая последняя школа мысли изучает шизофрению посредством эпигенетики.
 Визуализация модели стресс-уязвимость, также известной как модель диатеза-стресса
Визуализация модели стресс-уязвимость, также известной как модель диатеза-стресса Идея эпигенетики была описана еще в 1942 году, когда Конрад Уоддингтон описал это как то, как среда регулирует генетику. По мере развития области и доступных технологий этот термин также стал относиться к молекулярным механизмам регуляции. Идея о том, что эти эпигенетические изменения могут быть переданы будущим поколениям, постепенно становится все более общепринятой.
Хотя эпигенетика - относительно новая область исследований, конкретные приложения и внимание к психическим расстройствам, таким как шизофрения, стали еще более новой областью. исследований.
Основные симптомы шизофрении можно разделить на три большие категории. Эти симптомы часто используются для построения и изучения животных моделей шизофрении в области эпигенетики. Положительные симптомы считаются отклонениями лимбической системы, в то время как негативные и когнитивные симптомы считаются аномалиями лобных долей.
Положительные симптомы:
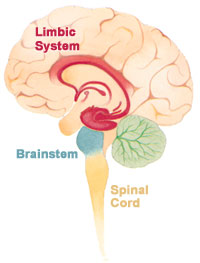 лимбическая система и связанные с ней структуры мозга, где аномалии приводят к положительным симптомам шизофрении.
лимбическая система и связанные с ней структуры мозга, где аномалии приводят к положительным симптомам шизофрении. Отрицательные симптомы:
Когнитивные расстройства:
Существует множество доказательств того, что шизофрения - это наследственное заболевание. Одним из ключевых доказательств является исследование близнецов, которое показало, что вероятность развития болезни составляет 53% для одного члена монозиготных близнецов (близнецов с одинаковым генетическим кодом) по сравнению с 15% для дизиготных близнецов, которые не разделяют точная ДНК. Другие ставят под сомнение доказательства наследственности из-за разных определений шизофрении и сходной среды для обоих близнецов.
Тот факт, что даже монозиготные близнецы не имеют 100% конкордантности, предполагает факторы окружающей среды. играют роль в уязвимости и развитии расстройства. Были предложены различные факторы окружающей среды, включая употребление марихуаны, осложнения во время беременности, социально-экономический статус и окружающую среду, а также недоедание матери. По мере развития эпигенетики эти и другие внешние факторы риска, вероятно, будут учитываться в эпидемиологических исследованиях.
Некоторые гены были определены как важные при изучении шизофрении, но есть Некоторые из них играют особую роль при изучении эпигенетических модификаций болезни.
Оба белка создаются ГАМКергическими нейронами. Несколько исследований продемонстрировали, что уровни как рилина, так и GAD67 снижены у пациентов с шизофренией и на моделях животных.
Эпигенетику можно изучать и исследовать с помощью различных методов. Один из наиболее распространенных методов - это исследование посмертной ткани мозга пациентов с шизофренией и анализ их на биомаркеры. Другие распространенные методы включают исследования тканевых культур нейронов, полногеномный анализ клеток, не относящихся к головному мозгу, у живых пациентов (см. PBMC ), а также модели трансгенных и шизофренических животных.
Другие исследования, которые являются которые проводятся в настоящее время или могут быть выполнены в будущем, включают лонгитюдные исследования пациентов, групп риска и монозиготных близнецов, а также исследования, изучающие взаимодействие конкретных генов и окружающей среды и эпигенетические эффекты.
Эпигенетика (переводится как «выше генетики») - это изучение того, как гены регулируются посредством обратимых и наследуемых молекулярных механизмов. Эпигенетические изменения изменяют экспрессию гена либо путем активации гена, который кодирует определенный белок, либо путем репрессии гена. Существует две основные категории модификаций: метилирование ДНК и модификации гистонов. Результаты исследований показали, что несколько примеров обоих этих изменений связаны с шизофренией и ее симптомами.
 Механизмы эпигенетики в клетке
Механизмы эпигенетики в клетке метилирование ДНК - это ковалентное добавление метил группу к сегменту кода ДНК. Эти группы -CH3 добавляются к остаткам цитозина ферментами DNMT (ДНК-метитрансферазы). Связывание метильной группы с областями промотора препятствует связыванию факторов транскрипции и заглушает ген, предотвращая транскрипцию этого кода. Метилирование ДНК - один из наиболее хорошо изученных эпигенетических механизмов, и было обнаружено несколько открытий, связывающих его с шизофренией.
В различных исследованиях последовательно показано, что уровни рилина и GAD67 подавляются в образцах кортикальной ткани и гиппокампа у людей с шизофренией. Эти белки используются ГАМКергическими нейронами, и отклонения в их уровнях могут привести к некоторым симптомам, обнаруживаемым у людей с шизофренией. Гены этих двух белков находятся в областях генетического кода, которые могут быть метилированы (см. остров CpG ). Недавние исследования продемонстрировали эпигенетическую связь между уровнями белков и шизофренией. Одно исследование показало, что нейроны коры с более низким уровнем GAD67 и рилина также показали повышенный уровень DNMT1, одного из ферментов, который добавляет метильную группу. Также было показано, что состояние шизофренического типа может быть вызвано у мышей, когда им хронически давали l-метионин, предшественник, необходимый для активности DNMT. Эти и другие открытия обеспечивают прочную связь между эпигенетическими изменениями и шизофренией.
Метилирование ДНК также может влиять на экспрессию BDNF (нейротрофического фактора мозга). Белок BDNF важен для познания, обучения и даже для уязвимости к травмам в раннем возрасте. Sun et al. показали, что состояние страха приводит к изменениям уровней метилирования ДНК в промоторных областях BDNF в нейронах гиппокампа. Также было показано, что ингибирование активности DNMT приводит к изменению уровней BDNF в гиппокампе. Также было показано, что на метилирование ДНК BDNF влияет постнатальный социальный опыт, стрессовая среда и лишение социального взаимодействия. Кроме того, эти стимулы также связаны с повышенной тревожностью, проблемами с познанием и т. Д. Хотя прямой связи между шизофренией и уровнями BDNF не установлено, эти результаты предполагают связь со многими проблемами, которые похожи на симптомы.
Гистоны - это белки, вокруг которых заключена ДНК-хромосома. Гистоны представлены в виде октамера (набор из 8 белков), и они могут быть модифицированы посредством ацетилирования, метилирования, SUMOylation и т. Д. Эти изменения могут открываться или закрыть хромосому. Таким образом, в зависимости от того, какой гистон модифицируется и точного процесса, модификации гистонов могут либо заглушать, либо способствовать экспрессии генов (тогда как метилирование ДНК почти всегда заглушает).
Поскольку подполе модификаций гистонов относительно новое, результатов пока немного. Некоторые исследования показали, что пациенты с шизофренией имеют более высокий уровень метилирования в H3 (3-й гистон в октамере) в префронтальной коре, области, которая может быть связана с негативными симптомами. Также было показано, что ацетилирование гистонов и фосфорилирование увеличивается на промоторе белка BDNF, который участвует в обучении и памяти.
Более поздние исследования показали, что посмертная ткань мозга от пациенты с шизофренией имели более высокие уровни HDAC, гистондеацетилазы, фермента, удаляющего ацетильные группы из гистонов. Уровни HDAC1 обратно коррелируют с экспрессией белка GAD67, которая снижается у пациентов с шизофренией.
Исследования показали, что эпигенетические изменения могут передаваться будущим поколениям через мейоз и митоз. Эти результаты показывают, что факторы окружающей среды, с которыми сталкиваются родители, могут влиять на то, как регулируется генетический код ребенка. Результаты исследований показали, что это верно и для пациентов с шизофренией. У крыс передача материнского поведения и даже стрессовых реакций может быть объяснена тем, как метилируются определенные гены в гиппокампе матери. Другое исследование показало, что метилирование гена BDNF, на которое могут повлиять стресс и злоупотребления в раннем детстве, также передается будущим поколениям.
Пока есть убежище ' На данный момент было проведено множество исследований, связывающих факторы окружающей среды с механизмами эпигенетики, связанной с шизофренией, несколько исследований показали интересные результаты. Согласно недавним исследованиям, пожилой отцовский возраст является одним из факторов риска шизофрении. Это происходит через мутагенез, который вызывает дальнейшие спонтанные изменения, или через геномный импринтинг. По мере старения родителей в эпигенетическом процессе может происходить все больше и больше ошибок. Есть также свидетельства связи между вдыханием бензола при сжигании древесины и развитием шизофрении. Это могло произойти из-за эпигенетических изменений. Метамфетамин также был связан с шизофренией или подобными психотическими симптомами. Недавнее исследование показало, что потребители метамфетамина изменили уровни DNMT1, аналогично тому, как пациенты с шизофренией показали аномальные уровни DNMT1 в ГАМКергических нейронах.
Одним из наиболее интересных открытий, касающихся фактора окружающей среды с эпигенетическими механизмами шизофрении, является воздействие к никотину. Широко известно, что 80% больных шизофренией употребляют табак в той или иной форме. Более того, курение, по-видимому, улучшает познавательные способности у людей с шизофренией. Однако только недавнее исследование Сатта и др. Показало, что никотин приводит к снижению уровня DNMT1 в ГАМКергических нейронах мыши, молекулы, которая добавляет метильные группы к ДНК. Это привело к увеличению экспрессии GAD67.
Существуют несколько ограничений для текущих методов исследования и научных результатов. Одна из проблем патологоанатомических исследований заключается в том, что они демонстрируют только один снимок пациента с шизофренией. Таким образом, трудно сказать, связаны ли результаты биомаркеров с патологией шизофрении.
Другое ограничение заключается в том, что у живых пациентов с шизофренией невозможно получить самую важную ткань, ткань мозга. Чтобы обойти эту проблему, в нескольких исследованиях использовались более доступные источники, такие как лимфоциты или линии зародышевых клеток, поскольку некоторые исследования показали, что эпигенетические мутации могут быть обнаружены в других тканях.
Эпигенетические исследования таких расстройств, как шизофрения, также зависят от субъективности психиатрических диагнозов и спектрального характера проблем психического здоровья. Эта проблема с классификацией проблем психического здоровья привела к промежуточным фенотипам, которые могли бы лучше подходить.
Появление эпигенетики как средства проведения исследований в области шизофрении открыло множество возможностей как для раннего выявления, диагностики и лечения. Хотя эта область все еще находится на начальной стадии, многообещающие результаты уже получены. Некоторые посмертные исследования мозга, посвященные экспрессии генов метилирования гистонов, показали многообещающие результаты, которые могут быть использованы для раннего выявления у других пациентов. Однако основная часть трансляционных исследований и результатов была сосредоточена на терапевтических вмешательствах.
Поскольку эпигенетические изменения обратимы и чувствительны к фармакологическим методам лечения и лекарствам, есть многообещающие перспективы в развивающие методы лечения. Как отмечали многие, шизофрения - это пожизненное заболевание, имеющее широко распространенные последствия. Таким образом, возможно, не удастся полностью обратить болезнь вспять. Однако недавние результаты показывают, что можно лечить пациентов с шизофренией, облегчить симптомы или повысить эффективность антипсихотических препаратов.
Ингибиторы HDAC (гистондеацетилазы) - это один класс препаратов, которые исследуются. Исследования показали, что уровни рилина и GAD67 (которые снижены на моделях шизофренических животных) повышаются после лечения ингибиторами HDAC. Кроме того, существует дополнительное преимущество селективности, поскольку ингибиторы HDAC могут быть специфичными для типа клеток, типа ткани и даже областей мозга.
Ингибиторы HMT (гистон-деметилазы) также действуют на гистоны. Они предотвращают деметилирование гистонового белка H3K4 и открывают эту часть хроматина. Было показано, что транилципромин, антидепрессант, обладает ингибирующими свойствами в отношении ГМТ, и в одном исследовании лечение пациентов с шизофренией транилципромином показало улучшение в отношении негативных симптомов.
Было также показано, что ингибиторы DNMT увеличивают уровни белка наматывания и GAD67 в культурах клеток. Однако некоторые из нынешних ингибиторов DNMT, такие как зебуларин и прокаинамид, не проникают через гематоэнцефалический барьер и не могут оказаться столь же эффективными при лечении. Хотя ингибиторы DNMT могут предотвратить добавление метильной группы, также проводятся исследования индукторов деметилата ДНК, которые фармакологически индуцируют удаление метильных групп. Было показано, что современные антипсихотические препараты, такие как клозапин и сульпирид, также вызывают деметилирование.