 Общий диазирин
Общий диазирин Диазирин - это класс органических молекул, состоящих из углерода, связанного с двумя атомами азота, которые связаны двойной связью друг с другом, образуя циклопропен -подобное кольцо, 3H-диазирен. При облучении ультрафиолетовым светом диазирины образуют реактивные карбены, которые могут вставляться в связи C-H, N-H и O-H. Следовательно, популярность диазиринов возросла в качестве небольших фотореактивных сшивающих реагентов. Они часто используются в исследованиях фотоаффинного мечения для наблюдения за различными взаимодействиями, включая взаимодействия лиганд-рецептор, лиганд-фермент, белок-белок и белок-нуклеиновая кислота.
В литературе существует ряд методов получения диазиринов, которые начинаются с различных реагенты.
Обычно схемы синтеза, которые начинаются с кетонов, включают превращение кетона с желаемыми заместителями в диазиридины. Затем эти диазиридены окисляются с образованием желаемых диазиринов.
Диазиридины можно получить из кетонов оксимированием с последующим тозилированием (или мезилированием) и, наконец, обработкой аммиаком. Обычно реакции оксимации осуществляются путем взаимодействия кетона с хлоридом гидроксиламмония при нагревании в присутствии основания, такого как пиридин. Последующее тозилирование или мезилирование альфа-замещенного кислорода тозилом или мезилхлоридом в присутствии основания дает тозил или мезилоксим. Конечная обработка тозил- или мезилоксима аммиаком дает диазиридин.
 Обычный синтез диазиридина оксимированием, тозилированием и обработкой аммиаком.
Обычный синтез диазиридина оксимированием, тозилированием и обработкой аммиаком. Диазиридины также могут быть получены непосредственно реакцией кетонов с аммиаком в присутствии аминирующего агента, такого как монохлорамин или гидроксиламин-O-сульфоновая кислота.
Диазиридины можно окислять до диазиринов несколькими способами. К ним относятся окисление реагентами на основе хрома, такими как окисление Джонса, окисление йодом и триэтиламином, окисление оксидом серебра, окисление оксалилхлоридом или даже электрохимическое окисление на платино-титановом аноде.
 Джонс. окисление родового диазиридина до диазирина.
Джонс. окисление родового диазиридина до диазирина. Диазирины могут быть альтернативно образованы в однореакторном процессе с использованием реакции Грэма. В этих схемах амидины могут быть напрямую превращены в диазирины окислением гипогалита. Эта реакция дает галогенированный диазирин, который можно дополнительно модифицировать.
Полученный вышеупомянутый галодиазирин может подвергаться обменной реакции для дальнейшей функционализации диазирена. В этих реакциях анионные нуклеофилы, такие как фторид тетра-н-бутиламмония или метокситетра-н-бутиламмоний, могут заменять галогенные заместители, давая фтордиазирин или метоксидиазирин соответственно.
 Реакция обмена диазирина с использованием различных анионов и противоиона тетра-n -бутиламмоний.
Реакция обмена диазирина с использованием различных анионов и противоиона тетра-n -бутиламмоний. При облучении УФ-светом диазирины образуют реактивные карбен. Карбен может существовать в синглетной форме, в которой два свободных электрона занимают одну и ту же орбиталь, или в триплетной форме с двумя неспаренными электронами на разных орбиталях.
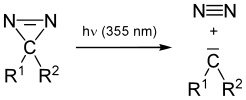 Диазирины могут быть разложены с помощью УФ-света.
Диазирины могут быть разложены с помощью УФ-света. Заместители в диазирине влияют на то, какие карбеновые частицы образуются при облучении и последующем фотолитическом расщеплении. Заместители диазирина, которые являются донорами электронов по своей природе, могут передавать электронную плотность пустой р-орбитали карбена, которая будет образовываться, и, следовательно, могут стабилизировать синглетное состояние. Например, фенилдиазирин производит фенилкарбен в синглетном карбеновом состоянии, тогда как п-нитрофенилхлордиазирин или трифторфенилдиазирин производят соответствующие триплетные карбеновые продукты.
Электронодонорные заместители также могут способствовать фотоизомеризации с образованием линейного диазосоединения, а не синглетного карбена, и следовательно, эти соединения не подходят для использования в биологических анализах. С другой стороны, трифторарилдиазирины, в частности, проявляют благоприятную стабильность и фотолитические свойства и наиболее часто используются в биологических применениях.
 Три диазирина показаны выше. Фенилдиазирин производит синглетный карбен, тогда как трифторметилфенилдиазирин и п-нитрофенилхлордиазирин производят карбены в триплетном состоянии.
Три диазирина показаны выше. Фенилдиазирин производит синглетный карбен, тогда как трифторметилфенилдиазирин и п-нитрофенилхлордиазирин производят карбены в триплетном состоянии. Карбены, полученные из диазиринов, быстро гасятся реакцией с молекулами воды, и, следовательно, выходы для анализов фотореактивного сшивания часто низкие. Тем не менее, поскольку эта функция сводит к минимуму неспецифическую маркировку, на самом деле это преимущество использования диазиринов.
Диазирины часто используются в качестве фотореактивных сшивающих реагентов, поскольку реактивные карбены, которые они образуют при облучении УФ-светом, могут вставляться в связи C-H, N-H и O-H. Это приводит к зависимому от близости мечения других видов диазиринсодержащим соединением.
Диазирины часто предпочтительнее других фотореактивных сшивающих реагентов из-за их меньшего размера, большей длины волны облучения, необходимого короткого периода облучения и стабильности в присутствии различных нуклеофилов как в кислотных, так и в основных условиях. Бензофеноны, которые образуют реактивные триплетные карбонильные соединения при облучении, часто требуют длительных периодов облучения, что может привести к неспецифическому мечениям, и, кроме того, часто инертны по отношению к различным полярным растворителям. Арилазиды требуют облучения с низкой длиной волны, что может повредить исследуемые биологические макромолекулы.
Диазирины широко используются в исследованиях мечения рецепторов. Это связано с тем, что диазиринсодержащие аналоги различных лигандов можно синтезировать и инкубировать с соответствующими рецепторами, а затем подвергать воздействию света для получения реактивных карбенов. Карбен будет ковалентно связываться с остатками в сайте связывания рецептора. Соединение карбена может включать биоортогональную метку или маркер, с помощью которого можно выделить интересующий белок. Затем белок можно расщепить и секвенировать с помощью масс-спектрометрии, чтобы определить, с какими остатками связан карбенсодержащий лиганд, и, следовательно, идентичность сайта связывания в рецепторе.
Примеры диазиринов, используемых в исследованиях мечения рецепторов, включают:


Аналогичным образом с меткой рецептора, диазиринсодержащие соединения, которые являются аналогами природных субстратов, также использовались для идентификации связывающих карманов ферментов. Примеры включают:

Диазирины также использовались в экспериментах по фотоаффинному маркированию нуклеиновых кислот. Примеры включают:


Диазирины также использовались для изучения липидных взаимодействий белков, например взаимодействия различных сфинголипидов с белками in vivo.