Соединения свинца существуют в двух основных степенях окисления: +2 и +4. Первое встречается чаще. Неорганические соединения свинца (IV) обычно являются сильными окислителями или существуют только в очень кислых растворах.
Различные окисленные формы свинца легко восстанавливаются до металла. Примером является нагревание PbO с мягкими органическими восстановителями, такими как глюкоза. Смесь оксида и сульфида, нагретая вместе, также образует металл.
Металлический свинец подвергается воздействию (окислению) воздухом только на поверхности, образуя тонкий слой оксида свинца. что защищает его от дальнейшего окисления. Металл не подвергается воздействию серной или соляной кислот. Он растворяется в азотной кислоте с выделением газа оксида азота с образованием растворенного Pb (NO 3)2.
При нагревании с нитратами щелочных металлов металлический свинец окисляется с образованием PbO (также известного как глет ), оставляя соответствующий щелочной нитрит. PbO является представителем степени окисления свинца +2. Он растворим в азотной и уксусной кислотах, из которых можно осаждать галогенид, сульфат, хромат, карбонат (PbCO 3) и основной карбонат (Pb. 3( ОН). 2(CO. 3). 2) соли свинца. Сульфид также может быть осажден из растворов ацетата. Все эти соли плохо растворимы в воде. Среди галогенидов иодид менее растворим, чем бромид, который, в свою очередь, менее растворим, чем хлорид.
Оксид свинца (II) также растворим в гидроксиде щелочного металла гидроксиде решения для формирования кор реагирующая соль плюмбита.
Хлорирование растворов плюмбита вызывает образование +4 окисления свинца штат.
Диоксид свинца является представителем степени окисления +4, и является сильным окислителем. Хлорид этой степени окисления образуется с трудом и легко разлагается на хлорид свинца (II) и газообразный хлор. Бромид и йодид свинца (IV) неизвестны. Диоксид свинца растворяется в растворах гидроксида щелочного металла с образованием соответствующих плюмбатов.
Также свинец имеет оксид со смешанными степенями окисления +2 и +4, красный свинец (Pb. 3O. 4), также известный как миний.
Свинец легко образует эквимолярный сплав с металлом натрия, который реагирует с алкилгалогенидами с образованием металлоорганических соединений свинца, таких как тетраэтилсвинец..
Известны три оксида: PbO, Pb3O4 (иногда называемый «миниевым») и PbO 2. Первый имеет два аллотропа: α-PbO и β-PbO, оба со слоистой структурой и тетракоординированным свинцом. Альфа-аллотроп имеет красный цвет и имеет расстояние Pb – O 230 пм; бета-аллотроп имеет желтый цвет и имеет расстояние Pb – O 221 и 249 пм (из-за асимметрии). Благодаря сходству, оба аллотропа могут существовать в стандартных условиях (бета с небольшими (10 относительными) примесями, такими как Si, Ge, Mo и т. Д.). PbO реагирует с кислотами с образованием солей и со щелочами с образованием плюмбитов, [Pb (OH) 3 ] или [Pb (OH) 4].
. Диоксид может быть получен, например, путем галогенизации свинца. (II) соли. Альфа-аллотроп - это ромбоэдрический, а бета-аллотроп - тетрагональный. Оба аллотропа имеют черно-коричневый цвет и всегда содержат некоторое количество воды, которую невозможно удалить, поскольку нагревание также вызывает разложение (до PbO и Pb 3O4). Диоксид - мощный окислитель: он может окислять соляную и серную кислоты. Он не реагирует с щелочным раствором, но реагирует с твердыми щелочами с образованием гидроксиплюмбатов или с основными оксидами с образованием свинца.
Реакция свинца с серой или сероводородом дает сульфид свинца. Твердое вещество имеет структуру, подобную NaCl (простая кубическая), которую оно сохраняет до температуры плавления 1114 ° C (2037 ° F). Если нагревание происходит в присутствии воздуха, соединения разлагаются с образованием моноксида и сульфата. Эти соединения практически нерастворимы в воде, слабых кислотах и растворе (NH 4)2S / (NH 4)2S2), который является ключевым для отделения свинца от аналитических элементов I – III групп, олова, мышьяка и сурьмы. Соединения растворяются в азотной и соляной кислотах, чтобы получить элементарную серу и сероводород соответственно. Нагревание смесей моноксида и сульфида приводит к образованию металла.
При нагревании карбоната свинца с фтористым водородом образуется гидрофторид, который при плавлении разлагается до дифторида. Этот белый кристаллический порошок более растворим, чем дииодид, но хуже, чем дибромид и дихлорид. Координированных фторидов свинца не существует (кроме нестабильный катион PbF). Тетрафторид, желтый кристаллический порошок, нестабилен.
Другие дигалогениды получаются при нагревании солей свинца (II) с галогенидами других металлов; дигалогениды свинца выпадают в осадок с образованием белого орторомбического соединения кристаллы (дииодидная форма желтого гексагональные кристаллы). Их также можно получить путем прямой реакции элементов при температуре, превышающей точки плавления дигалогенидов. Их растворимость увеличивается с температурой; добавление большего количества галогенидов сначала снижает растворимость, но затем увеличивается из-за комплексообразования с максимальным координационным числом, равным 6. Комплексообразование зависит от числа галогенидных ионов, атомного номера щелочного металла, добавляемый галогенид, температура и ионная сила раствора. Тетрахлорид получают при растворении диоксида в соляной кислоте; для предотвращения экзотермического разложения его выдерживают в концентрированной серной кислоте. Тетрабромид может не существовать, а тетраиодида определенно не существует. Также был получен диастатид.
Металл не подвергается воздействию серной или соляной кислот. Он растворяется в азотной кислоте с выделением газа оксида азота с образованием растворенного Pb (NO 3)2. Это хорошо растворимое твердое вещество в воде; таким образом, это ключ к получению осадков. из галогенида, сульфата, хромата, карбоната и основного карбоната Pb 3 (OH) 2 (CO 3)2соли свинца.
 Диаграмма, показывающая формы свинца в хлоридной среде.
Диаграмма, показывающая формы свинца в хлоридной среде. Свинец (II) образует серию комплексов с хлорид, образование которого изменяет химический состав свинца, вызывающего коррозию. Это будет ограничивать растворимость свинца в солевой среде.
| Pb + Cl → PbCl | K1= 12,59 |
| PbCl + Cl → PbCl 2 | K2= 14,45 |
| PbCl 2 + Cl → PbCl 3 | K3= 3,98 × 10 |
| PbCl 3 + Cl → PbCl 4 | K4= 8,92 × 10 |
Самыми известными соединениями являются два простейших плюмбана дератива: тетраметилсвинец (TML) и тетраэтил свинец (ТЕЛ); однако их гомологи, а также (HEDL) обладают меньшей стабильностью. Тетралкильные деративы содержат свинец (IV); связи Pb – C ковалентны. Таким образом, они напоминают типичные органические соединения.
Свинец легко образует эквимолярный сплав с металлом натрия, который взаимодействует с алкилгалогенидами с образованием металлоорганических соединений свинец, такой как тетраэтилсвинец. Энергии связи Pb – C в TML и TEL составляют всего 167 и 145 кДж / моль; соединения, таким образом, разлагаются при нагревании, и первые признаки состава TEL наблюдаются при 100 ° C (210 ° F). Пиролиз дает элементарный свинец и алкильные радикалы; их взаимодействие вызывает синтез HEDL. Они также разлагаются под воздействием солнечного света или ультрафиолетового излучения. В присутствии хлора алкилы начинают замещаться хлоридами; R 2 PbCl 2 в присутствии HCl (побочный продукт предыдущей реакции) приводит к полной минерализации с образованием PbCl 2. Реакция с бромом следует тому же принципу.
Сульфат свинца (II) плохо растворим, что можно увидеть на следующей диаграмме, показывающей добавление SO 4 к раствору, содержащему 0,1 М Pb. PH раствора составляет 4,5, как и выше, концентрация Pb никогда не может достигнуть 0,1 М из-за образования Pb (OH) 2. Обратите внимание, что растворимость Pb снижается в 10000 раз, когда SO 4 достигает 0,1 М.
 |  |
| График, показывающий водную концентрацию растворенного Pb как функцию SO 4 | Диаграмма для свинца в сульфатной среде |
Добавление Хлорид может снизить растворимость свинца, хотя в богатой хлоридом среде (такой как царская водка ) свинец может снова стать растворимым в виде анионных хлорокомплексов.
 | 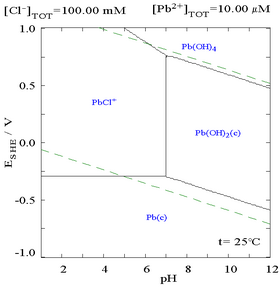 |
| Диаграмма, показывающая растворимость свинца в хлоридной среде. Концентрации свинца представлены в виде функции от общего количества хлоридов. | Диаграмма Пурбе для свинца в хлоридной (0,1 М) среде |
Полянский Н.Г. (1986)). Филлипова Н.А. (ред.). Аналитическая химия элементов: Свинец [Аналитическая химия элементов: Свинец]. Наука. CS1 maint: ref = harv (ссылка )