 | |
 | |
| Имена | |
|---|---|
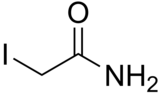
| Предпочтительное название IUPAC 2-йодацетамид | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChEMBL |
|
| ChemSpider | |
| ECHA InfoCard | 100.005.119 |
| Номер EC |
|
| IUPHAR / BPS | |
| PubChem CID | |
| номер RTECS |
|
| UNII | |
| CompTox Dashboard (EPA ) | |
InChI
| |
SMILES
| |
| Свойства | |
| Химическая формула | C2H4INO |
| Молярная масса | 184,964 г · моль |
| Внешний вид | белые кристаллы (желтый цвет указывает на присутствие йода) |
| Температура плавления | 94 ° C (201 ° F; 367 K) |
| Опасности | |
| Паспорт безопасности | MSDS 1, MSDS 2 |
| NFPA 704 (огненный алмаз) |  0 3 1 0 3 1 |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобокс | |
2-йодацетамид представляет собой алкилирующий агент, используемый для целей картирования пептида. Его действие аналогично действию йодацетата. Его обычно используют для ковалентного связывания с тиольной группой цистеина, поэтому белок не может образовывать дисульфидные связи. Также используется в исследованиях убиквитина в качестве ингибитора ферментов деубиквитиназы (DUBs), поскольку он алкилирует остатки цистеина в активном центре DUB.
Йодацетамид является необратимым ингибитором всех цистеиновых пептидаз, с механизм ингибирования, происходящий от алкилирования каталитического остатка цистеина (см. схему). По сравнению с его кислотным производным, йодацетатом, йодацетамид реагирует значительно быстрее. Это наблюдение противоречит стандартной химической реакционной способности, однако наличие благоприятного взаимодействия между положительным ионом имидазолия каталитического гистидина и отрицательно заряженной карбоксильной группой иодацетата является причиной повышенной относительной активности йодацетамида.
 Механизм. необратимого ингибирования цистеинпептидаз йодацетамидом.
Механизм. необратимого ингибирования цистеинпептидаз йодацетамидом. Он обычно используется во время подготовки проб для de novo (пептидного) секвенирования с помощью масс-спектрометрии белков, но недавние критики Предлагаем избегать его использования