Тест Грисса - это аналитический химический тест, который определяет присутствие нитрит-иона в растворе. Одно из наиболее важных применений - определение нитритов в питьевой воде. Реакция Грисса диазотирования, на которой основан реагент Грисса, была впервые описана в 1858 году Питером Гриссом. Этот тест также широко используется для обнаружения нитратов, которые являются обычным компонентом взрывчатых веществ, поскольку они могут быть преобразованы в нитриты и обнаружены с помощью теста Грисса.
Нитрит обнаруживается и анализируется по образованию красно-розового цвета при обработке нитритсодержащего образца реагентом Грисса, который состоит из двух компонентов. в кислом растворе: производное анилина и связующий агент. В наиболее распространенных вариантах используются сульфаниламид и N- (1-нафтил) этилендиамин : типичный коммерческий реагент Грисса содержит 0,2% N- (1-нафтил) этилендиамина дигидрохлорида и 2% сульфаниламид в 5% фосфорной кислоте. Этот диамин используется вместо более простого и дешевого 1-нафтиламина, поскольку последний является сильнодействующим канцерогеном, и, кроме того, диамин образует более полярный и, следовательно, гораздо более растворимый краситель в кислой водной среде. Другие применяемые производные анилина включают сульфаниловую кислоту, нитроанилин и п-аминоацетофенон.
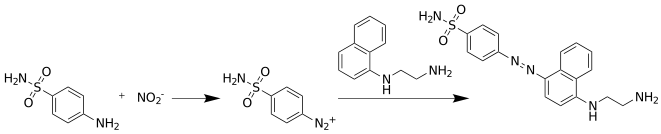
Тест Грисса включает две последовательные реакции. Когда добавляется сульфаниламид, ион нитрита реагирует с ним в реакции диазотирования Грисса с образованием соли диазония, которая затем реагирует с N- (1-нафтил) этилендиамином в азосочетании реакция с образованием розово-красного азокрасителя.
. Используя спектрофотометр, можно количественно определить концентрацию нитрита. Предел обнаружения теста Грисса обычно составляет от 0,02 до 2 мкМ, в зависимости от точных сведений о конкретных компонентах, используемых в реагенте Грисса.
Тест использовался в судебно-медицинская экспертиза в течение многих лет проверяет наличие следов нитроглицерина. Каустическая сода используется для разрушения пробы, содержащей нитроглицерин, с образованием нитрит-ионов.
Испытание включает взятие пробы с эфиром и разделение его на две чаши. В первую емкость добавляется каустическая сода, затем реагент Грисса; если раствор станет розовым в течение десяти секунд, это указывает на присутствие нитритов. Сам тест считается положительным, если после добавления во вторую емкость только реактива Грисса раствор остается прозрачным.
Осуждению Джудит Уорд и Бирмингемской шестерки способствовала неправильная интерпретация результатов теста Грисса Фрэнком Скузом.