 Катион бензолдиазония
Катион бензолдиазония Соединения диазония или соли диазония представляют собой группу органических соединения, имеющие общую функциональную группу R-N. 2X., где R может быть любой органической группой, такой как алкил или арил, и X представляет собой неорганический или органический анион, такой как галоген.
Согласно табличным константам линейной зависимости свободной энергии (например, Hammett σ m и σ p), диазониевая группа (N 2) является одним из наиболее сильно акцептирующих электронов заместителей. Таким образом, α-положение разновидностей алкандиазония и кислотных протонов на диазонио-замещенных фенолах и бензойных кислотах значительно снижает значения pK a по сравнению с их незамещенными аналогами. Например, водный pK a метандиазония оценивается как <10, while that of the phenolic proton of 4-hydroxybenzenediazonium was measured to be 3.4.
. С точки зрения реакционной способности, химический состав солей диазония определяется их склонностью к дедиазотированию посредством термодинамических (энтальпических и энтропийных) благоприятное вытеснение газообразного азота. Реакция (MeN 2 → Me + N 2) имеет изменение энтальпии 43 ккал / моль, в то время как (EtN 2 → Et + N 2) имеет изменение энтальпии 11 ккал / моль. Для вторичных и третичных разновидностей алкандиазония энтальпическое изменение рассчитано как близкое к нулю или отрицательное, с минимальным активационным барьером для удаления азота. Следовательно, вторичные и (особенно) третичные виды алкандиазония являются либо несвязанными, несуществующими видами, либо, в лучшем случае, чрезвычайно быстротечными промежуточными продуктами.

Карбоксилат метилдиазония считается мимолетным промежуточным продуктом в метилировании карбоновых кислот диазометаном, и разновидности алкандиазония, образующиеся при диазотировании аминов, изучались в исследованиях физической органической химии. Однако соли алкандиазония в остальном синтетически не важны из-за их экстремальной и неконтролируемой реакционной способности S N 2 / S N 1 / E1.
Напротив, соли арендиазония более стабильны, хотя все еще опасно взрывоопасны при определенных условиях, поскольку S N 2 геометрически невозможен и не встречается, в то время как S N 1 возникает с гораздо большей трудностью по сравнению с разновидностями алкандиазония из-за трудности образования высокоэнергетического арильного катиона и более сильной связи C (sp) –N по сравнению со связью C (sp) –N в соединениях алкандиазония. Обычно хлоридную соль получают при 5 ° C из анилина и NaNO 2 / водн. HCl и соли ArN 2 Cl имеют тенденцию к разложению (иногда со взрывом) при более высоких температурах. Однако использование редокс-неактивных и объемных HSO 4, BF 4 или TsO в качестве противоанионов позволило хранить соли арендиазония неограниченное время при 0 ° C и безопасно обращаться с ними в течение коротких периодов времени. время при температуре до 50 ° С. Соли арендиазония в некоторых случаях подвергаются S N 1 (Ar) (диссоциативное мономолекулярное нуклеофильное ароматическое замещение), тогда как большинство их реакций протекает с S RN 1 (Ar) ( диссоциативное радикальное нуклеофильное ароматическое замещение), при котором происходит начальный перенос электрона, что позволяет образовывать арильный радикал, а не катион.
Соли арендиазония - исключительно универсальные реагенты для химического синтеза. Поскольку арильные радикалы и катионы обладают высокой электрофильностью и будут реагировать практически с любым нуклеофильным реагентом, соли арендиазония образуют «транзитный узел» для химии аренов, из которого можно получить почти любое другое ароматическое производное. Более того, эта полезность подчеркивается их доступностью: соли арендиазония легко доступны в результате диазотирования ариламинов (анилинов и гетероариламинов), которые, в свою очередь, получают из исходного арена электрофильным нитрованием с последующим опосредованным или катализируемым металлом восстановлением. После электрофильного ароматического замещения химия диазония является наиболее часто применяемой стратегией для получения ароматических соединений.
В промышленности соли арендиазония являются важными промежуточными продуктами в органическом синтезе азокрасителей.
Процесс образования соединений диазония называется «диазотированием», «диазонирование» или «диазотирование». Впервые об этой реакции сообщил Питер Грисс в 1858 году, который впоследствии открыл несколько реакций этого нового класса соединений. Чаще всего соли диазония получают обработкой ароматических аминов азотистой кислотой и дополнительной кислотой. Обычно азотистая кислота образуется in situ (в той же колбе) из нитрита натрия и избытка минеральной кислоты (обычно водная HCl, H 2SO4, pH 3CC6H4SO3H, или HBF 4):
 Образец тетрафторбората бензолдиазония.
Образец тетрафторбората бензолдиазония. Водные растворы солей диазония хлорида, традиционно получаемые из анилина, нитрита натрия и хлористоводородной кислоты. получают при 0-5 ° C.Однако можно выделить соединения диазония в виде солей тетрафторбората или тозилата, которые являются стабильными твердыми веществами при комнатной температуре. Часто предпочтительно, чтобы соль диазония оставалась в растворе, но они имеют тенденцию перенасыщать. Операторы имеют он был ранен или даже убит в результате неожиданной кристаллизации соли с последующей ее детонацией.
Из-за этих опасностей соединения диазония обычно не выделяются. Вместо этого они используются на месте. Этот подход проиллюстрирован на примере получения аренсульфонильного соединения:

Наиболее широко применяемой реакцией диазониевых солей является азосочетание. В этом процессе соединение диазония атакуется богатыми электронами субстратами, т.е. соединяется с ними. Когда партнерами связывания являются арены, такие как анилины и фенолы, процесс является примером электрофильного ароматического замещения :
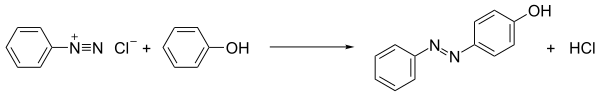
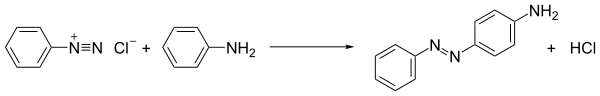
Другим коммерчески важным классом связывающих партнеров являются ацетоуксусные амиды, что проиллюстрировано получением пигмента желтого 12, дневника. 293>Полученные азосоединения часто являются полезными красителями и фактически называются азокрасителями. Глубокие цвета красителей отражают их расширенное конъюгацию. Например, краситель, называемый анилиновый желтый, получают путем смешивания анилина и холодного раствора соли диазония и затем его энергичного встряхивания. Анилиновый желтый получают в виде твердого вещества желтого цвета. Аналогичным образом, холодный щелочной раствор Нафтал en-2-ol (бета-нафтол) дает интенсивный оранжево-красный осадок. Метиловый оранжевый является примером азокрасителя, который используется в лаборатории в качестве индикатора pH.
Катионы арендиазония претерпевают несколько реакций, в которых группа N 2 замещается другой группой или ионом. Некоторые из основных из них следующие.
Пара катионов диазония может быть соединена с образованием биарилов. Это превращение иллюстрируется сочетанием соли диазония, полученной из антраниловой кислоты, с получением дифеновой кислоты ((C 6H4CO2H)2). В родственной реакции, та же соль диазония претерпевает потерю N 2 и CO 2 с образованием бензина.
Хлорид бензолдиазония, нагретый с хлоридом меди или бромидом одновалентной меди, соответственно растворенными в HCl или HBr, дает хлорбензол или бромбензол соответственно.

Реакция Гаттермана хлорид бензолдиазония нагревают с медным порошком и HCl или HBr для получения хлорбензола и бромбензола соответственно. изд. в честь немецкого химика Людвига Гаттермана.


Йод нелегко ввести непосредственно в бензольное кольцо. Однако его можно ввести путем обработки катионов арендиазония йодидом калия :
Фторбензол получается термическим разложением бензолдиазония. Конверсия фторбората Реакция Бальца-Шимана.
![{\displaystyle {\ce {[C6H5N+2]BF4- ->C6H5F + BF3 + N2}}}]( https://wikimedia.org/api/rest_v1/media/ math / render / svg / 98854fdc1405b490fdd0d68f060887ff90168c5b )
Традиционная реакция Бальца – Шимана была предметом множества мотивов, например с использованием гексафторфосфатов (PF 6) и гексафторантимоната (SbF 6) вместо тетрафторборатов. Диазотирование можно проводить с помощью солей нитрозония, таких как [NO] SbF 6.
Катионы арендиазония, восстановленные гипофосфористой кислотой, этанол или станнит натрия дает бензол:
![{\displaystyle {\ce {[C6H5N2+]Cl- + H3PO2 + H2O ->C6H6 + N2 + H3PO3 + HCl}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ae4fe80352442662e0e0ea86f444c2e7e154a36a)
![{\displaystyle {\ce {[C6H5N2+]Cl- + CH3CH2OH ->C6H6 + N2 + CH3CHO + HCl}}}]( https://wikimedia.org/api/rest_v1/media/math/render/ svg / 1fd6aff8b1cca4b87fa0f2eb030d2df4b7521ff8 )
Фенолы ар образуется при нагревании водных растворов солей арендиазония:
Эта реакция носит немецкое название Phenolverkochung (« варка с получением фенолов »). Образовавшийся фенол может реагировать с солью диазония, и, следовательно, реакция протекает в присутствии кислоты, которая подавляет эту дальнейшую реакцию. Гидроксилирование по типу Сандмейера также возможно с использованием Cu 2 O и Cu в воде.
Нитробензол может быть получено путем обработки бензолдиазонийфторбората нитритом натрия в присутствии меди. Альтернативно, диазотирование анилина может проводиться в присутствии закиси меди, которая генерирует нитрит меди in situ:

Цианогруппа обычно не может быть введена нуклеофильным замещением галоаренов, но такие соединения можно легко получить из солей диазония.Примером является получение бензонитрила с использованием реагента цианид меди :

Эта реакция представляет собой особый тип реакции Сандмейера.
Две исследовательские группы сообщили о трифторметилировании солей диазония в 2013 году. Гуссен сообщил о получении Комплекс CuCF 3 из CuSCN, TMSCF 3 и Cs 2CO3. Напротив, Fu сообщил о трифторметилировании с использованием реагента Умемото (S-трифторметилдибензотиофения тетрафторборат) и порошка Cu (условия типа Гаттермана). Их можно описать следующим уравнением:
![{\displaystyle {\ce {C6H5N2+ + [CuCF3] ->C6H5CF3 + [Cu] + + N2}}}]( https: //wikimedia.org/api/rest_v1/media/math/render/svg/186b334438ab68ac9d7c76d6da6d2c60b3bbf50d)
Скобка указывает на то, что другие лиганды на меди, вероятно, присутствуют, но опущены.
Соли диазония могут быть превращены в тиолы с помощью двухэтапной процедуры. Обработка хлорида бензолдиазония этилксантатом калия с последующим гидролизом промежуточного сложного эфира ксантогената дает тиофенол :


Арильная группа может быть соединена с другой с помощью арендиазония. Например, обработка хлорида бензолдиазония бензолом (ароматическим соединением) в присутствии гидроксида натрия дает дифенил :
![{\displaystyle {\ce {[C6H5N2+]Cl- + C6H6 ->C6H5-C6H5 + N2 + HCl}}}]( https://wikimedia.org/api/rest_v1/media/math/render/svg/62f872781ba025ad2794380235783323c9a464c9 )
Эта реакция известна как реакция Гомберга-Бахмана. Подобное превращение также достигается обработкой хлорида бензолдиазония этанолом и порошком меди.
Группа Bpin (пинаколатобор), используемая в реакциях кросс-сочетания Сузуки-Мияура, может быть установлена реакцией диазониевой соли с бис (пинаколато) дибороном в присутствии бензоила пероксид (2 мол.%) в качестве инициатора:
Хлорид бензолдиазония реагирует с соединениями, содержащими активированные двойные связи, с образованием фенилированных продуктов. Реакция называется арилирование Меервейна :
![{\displaystyle {\ce {[C6H5N+2]Cl- + ArCH=CHCOOH ->ArC = C-C6H5 + N2 + CO2 + HCl}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c56c56d4d1da0b2573f3464b3f344c9c72cbf35e)
В своих реакциях с комплексами металлов катионы диазония ведут себя аналогично NO. Например, комплексы низковалентных металлов присоединяются к солям диазония. Иллюстративные комплексы: [Fe (CO) 2 (PPh 3)2(N2Ph) ] и хиральный металлический комплекс Fe (CO) (NO) (PPh 3) (N 2 Ph).
В потенциальном применении в нанотехнологии, соли диазония 4-хлорбензолдиазония тетрафторборат очень эффективно функционализируют одностенные нанотрубки. Для получения нанотрубок их смешивают с ионной жидкостью в ступке пестиком. Соль диазония добавляется вместе с карбонатом калия, и после измельчения смеси при комнатной температуре поверхность нанотрубок покрывается хлорфенильными группами с эффективностью 1 из 44 атомов углерода. Эти добавленные заместители предотвращают образование тесных пучков трубок из-за больших сил сцепления между ними, что является повторяющейся проблемой в технологии нанотрубок.
Также возможно функционализировать кремниевые пластины солями диазония, образующими монослой арил. В одном исследовании поверхность кремния промывалась фтористым водородом аммония, оставаясь покрытой кремний-водородными связями (гидридная пассивация). Реакция поверхности с раствором соли диазония в ацетонитриле в течение 2 часов в темноте представляет собой спонтанный процесс через свободнорадикальный механизм :
Пока что прививка Соли диазония на металлах были получены на железе, кобальте, никеле, платине, палладии, поверхности цинка, меди и золота. Сообщалось также о прививке к алмазным поверхностям. Возникает один интересный вопрос - фактическое расположение арильной группы на поверхности. Исследование in silico демонстрирует, что в период 4 элемента от титана до меди энергия связи уменьшается слева направо, потому что количество d-электронов увеличивается. Металлы слева от железа расположены под наклоном или плоско на поверхности, способствуя образованию связи пи между металлом и углеродом, а металлы справа от железа располагаются в вертикальном положении, предпочитая металл углероду образование сигма-связи. Это также объясняет, почему прививка диазониевой соли до сих пор была возможна с теми металлами, которые расположены справа от железа в периодической таблице.
Соли диазония могут быть восстановлены с помощью олова. хлорид (SnCl 2) к соответствующим производным гидразина. Эта реакция особенно полезна в синтезе индола по Фишеру, триптановых соединений и индометацина. Использование дитионита натрия является усовершенствованием по сравнению с хлоридом олова, поскольку это более дешевый восстановитель с меньшими экологическими проблемами.
Ионы алкандиазония, которые редко встречаются в органической химии, участвуют в качестве возбудителей канцерогенов. В частности, считается, что нитрозамины подвергаются метаболической активации с образованием разновидностей алкандиазония.
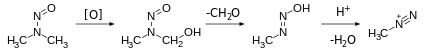 Метаболическая активация нитрозамина NDMA, включая его превращение в алкилирующий агент.
Метаболическая активация нитрозамина NDMA, включая его превращение в алкилирующий агент. Первое применение солей диазония заключалось в производстве водостойких окрашенных тканей путем погружения ткани в водный раствор. соединения диазония с последующим погружением в раствор связующего (богатое электронами кольцо, которое подвергается электрофильному замещению). Основное применение соединений диазония остается в производстве красителей и пигментов.
Соединения диазония являются стандартными реагентами, используемыми в синтезе органических соединений, особенно арильных производных.
Соли диазония чувствительны к свету и разрушаются под воздействием около УФ или фиолетового света. Это свойство привело к их использованию при воспроизведении документов. В этом процессе бумага или пленка покрываются солью диазония. После контактного воздействия на свету остаточный диазокраситель с водным раствором связующего вещества превращается в стабильный азокраситель. В более распространенном процессе используется бумага, покрытая диазо, связующим веществом и кислотой для предотвращения связывания; после экспонирования изображение проявляется паровой смесью аммиака и воды, которая усиливает сцепление.
Твердые галогениды диазония часто опасно взрывоопасны, и сообщалось о смертельных случаях и травмах.
Природа анионов влияет на стабильность соли. Перхлораты арендиазония, такие как перхлорат нитробензолдиазония, использовались для инициирования взрывчатых веществ.
реакция диазосочетания