 Химическая структура азокрасителя оранжевого цвета.
Химическая структура азокрасителя оранжевого цвета. Азокрасители представляют собой органические соединения, содержащие функциональную группу R-N = N-R ', в которой R и R' обычно представляют собой арил. Они представляют собой коммерчески важное семейство азосоединений, то есть соединений, содержащих связь CN = NC. Азокрасители широко используются для обработки текстильных изделий, кожаных изделий и некоторых пищевых продуктов. Химически связанные с азо - красители азо пигменты, которые являются нерастворимыми в воде и других растворителях.
Известно много видов азокрасителей и существует несколько систем классификации. Некоторые классы включают дисперсные красители, металлокомплексные красители, реактивные красители и основные красители. Основные красители, также называемые прямыми красителями, используются для текстильных изделий на основе целлюлозы, в том числе для хлопка. Красители связываются с тканью неэлектростатическими силами. Согласно другой классификации азокрасители могут быть классифицированы по количеству азогрупп.
 Трипановый синий является примером прямого красителя, используемого для хлопка.
Трипановый синий является примером прямого красителя, используемого для хлопка. В результате п- делокализации арилазосоединения имеют яркие цвета, особенно красные, оранжевые и желтые. Примером может служить Disperse Orange 1. Некоторые азосоединения, например метиловый оранжевый, используются в качестве кислотно-основных индикаторов. Большинство дисков DVD-R / + R и некоторые CD-R используют синий азокраситель в качестве записывающего слоя.
 Многие фенольные диазокрасители участвуют в таутомерных равновесиях, показанных здесь в упрощенной форме (Ar = арил).
Многие фенольные диазокрасители участвуют в таутомерных равновесиях, показанных здесь в упрощенной форме (Ar = арил). Азокрасители твердые. Большинство из них представляют собой соли, причем окрашенным компонентом обычно является анион, хотя известны некоторые катионные азокрасители. Анионный характер большинства красителей обусловлен присутствием 1-3 групп сульфоновой кислоты, которые полностью ионизируются при pH окрашенного изделия:
Большинство белков являются катионными, поэтому окрашивание кожи и шерсти соответствует реакции ионного обмена. Анионный краситель прилипает к этим изделиям за счет электростатических сил. Катионные азокрасители обычно содержат центры четвертичного аммония.
Большинство азокрасителей получают путь азосочетания, что влечет за собой реакцию электрофильного замещения в качестве диазонии катиона арил с другим соединения, партнером связывания. Классическими партнерами по связыванию являются другие ароматические соединения с электронодонорными группами:
На практике ацетоуксусные амиды широко используются в качестве партнеров связывания:
Азокрасители также получают конденсацией нитроароматических соединений с анилинами с последующим восстановлением образующегося промежуточного азокси :
Для окрашивания текстиля типичным партнером нитросшивки будет 4,4'-динитростильбен-2,2'-дисульфонат динатрия. Типичные анилиновые партнеры показаны ниже. Поскольку анилины получают из нитросоединений, некоторые азокрасители получают путем частичного восстановления ароматических нитросоединений.
Многие азокрасители получают реакциями из уже существующих азосоединений. Типичные реакции включают образование комплексов с металлами и ацилирование.
Прямой коричневый 78
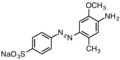
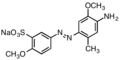
Basic Red 18, катионный азокраситель
Азопигменты похожи по химической структуре на азокрасители, но в них отсутствуют солюбилизирующие группы. Поскольку они нерастворимы практически во всех средах, их нелегко очистить, и поэтому требуются предшественники высокой степени очистки.
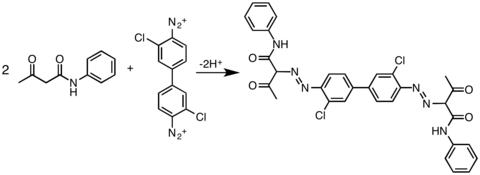 Синтез CI Pigment Yellow 12, азопигмента (также классифицируется как диарилидный пигмент ).
Синтез CI Pigment Yellow 12, азопигмента (также классифицируется как диарилидный пигмент ). Азопигменты играют важную роль в различных пластмассах, каучуках и красках (включая краски художников). Они обладают прекрасными окрашивающими свойствами, в основном в диапазоне от желтого до красного, а также хорошей светостойкостью. Светостойкость зависит не только от свойств органических азосоединений, но и от того, как они абсорбируются на носителе пигмента.
Чтобы красители были полезными, они должны обладать высокой степенью химической и фотолитической стабильности. В результате такой стабильности фотолиз не считается путем разложения азокрасителей. Чтобы продлить срок службы продуктов, окрашенных азокрасителями, важно обеспечить устойчивость к микробным атакам, и испытания показали, что азокрасители практически не разлагаются при кратковременных тестах в аэробных условиях. Однако в анаэробных условиях изменение цвета может наблюдаться как следствие биоразложения.
Многие азопигменты нетоксичны, хотя некоторые, такие как динитроанилин оранжевый, орто-нитроанилин оранжевый или пигмент оранжевый 1, 2 и 5, являются мутагенными и канцерогенными.
Азокрасители, производные бензидина, являются канцерогенами ; воздействие их традиционно связывают с раком мочевого пузыря. Соответственно, производство бензидиназокрасителей было прекращено в 1980-х годах во многих западных странах.
Некоторые азокрасители разлагаются в восстановительных условиях с высвобождением любого из группы определенных ароматических аминов. Потребительские товары, содержащие перечисленные ароматические амины, происходящие из азокрасителей, были запрещены к производству и продаже в странах Европейского Союза в сентябре 2003 года. Поскольку лишь небольшое количество красителей содержало такое же небольшое количество аминов, затронуто было относительно небольшое количество продуктов.