 | |
| Имена | |
|---|---|
| Имя ИЮПАК Бис (циклопентадиенил) ванадий | |
| Другие названия Ванадоцен | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ECHA InfoCard | 100.149.756 |
| PubChem CID | |
| UNII | |
| Панель управления CompTox (EPA ) | |
УЛЫБКА
| |
| Свойства | |
| Химическая формула | V (C 5H5)2 |
| Молярная масса | 181,128 г / моль |
| Внешний вид | Фиолетовый кристалл |
| Температура плавления | 167 ° C (333 ° F ; 440 K) |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
Ванадоцен, бис (η-циклопентадиенил) ванадий, представляет собой металлоорганическое соединение с формулой V (C 5H5)2, обычно сокращенно Cp 2 В. Это фиолетовое кристаллическое парамагнитное твердое вещество. Ванадоцен имеет относительно ограниченное практическое применение, но он широко изучен.
V (C 5H5)2- металлоцен, класс металлоорганических соединений, которые обычно имеют ион металла, расположенный между двумя циклопентадиенильными кольцами. В твердом состоянии молекула имеет симметрию D 5d. Центр ванадия (II) расположен на равном расстоянии между центром двух циклопентадиенильных колец в кристаллографическом центре инверсии. Среднее расстояние связи VC составляет 226 пм. Кольца Cp ванадоцена динамически разупорядочены при температурах выше 170 К и только полностью упорядочены. при 108 К.
ванадоцен был впервые получен в 1954 году Бирмингемом, Фишером и Уилкинсоном путем восстановления дихлорида ванадоцена алюминием. гидрид, после чего ванадоцен был сублимирован в вакууме при 100 C. Современный синтез ванадоцена, который позволяет производить в более высоких количествах, требует обработки [V 2Cl3(THF) 6]2[Zn 2Cl6] с циклопентадиенилнатрий.
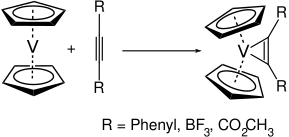
Ванадоцен - реактивная молекула. Поскольку он имеет только 15 валентных электронов, он легко реагирует со многими лигандами. С алкинами, например, он реагирует с образованием соответствующих комплексов ванадий-циклопропен.
В одной реакции участвует монооксид углерода, что приводит к ионному производному ванадоцена при проведении в инертной атмосфере:
Ванадоцен легко окисляется до монокатиона при обработке ферроцением соль в толуоле.
Эти монокатионы чрезвычайно чувствительны к воздуху и имеют окислительно-восстановительный потенциал -1,10 В.
Ванадоцен реагирует с высоким давлением окиси углерода с образованием CpV (CO) 4.