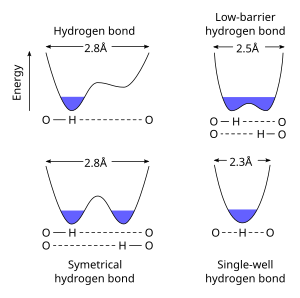
 Энергетические профили для различных типов водородных связей между гетероатомами кислорода. Стандартные водородные связи асимметричны, водород связан с одним гетероатомом. Когда pKa между гетероатомами равны, образуется симметричная водородная связь с водородом, находящимся в равновесии между двумя положениями. На более коротких расстояниях барьер между двумя энергетическими минимумами достаточно низок, чтобы водород был в равной степени связан в виде водородной связи с низким барьером или одноямной водородной связи.
Энергетические профили для различных типов водородных связей между гетероатомами кислорода. Стандартные водородные связи асимметричны, водород связан с одним гетероатомом. Когда pKa между гетероатомами равны, образуется симметричная водородная связь с водородом, находящимся в равновесии между двумя положениями. На более коротких расстояниях барьер между двумя энергетическими минимумами достаточно низок, чтобы водород был в равной степени связан в виде водородной связи с низким барьером или одноямной водородной связи. С низким барьером водородная связь ( LBHB) представляет собой особый тип водородной связи. LBHB могут возникать, когда pKa двух гетероатомов близко совпадают, что позволяет более равномерно распределять водород между ними. Это разделение водорода вызывает образование особенно коротких прочных водородных связей.
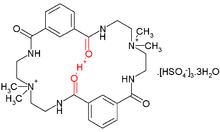 В этом макроциклическом соединении азакраун- типа протон находится между двумя амидно- карбонильными атомами кислорода, разделенными расстоянием 2,45 Å.
В этом макроциклическом соединении азакраун- типа протон находится между двумя амидно- карбонильными атомами кислорода, разделенными расстоянием 2,45 Å. Стандартные водородные связи длиннее (например, 2,8 Å для водородной связи O O), и ион водорода явно принадлежит одному из гетероатомов. Когда pKa гетероатомов близко согласованы, LBHB становится возможным на более коротком расстоянии (~ 2,55 Å). При дальнейшем уменьшении расстояния (lt;2,29 Å) связь характеризуется как одинарная или коротко-прочная водородная связь.
Водородные связи с низким барьером возникают в исключающих воду средах белков. Множественные остатки действуют вместе в системе реле заряда, чтобы контролировать значения pKa вовлеченных остатков. LBHB также встречаются на поверхности белков, но они нестабильны из-за их близости к объемной воде и противоречивых требований сильных солевых мостиков на границе раздела белок-белок.
Было высказано предположение, что низкобарьерные водородные связи важны для ферментативного катализа в двух типах обстоятельств. Во-первых, водородная связь с низким барьером в цепи реле заряда в активном центре может активировать каталитический остаток (например, между кислотой и основанием в каталитической триаде ). Во-вторых, образование LBHB могло бы образоваться во время катализа для стабилизации переходного состояния (например, с переходным состоянием субстрата в оксианионной дырке ). Оба эти механизма спорны, и теоретические и экспериментальные данные о том, имеют ли они место, расходятся. С 2000-х годов все пришли к единому мнению, что LBHB не используются ферментами для катализа. Однако в 2012 году было предложено, чтобы водородная связь с низким барьером участвовала в дискриминации фосфат-арсенат для фосфатного транспортного белка. Это открытие может указывать на возможность того, что водородные связи с низким барьером играют каталитическую роль в выборе размера ионов в некоторых очень редких случаях.