D-аминокислоты - это аминокислоты, где стереогенные углерод альфа к аминогруппе имеет D-конфигурацию. Для большинства встречающихся в природе аминокислот этот углерод имеет L-конфигурацию. D-аминокислоты чаще всего встречаются в природе в виде остатков в белках. Они образованы из остатков D-аминокислот, полученных из рибосом.

D-аланин.
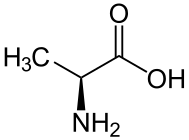
L-аланин.
L- и D-аминокислоты обычно являются энантиомерами. Исключение составляют две аминокислоты с двумя стереогенными центрами, треонин и изолейцин. За исключением этих двух особых случаев, L- и D-аминокислоты имеют идентичные свойства (цвет, растворимость, температура плавления) во многих условиях. Однако в биологическом контексте, который является хиральным, эти энатиомеры могут вести себя по-разному. Таким образом, D-аминокислоты имеют низкую питательную ценность отчасти потому, что они плохо перевариваются.
Два фермента превращают L-аминокислоты в D-аминокислоты. D- Аминокислотная рацемаза, PLP-зависимый фермент, рацемизирует аминокислоты посредством образования альфа-иминокислот, при этом стереогенный центр теряется. Оксидазы L-аминокислот превращают L-аминокислоты в альфа- кетокислоты, которые восприимчивы к восстановительному аминированию. Некоторые аминокислоты склонны к рацемизации, одним из примеров является лизин, который рацемизируется посредством образования пипеколиновой кислоты.
. В пептидах остатки L-аминокислот медленно рацемизируются, что приводит к образованию некоторого количества D -аминокислотные остатки. Рацемизация происходит за счет депротонирования метина, который является альфа по отношению к амидогруппе. Скорость увеличивается с увеличением pH.
Многие D-аминокислоты, обнаруженные в высших организмах, происходят из микробных источников. D-аланин в пептидогликанах, которые составляют стенки бактериальных клеток, помогает хозяину противостоять атакам протеолитических ферментов. Несколько антибиотиков, например бацитрацин, содержат остатки D-аминокислот.