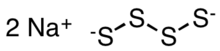 | |
| Имена | |
|---|---|
| Название IUPAC Тетрасульфид натрия | |
| Другие названия динатрийтетрасульфид, сульфид натрия | |
| Идентификаторы | |
| Номер CAS | |
| ECHA InfoCard | 100.031.628 |
| Номер EC |
|
| UNII | |
| CompTox Dashboard (EPA ) | |
| Свойства | |
| Химическая формула | Na2S4 |
| Молярная масса | 174,24 г / моль |
| Внешний вид | Темно-красный, слегка вязкий жидкий или желтый кристаллический порошок |
| Плотность | 1,268 г / см при 15,5 ° C |
| Температура плавления | 275 ° C (527 ° F; 548 K) |
| Растворимость в воде | Растворим в вода |
| Опасности | |
| Основные опасности | Стабилен при комнатной температуре, но может быть взрывоопасным при нагревании. Реакции с кислотами или окислителями приводят к образованию газообразных побочных продуктов, которые могут быть опасны при вдыхании. |
| Данные по безопасности лист | [1] |
| NFPA 704 (огненный алмаз) |  1 3 1 1 3 1 |
| Самовоспламенение. температура | Неприменимо |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
Тетрасульфид натрия представляет собой неорганическое соединение с формулой Na 2S4. Это желто-оранжевое твердое вещество, растворяющееся при гидролизе в воде. Они являются предшественниками некоторых специальных полимеров и промежуточных продуктов в прототипах натрий-серной батареи.
Он получается в результате реакции между элементарной серой и гидросульфидом натрия в спиртовом растворе:
Полисульфидные анионы имеют зигзагообразные цепочки атомов серы. Расстояния SS составляют около 2,05 Å, а двугранные углы SSSS составляют около 90 °.
При обработке кислотой он превращается в сероводород и элементарная сера. Обработка алкилирующими агентами дает органические полисульфиды. В одном коммерческом применении его используют для получения сшивающего агента бис (триэтоксисилилпропил) тетрасульфида :
Иногда в виде смеси с другими полисульфидами тетрасульфид натрия используется для получения полимера, называемого тиоколом. Реакция включает алкилирование этиленхлоридом :
Эти материалы имеют приблизительную формулу (C 2H4)Sx]n(x ~ 4), обладают высокой устойчивостью к разрушению под действием растворителей и кислот.