Есть три набора галогенидов индия, тригалогенидов, моногалогенидов и нескольких промежуточных галогенидов. В моногалогенидах степень окисления индия равна +1, и их собственными названиями являются фторид индия (I), хлорид индия (I), бромид индия (I) и иодид индия (I).
Промежуточные галогениды содержат индий со степенью окисления , +1, +2 и +3.
Во всех тригалогенидах степень окисления индия составляет +3, а их собственные названия - фторид индия (III), хлорид индия (III), бромид индия (III) и иодид индия (III). Тригалогениды являются кислотой Льюиса. Трихлорид индия является отправной точкой в производстве триметилиндия, который используется в полупроводниковой промышленности.
InF 3 представляет собой белое кристаллическое твердое вещество с т.пл. 1170 ° C. В его состав входит 6-координатный индий.
InCl 3 представляет собой белое кристаллическое твердое вещество, т.пл. 586 ° C. Он имеет ту же структуру, что и AlCl 3.
InBr 3 представляет собой бледно-желтое кристаллическое твердое вещество, т.пл. 435 ° С. Он имеет ту же структуру, что и AlCl 3. InBr 3 находит некоторое применение в органическом синтезе в качестве водостойкой кислоты Льюиса.
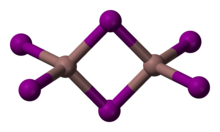 Шаровидная модель В 2I6молекула
Шаровидная модель В 2I6молекула InI 3 представляет собой окрашенное кристаллическое твердое вещество, обычно описываемое как оранжевое. Известны отчетливые желтые и красные формы. Красная форма превращается в желтую при 57 ° C. Структура красной формы не была определена с помощью рентгеновской кристаллографии, однако спектроскопические данные указывают на то, что индий может иметь шести координаты. Желтая форма состоит из In 2I6с 4 координатными центрами индия. Он используется в качестве «геттера йодида» в процессе Cativa.
Известно удивительное количество промежуточных хлоридов и бромидов, но только один йодид и не дифторид. Вместо кажущейся степени окисления +2 эти соединения содержат индий в степенях окисления +1 и +3. Таким образом, дииодид описывается как InInX 4. Некоторое время спустя было подтверждено существование соединений, содержащих анион In 2. Br., который содержит индий-индийскую связь. Ранние работы по хлоридам и бромидам включали исследования бинарных фазовых диаграмм тригалогенидов и родственного моногалогенида. Многие из соединений изначально были неправильно идентифицированы, поскольку многие из них неконгруэнтны и разлагаются перед плавлением. Существование большинства хлоридов и бромидов, о которых ранее сообщалось, в настоящее время либо подтверждено рентгеновскими дифракционными исследованиями, либо их структура утеряна. Возможно, самым неожиданным случаем ошибочной идентификации стал неожиданный результат: тщательное повторное исследование бинарной фазовой диаграммы InCl / InCl 3 не обнаружило InCl 2... Причина такого обилия соединений в том, что индий образует 4 и 6 координированных анионов, содержащих индий (III), например В. Br., In. Cl., а также анион In 2. Br., который неожиданно содержит индий-индиевую связь.
In7Cl9- твердое вещество желтого цвета, стабильное до 250 ° C, которое входит в состав In 6 (InCl 6) Cl 3
In7Br9имеет структуру, аналогичную In <285.>и может быть сформулирован как In 6 (InBr 6) Br 3
In5Br7представляет собой бледно-желтое твердое вещество. Сформулирован в 3 (В 2Br6) Br. Анион In 2Br6имеет затмеваемую этаноподобную структуру с длиной связи металл-металл 270 мкм.
In2Cl3бесцветен и входит в состав In 3 InCl 6 В отличие от этого, In 2Br3содержит анион In 2Br6, как присутствует в In 5Br7, и состоит из In (In 2Br6) со структурой, подобной Ga 2Br3.
In4Br7, почти бесцветен с бледно-зеленовато-желтым оттенок. Он светочувствителен (как TlCl и TlBr), распадаясь на InBr 2 и металл In. Это смешанная соль, содержащая анионы In. Br. и In. Br., уравновешенные катионами In. Он сформулирован в 5 (InBr 4)2(InBr 6). Причины искаженной решетки приписывались разрыхляющей комбинации между дважды заполненными ненаправленными 5s орбиталями индия и соседние 4p гибридные орбитали брома.
In5Cl9сформулирован как In 3In2Cl9. Анион In 2. Cl. имеет два 6-координированных атома индия с 3-мя мостиковыми атомами хлора, биоктаэдры, разделяющие грани, со структурой, аналогичной Cr 2. Cl. и Tl 2. Cl..
InBr 2 представляет собой зеленовато-белое кристаллическое твердое вещество, в состав которого входит InIn Br 4. Он имеет ту же структуру, что и GaCl 2. InBr 2 растворим в ароматических растворителях, и были идентифицированы некоторые соединения, содержащие комплексы η-арена In (I) (см. тактильность для объяснения связывания в таком ионе арена с металлом. комплексы). С некоторыми лигандами InBr 2 образует нейтральные комплексы, содержащие индий-индийскую связь.
InI 2 представляет собой твердое вещество желтого цвета, которое образует InInI 4.
Твердые моногалогениды InCl, InBr и InI все нестабильны по отношению к воде, разлагаясь на частицы металла и индия (III). Они находятся между соединениями галлия (I), которые являются более реактивными, и таллием (I), которые устойчивы по отношению к воде. InI самый стабильный. До относительно недавнего времени моногалогениды были научным курьезом, однако с открытием того, что их можно использовать для получения кластерных и цепочечных соединений индия, они теперь вызывают гораздо больший интерес.
InF известен только как нестабильное газообразное соединение.
InCl при комнатной температуре имеет желтый цвет с кубической искаженной структурой NaCl. Красная высокая температура (>390 ° C) имеет структуру 
InBr представляет собой красное кристаллическое твердое вещество, т.пл. 285 ° C. Он имеет ту же структуру, что и 
InI представляет собой темно-красное пурпурное кристаллическое твердое вещество. Он имеет ту же структуру, что и 
Тригалогениды представляют собой кислоты Льюиса и образуют присоединение соединений с лигандами. Для InF 3 известно несколько примеров, однако известны другие аддитивные соединения галогенидов с тетраэдрической, тригонально-бипирамидальной и октаэдрической координационной геометриями. С галогенид-ионами есть примеры всех этих геометрических форм наряду с некоторыми анионами с октаэдрически координированным индием и мостиковыми атомами галогена, In 2. X. с тремя мостиковыми атомами галогена и In 2. X. только с одним. Кроме того, существуют примеры индия с квадратной плоской геометрией в ионе InX 5. Квадратная плоская геометрия In. Cl. была первой найденной для элемента основной группы.
Известны соли In. Cl., In. Br. и In. I.. Соль LiInF 4 была приготовлена, однако она не содержит тетраэдрических анионов, но имеет необычную слоистую структуру с октаэдрически координированными атомами индия. Соли InF 6, In. Cl. и In. Br. были изготовлены.
Ион In. Cl. оказался квадратно-пирамидальным в соли (NEt4) 2 InCl 5 с той же структурой, что и (NEt 4)2TlCl 5, но является тригонально-бипирамидным в сольвате тетрафенилфосфонийпентахлориндата ацетонитрила.
Ион In. Br. аналогичным образом обнаружен квадратно-пирамидным, хотя и искаженным, в бис (4- хлорпиридиния) соли и тригонального бипирамида в Bi 37 InBr 48.
Ионы In 2. X. содержат один мостиковый атом галогена. Изогнутый или линейный мостик не может быть определен по спектрам. Хлорид и бромид были обнаружены с помощью масс-спектрометрии с электрораспылением. Ион In 2. I. был получен в соли CsIn 2I7.
Цезиевые соли In 2. Cl. и In 2. Br. обе содержат биядерные анионы с октаэдрически координированными атомами индия.
InX 2 образуются, когда ион In 2X6диспропорционирует. Соли содержащие ионы In. X., и их колебательные спектры интерпретируются как показывающие, что они имеют симметрию C 3v, тригонально-пирамидальную геометрию со структурами, подобными изоэлектронным ионам Sn. X..
Были приготовлены соли хлорид-, бромид- и йодид-ионов (Bu 4N)2In2X6. В неводных растворителях этот ион диспропорционирует с образованием In. X. и In. X..
После открытия In 2Br6ряд родственных нейтральных соединений, содержащих ядро In 2X4, был образован в результате реакции дигалогенидов индия с нейтральные лиганды. Некоторые химики называют эти аддукты, когда они используются в качестве отправной точки для синтеза кластерных соединений, как In 2X4, например, аддукт TMEDA.