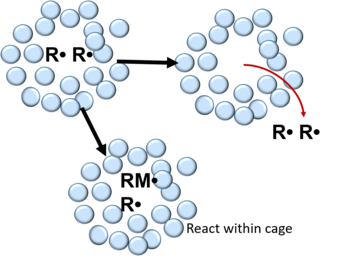
 Свободные радикалы в растворителе могут потенциально вступать в реакцию с мономером внутри клетки растворителя или диффундировать наружу
Свободные радикалы в растворителе могут потенциально вступать в реакцию с мономером внутри клетки растворителя или диффундировать наружу эффект клетки в химии описывает, как на свойства молекулы влияет ее окружение. Впервые введенный Франком и Рабиновичем в 1934 году, эффект клетки предполагает, что вместо того, чтобы действовать как отдельная частица, молекулы в растворителе более точно описываются как инкапсулированная частица. Чтобы взаимодействовать с другими молекулами, заключенная в клетку частица должна диффундировать из клетки растворителя. Типичный срок службы клетки для растворителя составляет 10 с.
В свободнорадикальной полимеризации радикалы, образующиеся при разложении молекулы инициатора, окружены клеткой, состоящей из молекул растворителя и / или мономера. Внутри клетки свободные радикалы подвергаются множеству столкновений, приводящих к их рекомбинации или взаимной дезактивации. Это можно описать следующей реакцией:
После рекомбинации свободные радикалы могут реагировать с молекулами мономера внутри стенок клетки или распространяются из клетки. В полимерах вероятность того, что пара свободных радикалов избежит рекомбинации в клетке, составляет 0,1 - 0,01, а в жидкостях - 0,3-0,8.
Эффект клетки можно количественно описать как эффективность рекомбинации клетки Fcгде:
Здесь F c определяется как отношение константы скорости рекомбинации клетки (k c) к сумме констант скорости для всех процессов клетки. Согласно математическим моделям, F c зависит от изменений нескольких параметров, включая размер радикала, форму и вязкость растворителя. Сообщается, что эффект клетки будет усиливаться с увеличением размера радикала и уменьшением массы радикала.
При свободнорадикальной полимеризации скорость инициирования зависит от того, насколько эффективен инициатор. Низкая эффективность инициатора во многом объясняется эффектом клетки. Скорость инициирования описывается как:
, где R i - скорость инициирования, k d - константа скорости диссоциации инициатора, [I] - начальная концентрация инициатора. Эффективность инициатора представляет собой долю первичных радикалов R ·, которые действительно способствуют инициированию цепи. Из-за эффекта клетки свободные радикалы могут подвергаться взаимной дезактивации, в результате чего образуются стабильные продукты вместо того, чтобы инициировать распространение, что снижает значение ƒ.