Твердый кислород образуется при нормальном атмосферном давлении при температуре ниже 54,36 К (-218,79 ° C, -361,82 ° F). Твердый кислород O2, как и жидкий кислород, представляет собой прозрачное вещество светлого небесно-голубого цвета, вызванного поглощением в красной части спектра видимого света.
Молекулы кислорода привлекли внимание из-за взаимосвязи между и кристаллическими структурами, электронными структурами и сверхпроводимостью. Кислород - единственная простая двухатомная молекула (и одна из немногих молекул в целом), несущая магнитный момент. Это делает твердый кислород особенно интересным. в состоянии покоя, поскольку он считается «управляемым спином» кристаллом, который отображает антиферромагнитный магнитный порядок в низкотемпературных фазах. Магнитные свойства кислорода широко изучены. При очень высоких давлениях твердый кислород переходит из состояния изолирующего в состояние металлического ; и при очень низких температурах он даже переходит в сверхпроводящее состояние . Структурные исследования твердого кислорода начались в 1920-х годах, и в настоящее время однозначно установлено шесть различных.
Плотность твердого кислорода составляет от 21 см / моль в α-фазе до 23,5 см / моль в γ-фазе.
 Фазовая диаграмма для твердого кислорода
Фазовая диаграмма для твердого кислорода Известно, что существует шесть различных фаз твердого кислорода :
Было известно, что кислород затвердевает в состоянии, называемом β-фазой, при комнатной температуре. растирание путем приложения давления и при дальнейшем увеличении давления β-фаза претерпевает фазовые переходы в δ-фазу при 9 ГПа и ε-фазу при 10 ГПа; и из-за увеличения молекулярных взаимодействий цвет β-фазы меняется на розовый, оранжевый, затем красный (стабильная фаза октаокислорода), и красный цвет далее темнеет до черного с повышением давления. Было обнаружено, что металлическая ζ-фаза появляется при 96 ГПа при дальнейшем сжатии кислорода ε-фазы.
Когда давление кислорода при комнатной температуре увеличивается на 10 ГПа ( 1,450,377 фунт / кв. Дюйм), он претерпевает резкий фазовый переход в другой аллотроп. Его объем значительно уменьшается, и он меняет цвет от небесно-голубого до темно-красного. Эта ε-фаза была открыта в 1979 году, но ее структура не ясна. Основываясь на его инфракрасном спектре поглощения, исследователи в 1999 году предположили, что эта фаза состоит из молекул O. 4в кристаллической решетке. Однако в 2006 г. методом рентгеновской кристаллографии было показано, что эта стабильная фаза, известная как ε кислород или красный кислород, находится в факт O. 8. Никто не предсказал структуру теоретически: ромбовидный кластер O. 8, состоящий из четырех молекул O. 2.
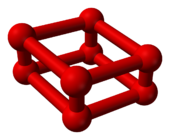 |  |
В этой фазе он имеет темно-красный цвет, очень сильный поглощение инфракрасного излучения, и a. Он также стабилен в очень большой области давления и был предметом многочисленных исследований дифракции рентгеновских лучей, спектроскопии и теории. Было показано, что он имеет моноклинную симметрию C2 / m, и его свойства поглощения инфракрасного излучения приписывались ассоциации молекул кислорода в более крупные единицы.
A ζ -фаза появляется при 96 ГПа, когда кислород в ε-фазе подвергается дальнейшему сжатию. Эта фаза была открыта в 1990 году путем повышения давления кислорода до 132 ГПа. Ζ-фаза с металлическим кластером проявляет сверхпроводимость при давлениях более 100 ГПа и температуре ниже 0,6 К.