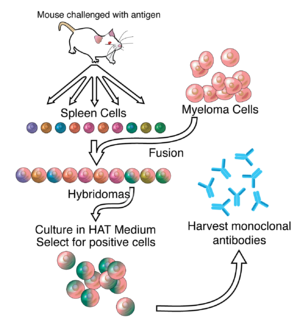
 Схематическое изображение того, как моноклональные антитела обычно образуются из гибридом. Для создания ZMapp гены, кодирующие антитела, были извлечены из гибридом, генетически сконструированы для замены компонентов мыши человеческими компонентами и трансфицированы в растения табака.
Схематическое изображение того, как моноклональные антитела обычно образуются из гибридом. Для создания ZMapp гены, кодирующие антитела, были извлечены из гибридом, генетически сконструированы для замены компонентов мыши человеческими компонентами и трансфицированы в растения табака. ZMapp представляет собой экспериментальный биофармацевтический лекарственный препарат, содержащий три химерных моноклональных антитела, которые разрабатываются для лечения болезни, вызванной вирусом Эбола. Два из трех компонентов были первоначально разработаны в Национальной микробиологической лаборатории (NML) Канадского агентства общественного здравоохранения, а третий - в США. Армейский научно-исследовательский медицинский институт инфекционных болезней ; коктейль был оптимизирован Гэри Кобингером, ученым-исследователем из NML, и подвергся дальнейшей доработке по лицензии Mapp Biopharmaceutical. ZMapp был впервые использован на людях во время вспышки вируса Эбола в Западной Африке в 2014 г., он был ранее протестирован только на животных и еще не подвергался рандомизированному контролируемому исследованию. В январе 2015 года NIH провел клиническое испытание с участием субъектов из Сьерра-Леоне, Гвинеи и Либерии с целью охвата 200 человек, но эпидемия пошла на убыль, и испытание завершилось досрочно, в результате чего его статистические возможности оказались недостаточными, чтобы дать значимый результат о том, работает ли ZMapp..
В 2016 году клиническое исследование показало, что ZMapp был неэффективен против Эболы по сравнению с двумя другими видами лечения.
Препарат состоит из трех моноклональных антител (mAb), первоначально полученные от мышей, подвергшихся воздействию белков вируса Эбола, которые были химеризованы с человеческими константными областями. Компоненты представляют собой химерное моноклональное антитело c13C6 из ранее существовавшего коктейля антител под названием «MB-003» и два химерных mAb из другого коктейля антител под названием ZMab, c2G4 и c4G7. ZMapp производится на табачном заводе Nicotiana benthamiana в процессе биопродукции, известном как «фарминг », компанией Kentucky BioProcessing, дочерней компанией Reynolds American.
Как и внутривенная терапия иммуноглобулином, ZMapp содержит смесь нейтрализующих антител, которые придают пассивный иммунитет человеку, усиливая нормальный иммунный ответ и предназначен для введения после контакта с вирусом Эбола. Такие антитела использовались для лечения и профилактики различных инфекционных заболеваний и предназначены для атаки на вирус, воздействуя на его поверхность и нейтрализуя его, чтобы предотвратить дальнейшее повреждение.
 Nicotiana benthamiana табак
Nicotiana benthamiana табак Два из трех компонентов препарата были первоначально разработаны в Национальной микробиологической лаборатории (NML) Агентства общественного здравоохранения Канады, а третий - в Медицинском научно-исследовательском институте инфекционных болезней армии США; коктейль был оптимизирован Гэри Кобингером, тогдашним руководителем филиала NML, и находится в процессе дальнейшей разработки Leaf Biopharmaceutical (LeafBio, Inc.), филиала Mapp Biopharmaceutical из Сан-Диего. LeafBio создал ZMapp в сотрудничестве со своим материнским предприятием и Defyrus Inc., каждое из которых лицензировало собственный коктейль антител под названием MB-003 и ZMab.
MB-003 - это коктейль из трех гуманизированных или химерных mAb человека-мыши: c13C6, h13F6 и c6D8. Исследование, опубликованное в сентябре 2012 года, показало, что макаки-резус, инфицированные вирусом Эбола (EBOV), выживали при получении MB-003 (смесь 3 химерных моноклональных антител) через один час после заражения. При лечении через 24 или 48 часов после заражения четыре из шести животных выжили и практически не имели виремии и имели несколько клинических симптомов, если таковые были.
MB-003 был создан учеными из Медицинский научно-исследовательский институт инфекционных заболеваний армии США, Джин Олингер и Джейми Петтитт в сотрудничестве с Mapp Biopharmaceutical при многолетнем финансировании правительственных агентств США, включая Национальный институт аллергии и инфекционных заболеваний, передовых биомедицинских исследований и Управление по разработке и Агентство по снижению угроз.
ZMAb представляет собой смесь трех мышиных mAb: m1H3, m2G4 и m4G7. Исследование, опубликованное в ноябре 2013 года, показало, что инфицированные EBOV обезьяны макаки выжили после лечения комбинацией трех моноклональных антител, специфичных к поверхностному гликопротеину (EBOV-GP) (ZMAb).) в течение 24 часов после заражения. Авторы пришли к выводу, что постэкспозиционное лечение привело к устойчивому иммунному ответу с хорошей защитой на срок до 10 недель и некоторой защитой на сроке 13 недель. ZMab был создан NML и передан по лицензии Defyrus, компании biodefense из Торонто, при дальнейшем финансировании Агентством общественного здравоохранения Канады.
Статья 2014 г. описали, как Мэпп и его сотрудники, включая исследователей из Агентства общественного здравоохранения Канады, Kentucky BioProcessing и Национального института аллергии и инфекционных заболеваний, сначала химеризовали три антитела, содержащие ZMAb, затем протестировали комбинации MB-003 и химерных антител ZMAb на морских свинках, а затем на приматах, чтобы определить лучшую комбинацию, которой оказались c13C6 из MB-003 и два химерных mAb из ZMAb, c2G4 и c4G7. Это ZMapp.
В эксперименте, также опубликованном в статье 2014 года, 21 примат макака-резус был инфицирован Kikwit конголезским вариантом EBOV. Трем приматам в контрольной группе дали нефункциональные антитела, и 18 человек в экспериментальной группе были разделены на три группы по шесть человек. Все приматы в группе лечения получали три дозы ZMapp с интервалом в 3 дня. Первая группа лечения получила первую дозу на 3-й день после заражения; вторая группа - на 4-й день после заражения, а третья группа - на 5-й день после заражения. Все три приматы в контрольной группе погибли; все 18 приматов в группе лечения выжили. Затем Мапп показал, что ZMapp подавляет репликацию гвинейского штамма EBOV в клеточных культурах.
Mapp продолжает участвовать в производстве препарата через свои контракты с Kentucky BioProcessing, дочерней компанией Reynolds American. Для получения лекарственного средства гены, кодирующие химерные mAb, вставляли в вирусные векторы, и растения табака инфицировали вирусным вектором, кодирующим антитела, с использованием культур Agrobacterium. Впоследствии из растений извлекаются и очищаются антитела. Считается, что после получения генов, кодирующих химерные mAb, весь цикл производства табака займет несколько месяцев. Разработка этих методов производства финансировалась Агентством перспективных исследовательских проектов в области обороны США в рамках его усилий по биологической защите после террористических атак 11 сентября.
ZMapp был впервые использован во время вспышки вируса Эбола в Западной Африке в 2014 году, поскольку ранее он не проходил никаких клинических испытаний на людях для определения его эффективности или потенциальных рисков. К октябрю 2014 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США одобрило использование нескольких экспериментальных препаратов, включая ZMapp, для лечения пациентов, инфицированных вирусом Эбола. Использование таких препаратов во время эпидемии также было признано этичным Всемирной организацией здравоохранения. В 2014 году ограниченный запас ZMapp был использован для лечения 7 человек, инфицированных вирусом Эбола; из них 2 умерли. Результат не считается статистически значимым. В августе 2014 года Mapp объявил, что запасы ZMapp исчерпаны.
Отсутствие лекарств и недоступность экспериментального лечения в наиболее пострадавших регионах от вспышки вируса Эбола в Западной Африке стимулировали некоторых полемика. Тот факт, что наркотик впервые был дан американцам и европейцам, а не африканцам, согласно Los Angeles Times, «вызвал возмущение, подпитывая африканское восприятие западной бесчувственности и высокомерия с глубоким чувством недоверие и предательство все еще сохраняются в связи с эксплуатацией и злоупотреблениями в колониальную эпоху ". Салим С. Абдул Карим, директор исследовательского центра СПИДа в Южной Африке, поместил этот вопрос в контекст истории эксплуатации. и злоупотребления. Отвечая на вопрос о том, как люди могли бы отреагировать, если бы ZMapp и другие препараты впервые были применены к африканцам, он сказал: «Это был бы кричащий заголовок на первой полосе:« Африканцев использовали в качестве подопытных кроликов для медицины американской фармацевтической компании »».
В начале августа Всемирная организация здравоохранения призвала к созыву группы медицинских властей, «чтобы рассмотреть, следует ли более широко выпускать экспериментальные препараты». В заявлении Питер Пиот (соавтор вируса Эбола); Джереми Фаррар, директор Wellcome Trust ; и Дэвид Хейманн из Центра глобальной безопасности здравоохранения Chatham House призвали к выпуску экспериментальных лекарств для пострадавших африканских стран.
На пресс-конференции 6 августа 2014 г. Барак Обама, Президент Соединенных Штатов был задан вопрос о том, следует ли ускорить рассмотрение коктейля для утверждения или предоставить его больным пациентам за пределами Соединенных Штатов. Он ответил: «Я думаю, мы должны позволить науке направлять нас. Я не думаю, что вся информация связана с тем, полезен ли этот препарат».
88>Национальные институты здравоохранения 27 февраля 2015 года объявили о начале рандомизированного контролируемого исследования ZMapp, которое будет проведено в Либерии и США. С марта 2015 г. по ноябрь 2015 г. в испытании приняли участие 72 человека, инфицированных вирусом Эбола; исследователи прекратили набор новых субъектов в январе 2016 г., так как не смогли достичь цели набора в 200 человек из-за уменьшения вспышки Эболы. В результате, хотя для тех, кто получал ZMapp, был рассчитан на 40% более низкий риск смерти, разница не была статистически значимой, и в конечном итоге нельзя было определить, превосходит ли использование ZMapp только оптимизированный стандарт лечения. Однако оказалось, что ZMapp безопасен и хорошо переносится.
Коктейль ZMapp был оценено Всемирной организацией здравоохранения для использования в экстренных случаях в соответствии с этическим протоколом MEURI. Группа согласилась с тем, что «преимущества ZMapp перевешивают его риски», отметив при этом, что он создает логистические проблемы, в частности, необходимость холодовой цепи для распределения и хранения. Четыре альтернативных метода лечения (Ремдезивир, Регенерон продукт REGN-EB3 (REGN3470-3471-3479), Фавипиравир и мАт114 ) также рассматривались для использования, но они находятся на более ранних стадиях разработки. В августе 2019 года национальные органы здравоохранения Демократической Республики Конго, Всемирная организация здравоохранения и Национальные институты здравоохранения объявили о прекращении использования ZMapp вместе со всеми другими препаратами для лечения Эболы, кроме REGN-EB3 и mAb114, в текущих клинических условиях. исследований, в которых указывается на более высокий уровень смертности пациентов, не получавших REGN-EB3 и mAb114.
В октябре 2020 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) одобрило атолтивимаб / мафтивимаб. / одесивимаб (Inmazeb, ранее REGN-EB3) с показанием для лечения инфекции, вызванной эболавирусом Заира.