 | |
| Имена | |
|---|---|
| Имена ИЮПАК Триоксид урана Оксид урана (VI) | |
| Другие имена Оксид уранила Оксид урана | |
| Идентификаторы | |
| Количество CAS | |
| 3D модель ( JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.014.274 |
| Номер ЕС | |
| PubChem CID | |
| UNII | |
ИнЧИ
| |
Улыбки
| |
| Характеристики | |
| Химическая формула | UO 3 |
| Молярная масса | 286,29 г / моль |
| Появление | желто-оранжевый порошок |
| Плотность | 5,5–8,7 г / см 3 |
| Температура плавления | ~ 200–650 ° C (разлагается) |
| Растворимость в воде | Частично растворим |
| Состав | |
| Кристальная структура | см. текст |
| Космическая группа | I 4 1 / amd ( γ -UO 3) |
| Термохимия | |
| Стандартная мольная энтропия ( S | 99 Дж моль −1 K −1 |
| Std энтальпия формации (Δ F H ⦵298) | −1230 кДж моль −1 |
| Опасности | |
| Паспорт безопасности | Внешний паспорт безопасности материала |
| Пиктограммы GHS |    |
| Сигнальное слово GHS | Опасность |
| Формулировки опасности GHS | H300, H330, H373, H411 |
| NFPA 704 (огненный алмаз) |  4 0 1 OX 4 0 1 OX |
| точка возгорания | Не воспламеняется |
| Родственные соединения | |
| Связанные оксиды урана | Диоксид урана Триуран октоксид |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| | |
| Ссылки на инфобоксы | |
Уран триоксид (УО 3), называемый также уранила оксид, оксид урана (VI), и урановой оксид, является шестивалентного оксида из урана. Твердое вещество может быть получено путем нагревания уранилнитрата до 400 ° C. Его наиболее часто встречающийся полиморф, γ-UO 3, представляет собой желто-оранжевый порошок.
Есть три метода получения триоксида урана. Как указано ниже, два из них используются в промышленности при переработке ядерного топлива и обогащении урана.

Триоксид урана отправляется между перерабатывающими предприятиями в виде геля, чаще всего с шахт на перерабатывающие предприятия. При использовании для конверсии все оксиды урана часто называют переработанным ураном (RepU).
Cameco Corporation, которая работает на крупнейшем в мире заводе по переработке урана в Блинд-Ривер, Онтарио, производит триоксид урана высокой чистоты.
Сообщалось, что при коррозии урана в водном растворе, богатом кремнеземом, образуется диоксид урана, триоксид урана и коффинит. В чистой воде скепит (UO 2) 8 O 2 (OH) 12 12 (H 2 O) образуется в первую неделю, а затем, через четыре месяца, образовался студтит (UO 2) O 2 4 (H 2 O).. Это изменение оксида урана также приводит к образованию метастудтита, более стабильного пероксида уранила, часто обнаруживаемого на поверхности отработавшего ядерного топлива, подверженного воздействию воды. Отчеты о коррозии металлического урана были опубликованы Королевским обществом.
Как и все соединения шестивалентного урана, UO 3 опасен при вдыхании, проглатывании и при контакте с кожей. Это ядовитое, слаборадиоактивное вещество, которое при вдыхании может вызывать одышку, кашель, острые поражения артерий и изменения хромосом лейкоцитов и гонад, приводящие к врожденным порокам развития. Однако при попадании внутрь уран в основном токсичен для почек и может серьезно повлиять на их функцию.
Единственный хорошо охарактеризованный бинарный триоксид любого актинида - это UO 3, несколько полиморфов которого известны. Твердый UO 3 теряет O 2 при нагревании с образованием зеленого U 3 O 8 : данные о температуре разложения на воздухе варьируются от 200 до 650 ° C. Нагревание до 700 ° C в атмосфере H 2 дает темно-коричневый диоксид урана (UO 2), который используется в стержнях МОКС- ядерного топлива.
 | Форма α (альфа): слоистое твердое тело, в котором двухмерные слои связаны атомами кислорода (показаны красным). | Гидратированный пероксид уранила, образующийся при добавлении пероксида водорода к водному раствору нитрата уранила при нагревании до 200–225 ° C, образует аморфный триоксид урана, который при нагревании до 400–450 ° C образует триоксид альфа-урана. Было заявлено, что присутствие нитрата снижает температуру, при которой происходит экзотермический переход от аморфной формы к альфа-форме. |
 | β (бета) UO 3. Это твердое тело имеет структуру, которая опровергает большинство попыток его описания. | Эта форма может быть образована путем нагревания диураната аммония, в то время как PC Debets и BO Loopstra обнаружили четыре твердые фазы в системе UO 3 -H 2 O-NH 3, которые все можно рассматривать как UO 2 (OH) 2 H 2. O, где часть воды была заменена аммиаком. Независимо от точной стехиометрии или структуры, было обнаружено, что при прокаливании при 500 ° C на воздухе образуется бета-форма триоксида урана. |
 | Форма γ (гамма) с различными урановыми средами, выделенными зеленым и желтым цветом. | Наиболее часто встречающимся полиморфом является γ-UO 3, рентгеновская структура которого была определена на основе данных порошковой дифракции. Соединение кристаллизуется в пространственной группе I4 1 / amd с двумя атомами урана в асимметричной единице. Оба окружены несколько искаженными октаэдрами атомов кислорода. Один атом урана имеет два более близких и четыре более удаленных атома кислорода, тогда как другой имеет четыре близких и два более удаленных атома кислорода в качестве соседей. Таким образом, неправильно описывать структуру как [UO 2 ] 2+ [UO 4 ] 2- , то есть уранилуранат. |
 | Окружение атомов урана показано желтым в гамма-форме. |  | Цепочки колец U 2 O 2 в гамма-форме образуются слоями, чередующиеся слои, идущие под углом 90 градусов друг к другу. Эти цепи показаны как содержащая желтые атомы урана, в октаэдрическом окружении, которые искажены в стороне квадратных плоского путем удлинения осевого кислорода - уран связей. |
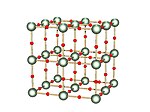 | Форма дельта (δ) представляет собой твердое тело кубической формы, в котором атомы кислорода расположены между атомами урана. |
Имеется твердая форма высокого давления с кольцами U 2 O 2 и U 3 O 3.

Водные и безводные формы UO 3

Безводные формы UO 3
Известно несколько гидратов триоксида урана, например UO 3 6H 2 O.
С помощью расчетов валентности связи можно оценить, насколько велик вклад данного атома кислорода в предполагаемую валентность урана. В расчетах валентности связи используются параметры, которые оцениваются после изучения большого количества кристаллических структур оксидов урана (и родственных соединений урана), обратите внимание, что степени окисления, которые обеспечивает этот метод, являются только руководством, которое помогает в понимании кристаллической структуры.
Используемая формула:
Сумма значений s равна степени окисления металлического центра.
Константы R O и B для связывания урана с кислородом приведены в таблице ниже. Для каждой степени окисления используйте параметры из приведенной ниже таблицы.
| Состояние окисления | R O | B |
|---|---|---|
| U (VI) | 2,08 Å | 0,35 |
| U (V) | 2,10 Å | 0,35 |
| U (IV) | 2,13 Å | 0,35 |
Эти расчеты можно производить на бумаге или в программном обеспечении.
Хотя триоксид урана встречается в виде твердого полимера в условиях окружающей среды, определенная работа была проделана в отношении молекулярной формы в газовой фазе, в исследованиях изоляции матриц и в расчетах.
При повышенных температурах газообразный UO 3 находится в равновесии с твердым U 3 O 8 и молекулярным кислородом.
С повышением температуры равновесие смещается вправо. Эта система была исследована при температурах от 900 ° C до 2500 ° C. Давление паров мономерного UO 3, находящегося в равновесии с воздухом и твердым U 3 O 8, при атмосферном давлении, около 10-5 мбар (1 мПа) при 980 ° C, повышается до 0,1 мбар (10 Па) при 1400 ° C, 0,34 мбар. (34 Па) при 2100 ° C, 1,9 мбар (193 Па) при 2300 ° C и 8,1 мбар (809 Па) при 2500 ° C.
Инфракрасная спектроскопия молекулярного UO 3, изолированного в матрице аргона, указывает на Т-образную структуру ( точечная группа C 2v) молекулы. Это контрастирует с обычно встречающейся симметрией молекулы D 3h, присущей большинству триоксидов. Из силовых констант авторы рассчитывают, что длина связи UO составляет от 1,76 до 1,79 Å (от 176 до 179 пм ).
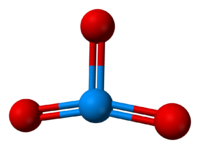 Расчетная геометрия молекулярного триоксида урана имеет симметрию C 2v.
Расчетная геометрия молекулярного триоксида урана имеет симметрию C 2v. Расчеты предсказывают, что точечной группой молекулярного UO 3 является C 2v с длиной аксиальной связи 1,75 Å, экваториальной длиной связи 1,83 Å и углом между аксиальными атомами кислорода 161 °. Более симметричная разновидность D 3h представляет собой седловую точку, на 49 кДж / моль выше минимума C 2v. В качестве объяснения авторы ссылаются на эффект Яна – Теллера второго порядка.
Кристаллическая структура фазы триоксида урана состава UO 2 82 была определена методами порошковой рентгеновской дифракции с использованием фокусирующей камеры типа Гинье. Элементарная ячейка кубическая с a = 4 138 ± 0 005 kX. Атом урана расположен в (000), а атомы кислорода в (Просмотр исходного кода MathML), (Просмотр исходного кода MathML) и (Просмотр исходного кода MathML) с некоторыми анионными вакансиями. Соединение изоструктурно ReO 3. Расстояние связи UO 2 073 Å согласуется с предсказанным Захариасеном для прочности связи S = 1.
Триоксид урана реагирует при 400 ° C с фреоном-12 с образованием хлора, фосгена, диоксида углерода и тетрафторида урана. Фреон-12 можно заменить фреоном-11, который образует четыреххлористый углерод вместо диоксида углерода. Это случай твердого пергалогенированного фреона, который обычно считается инертным, химически превращается при умеренной температуре.
Триоксид урана можно растворить в смеси трибутилфосфата и теноилтрифторацетона в сверхкритическом диоксиде углерода, во время растворения использовали ультразвук.
Исследовано обратимое внедрение катионов магния в решетку триоксида урана методом циклической вольтамперометрии с использованием графитового электрода, модифицированного микроскопическими частицами оксида урана. Этот эксперимент был также проведен для U 3 O 8. Это пример электрохимии твердого модифицированного электрода, эксперимент, который использовался для триоксида урана, связан с экспериментом с электродом с углеродной пастой. Также возможно восстановление триоксида урана металлическим натрием с образованием оксидов урана натрия.
Бывало, что литий можно вставить в решетку триоксида урана с помощью электрохимических средств, это похоже на то, как работают некоторые перезаряжаемые ионно-литиевые батареи. В этих перезаряжаемых элементах один из электродов представляет собой оксид металла, который содержит металл, такой как кобальт, который может быть восстановлен, чтобы поддерживать электронейтральность для каждого электрона, который добавляется к материалу электрода, когда ион лития входит в решетку этого оксидного электрода.
Оксид урана является амфотерным и реагирует как кислота и как основание, в зависимости от условий.
Растворение оксида урана в сильном основании, таком как гидроксид натрия, образует дважды отрицательно заряженный уранат- анион ( UO2- 4). Уранаты имеют тенденцию к соединению, образуя диуранат, U 2О2- 7, или другие полиуранаты. Важные diuranates включают диуранат аммония ((NH 4) 2 U 2 O 7), диуранат натрия (Na 2 U 2 O 7) и магний диуранат (MGU 2 O 7), который образует часть некоторых yellowcakes. Стоит отметить, что uranates вида M 2 UO 4 делать не содержат UO2- 4ионы, а скорее уплощенные октаэдры UO 6, содержащие уранильную группу и мостиковые атомы кислорода.
Растворение оксида урана в сильной кислоте, такой как серная или азотная кислота, образует двойной положительно заряженный катион уранила. Образовавшийся уранилнитрат (UO 2 (NO 3) 2 6H 2 O) растворим в простых и спиртовых, кетоновых и сложных эфирах ; например, трибутилфосфат. Эта растворимость используется для отделения урана от других элементов при ядерной переработке, которая начинается с растворения ядерных топливных стержней в азотной кислоте. Затем нитрат уранила превращается в триоксид урана при нагревании.
Из не азотной кислоты получается нитрат уранила, транс -UO 2 (NO 3) 2 2H 2 O, состоящий из восьми координированного урана с двумя бидентатных нитратогрупп лигандов и двух водных лигандов, а также знакомым O = U = O ядра.
Керамика на основе UO 3 становится зеленой или черной при обжиге в восстановительной атмосфере и от желтого до оранжевого цвета при обжиге в кислороде. Fiestaware оранжевого цвета - хорошо известный пример продукта с глазурью на основе урана. UO 3 также использовался в составах эмали, уранового стекла и фарфора.
До 1960 года UO 3 использовался в качестве агента кристаллизации в цветных кристаллических глазури. С помощью счетчика Гейгера можно определить, была ли глазурь или стекло изготовлено из UO 3.