Очередь является элементом вторичной структуры белков, где полипептидная цепь меняет свое направление в целом.
Согласно одному определению, виток - это структурный мотив, в котором атомы C α двух остатков, разделенных несколькими (обычно от 1 до 5) пептидными связями, близки (менее 7 Å [0,70 нм ]). Близость концевых атомов C α часто коррелирует с образованием межосновной водородной связи между соответствующими остатками. Такая водородная связь является основой первоначального, возможно, более известного определения поворота. Во многих случаях, но не все, водород-связь и C amp; alpha ; определение -Расстояния эквивалентны.
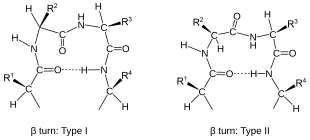 Схема бета-витков (тип I и тип II)
Схема бета-витков (тип I и тип II) Повороты классифицируются по разделению между двумя концевыми остатками:
| Тип | ф я + 1 | ψ я + 1 | ф я + 2 | ψ я + 2 |
|---|---|---|---|---|
| я | −60 ° | −30 ° | −90 ° | 0 ° |
| II | −60 ° | 120 ° | 80 ° | 0 ° |
| VIII | −60 ° | −30 ° | -120 ° | 120 ° |
| Я' | 60 ° | 30 ° | 90 ° | 0 ° |
| II ′ | 60 ° | -120 ° | −80 ° | 0 ° |
| VIa1 | −60 ° | 120 ° | −90 ° | 0 ° * |
| VIa2 | -120 ° | 120 ° | −60 ° | 0 ° * |
| VIb | −135 ° | 135 ° | −75 ° | 160 ° * |
| IV | повороты исключены из всех вышеперечисленных категорий | |||
Повороты классифицируются по двугранным углам их позвоночника (см. График Рамачандрана ). Поворот можно преобразовать в обратный поворот (в котором атомы основной цепи имеют противоположную хиральность ), изменив знак на его двугранных углах. (Обратный поворот не является истинным энантиомером, поскольку сохраняется хиральность атома C α.) Таким образом, γ-поворот имеет две формы, классическую форму с двугранными углами ( φ, ψ) примерно (75 °, -65 °) и обратная форма с двугранными углами (-75 °, 65 °). Встречается по крайней мере восемь форм бета-поворота, в зависимости от того, задействован ли цис- изомер пептидной связи и от двугранных углов двух центральных остатков. Классические и обратные β-повороты различаются простым числом, например, бета-повороты типа I и типа I '. Если водородная связь i → i + 3 берется в качестве критерия для поворотов, четырех категорий Венкатачалама (I, II, II ', I') достаточно, чтобы описать все возможные бета-повороты. Все четыре часто встречаются в белках, но чаще всего встречается I, за которым следуют II, I 'и II' в этом порядке.
Ω-петля является всеобъемлющим термином в течение более длительной, расширенной или нерегулярной петли без фиксированных внутренних водородных связей.
Во многих случаях один или несколько остатков участвуют в двух частично перекрывающихся витках. Например, в последовательности из 5 остатков оба остатка с 1 по 4 и остатки со 2 по 5 образуют очередь; в таком случае говорят о ( i, i + 1) двойном повороте. Множественные повороты (до семи раз) часто встречаются в белках. Ленты с бета-изгибом - это другой тип многооборотных лент.
Шпилька является частным случаем поворота, в котором направление белковых магистральных неудачами и фланговые вторичные элементы структуры взаимодействуют между собой. Например, бета-шпилька соединяет две антипараллельные β-нити с водородными связями (название довольно запутанное, поскольку β-шпилька может содержать много типов витков - α, β, γ и т. Д.).
Бета-шпильки для волос можно классифицировать по количеству остатков, составляющих виток, то есть не являющихся частью фланкирующих β-нитей. Если это число - X или Y (согласно двум различным определениям β листов), шпилька β определяется как X: Y.
Бета-витки на концах петель бета-шпилек имеют другое распределение типов по сравнению с другими; тип I 'является наиболее распространенным, за ним следуют типы II', I и II.
Иногда повороты обнаруживаются внутри гибких линкеров или петель, соединяющих белковые домены. Линкерные последовательности различаются по длине и обычно богаты полярными незаряженными аминокислотами. Гибкие линкеры позволяют соединительным доменам свободно скручиваться и вращаться, чтобы рекрутировать своих связывающих партнеров через динамику белкового домена. Они также позволяют своим партнерам по связыванию вызывать крупномасштабные конформационные изменения с помощью аллостерии на большие расстояния.
Были предложены две гипотезы о роли поворотов в сворачивании белков. С одной точки зрения, повороты играют решающую роль в складывании, объединяя и позволяя или разрешая взаимодействия между регулярными элементами вторичной структуры. Эта точка зрения подтверждается исследованиями мутагенеза, указывающими на критическую роль определенных остатков в поворотах некоторых белков. Кроме того, неродные изомеры пептидных связей X- Pro, в свою очередь, могут полностью блокировать конформационную укладку некоторых белков. С другой стороны, повороты играют пассивную роль при сбрасывании. Это мнение подтверждается плохой консервацией аминокислот, наблюдаемой в большинстве поворотов. Кроме того, ненативные изомеры многих пептидных связей X-Pro, в свою очередь, оказывают незначительное влияние или совсем не влияют на фолдинг.
За прошедшие годы было разработано множество методов прогнозирования бета-разворота. Недавно группа доктора Рагхавы разработала метод BetaTPred3, который предсказывает полный бета-поворот, а не отдельные остатки, падающие в бета-поворот. Этот метод также обеспечивает хорошую точность и является первым методом, который предсказывает все 9 типов бета-разворотов. Помимо прогнозирования, этот метод также можно использовать для определения минимального количества мутаций, необходимых для инициирования или разрушения бета-поворота в белке в желаемом месте.
Эти ссылки отсортированы по дате.