Гетерогенность опухоли описывает наблюдение, что разные опухолевые клетки могут демонстрировать различные морфологические и фенотипические профили, включая клеточную морфологию, экспрессию генов, метаболизм, подвижность, пролиферацию и метастатический потенциал. Это явление происходит как между опухолями (межопухолевая гетерогенность), так и внутри опухолей (внутриопухолевая гетерогенность). Минимальный уровень внутриопухолевой гетерогенности является простым следствием несовершенства репликации ДНК : всякий раз, когда клетка (нормальная или злокачественная) делится, приобретается несколько мутаций, что приводит к разнообразной популяции раковых клеток. Разнородность раковых клеток представляет значительные трудности в разработке эффективных стратегий лечения. Однако исследования в области понимания и характеристики неоднородности могут позволить лучше понять причины и прогрессирование заболевания. В свою очередь, это может привести к созданию более совершенных стратегий лечения, которые включают знания о неоднородности, чтобы обеспечить более высокую эффективность.
Гетерогенность опухолей наблюдалась при лейкозах, молочной железе, простате, толстой кишке, головном мозге, пищеводе, голове и шее, мочевом пузыре и гинекологических карциномах, липосаркомах и множественной миеломе.
Для объяснения неоднородности опухолевых клеток используются две модели. Это модель раковых стволовых клеток и модель клональной эволюции. Эти модели не исключают друг друга, и считается, что обе они вносят свой вклад в неоднородность в разной степени в разных типах опухолей.
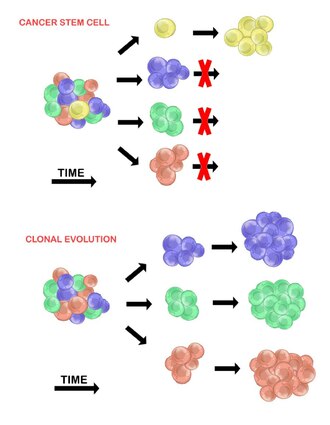 Способность раковых клеток образовывать опухоли в моделях гетерогенности раковых стволовых клеток и клональной эволюции.
Способность раковых клеток образовывать опухоли в моделях гетерогенности раковых стволовых клеток и клональной эволюции. Модель стволовых клеток рака утверждает, что в популяции опухолевых клеток, есть только небольшое подмножество клеток, которые tumourigenic (способны образовывать опухоли). Эти клетки называются раковыми стволовыми клетками ( РСК) и отличаются способностью как к самообновлению, так и к дифференцировке в неопухолевое потомство. Модель CSC утверждает, что наблюдаемая гетерогенность опухолевых клеток является результатом различий в стволовых клетках, из которых они произошли. Вариабельность стволовых клеток часто вызывается эпигенетическими изменениями, но также может быть результатом клональной эволюции популяции CSC, где полезные генетические мутации могут накапливаться в CSC и их потомстве (см. Ниже).
Доказательства модели раковых стволовых клеток были продемонстрированы на множестве типов опухолей, включая лейкемии, глиобластому, рак груди и рак простаты.
Однако существование CSC все еще обсуждается. Одна из причин этого заключается в том, что маркеры CSC трудно воспроизводить в нескольких опухолях. Кроме того, в методах определения опухолевого потенциала используются модели ксенотрансплантатов. Эти методы страдают от присущих им ограничений, таких как необходимость контролировать иммунный ответ у трансплантата животного, а также значительные различия в условиях окружающей среды от первичного участка опухоли до участка ксенотрансплантата ( например, отсутствие требуемых экзогенных молекул или кофакторов). Это вызвало некоторые сомнения в точности результатов CSC и выводов о том, какие клетки обладают опухолевым потенциалом.
Модель клональной эволюции была впервые предложена в 1976 году Питером Ноуэллом. В этой модели опухоли возникают из одной мутировавшей клетки, накапливая дополнительные мутации по мере развития. Эти изменения приводят к появлению дополнительных субпопуляций, и каждая из этих субпопуляций имеет способность делиться и мутировать дальше. Эта гетерогенность может привести к появлению субклонов, которые обладают эволюционным преимуществом перед другими в среде опухоли, и эти субклоны могут со временем стать доминирующими в опухоли. Когда эта модель была предложена, она позволила понять рост опухоли, неэффективность лечения и агрессию опухоли, которая происходит во время естественного процесса образования опухоли.
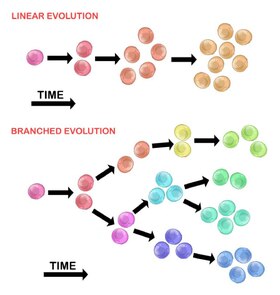 Разветвленная эволюция с большей вероятностью способствует гетерогенности опухоли.
Разветвленная эволюция с большей вероятностью способствует гетерогенности опухоли. Эволюция исходной опухолевой клетки может происходить двумя способами:
Последовательно упорядоченные мутации накапливаются в генах-драйверах, генах- супрессорах опухолей и ферментах репарации ДНК, что приводит к клональной экспансии опухолевых клеток. Линейное расширение с меньшей вероятностью отражает конечную точку злокачественной опухоли, поскольку накопление мутаций в гетерогенных опухолях является стохастическим.
Экспансия на несколько субклональных популяций происходит через механизм расщепления. Этот метод больше связан с неоднородностью опухоли, чем с линейным расширением. Приобретение мутаций является случайным в результате увеличения геномной нестабильности с каждым последующим поколением. Долговременное накопление мутаций может обеспечить селективное преимущество на определенных этапах прогрессирования опухоли. Микроокружение опухоли может также способствовать расширению опухоли, так как она способна изменять селективное давление, что опухолевые клетки подвергаются воздействию.
Между опухолевыми клетками наблюдались множественные типы гетерогенности, обусловленные как генетической, так и негенетической изменчивостью.
Генетическая гетерогенность является общей чертой опухолевых геномов и может происходить из нескольких источников. Некоторые виды рака возникают, когда экзогенные факторы вызывают мутации, такие как ультрафиолетовое излучение (рак кожи) и табак (рак легких). Более распространенным источником является геномная нестабильность, которая часто возникает, когда в клетках нарушаются ключевые регуляторные пути. Некоторые примеры включают нарушенные механизмы репарации ДНК, которые могут привести к увеличению ошибок репликации, и дефекты в механизме митоза, которые допускают крупномасштабное увеличение или потерю целых хромосом. Более того, некоторые виды лечения рака ( например, лечение темозоломидом и другими химиотерапевтическими препаратами) могут еще больше усилить генетическую изменчивость.
Мутационная гетерогенность опухоли относится к вариациям частоты мутаций в различных генах и образцах и может быть исследована с помощью MutSig. Этиология мутационных процессов может значительно различаться между образцами опухолей одного и того же или разных типов рака и может проявляться в различных контекстно-зависимых мутационных профилях. Его можно исследовать с помощью мутационных сигнатур COSMIC или MutaGene.
Опухолевые клетки также могут демонстрировать гетерогенность между профилями экспрессии. Это часто вызвано лежащими в основе эпигенетическими изменениями. Изменения в сигнатуре экспрессии были обнаружены в различных областях образцов опухоли у человека. Исследователи показали, что мутации, затрагивающие сходящиеся H3K36 метилтрансферазы SETD2 и гистона H3K4 деметилазы KDM5C возникла в пространственно разделенных опухолевых участков. Аналогичным образом, MTOR, ген, кодирующий регуляторную киназу клетки, оказался конститутивно активным, тем самым увеличивая фосфорилирование S6. Это активное фосфорилирование может служить биомаркером светлоклеточной карциномы.
Механохимическая неоднородность - отличительный признак живых эукариотических клеток. Он влияет на регуляцию эпигенетических генов. Гетерогенные динамические механохимические процессы регулируют взаимоотношения внутри группы клеточных поверхностей посредством адгезии. Развитие и распространение опухоли сопровождается изменением неоднородной хаотической динамики процесса механохимического взаимодействия в группе клеток, включая клетки внутри опухоли, и является иерархической для хозяина онкологических больных. Биологические явления механохимической неоднородности, может быть использованы для дифференциального рака желудка диагностики против пациентов с воспалением в слизистой оболочке желудка и повышение активности антиметастатической дендритных клеток на основе вакцин при механическом гетерогенизированные микрочастицы опухолевых клеток используются для их загрузки. Существует также возможный методический подход, основанный на одновременной диагностике и терапии ультразвуковой визуализацией, касающийся механохимического воздействия на конгломераты наночастиц с лекарствами в опухоли.
Гетерогенность между опухолевыми клетками может быть дополнительно увеличена из-за гетерогенности микроокружения опухоли. Региональные различия в опухоли ( например, доступность кислорода) оказывают различное избирательное давление на опухолевые клетки, что приводит к более широкому спектру доминирующих субклонов в различных пространственных областях опухоли. Влияние микросреды на клональное доминирование также является вероятной причиной гетерогенности между первичными и метастатическими опухолями, наблюдаемой у многих пациентов, а также межопухолевой гетерогенности, наблюдаемой у пациентов с одним и тем же типом опухоли.
Гетерогенные опухоли могут проявлять различную чувствительность к цитотоксическим препаратам среди разных клональных популяций. Это связано с клональными взаимодействиями, которые могут подавлять или изменять терапевтическую эффективность, что создает проблему для успешного лечения гетерогенных опухолей (и их гетерогенных метастазов).
Применение лекарств при гетерогенных опухолях редко убивает все опухолевые клетки. Первоначальная гетерогенная популяция опухолей может стать узким местом, так что выживут лишь немногие устойчивые к лекарствам клетки (если таковые имеются). Это позволяет популяциям устойчивых опухолей реплицироваться и выращивать новую опухоль с помощью механизма эволюции ветвления (см. Выше). Возникающая в результате репопуляция опухоль гетерогенная и устойчивая к начальному медикаментозному лечению. Повторно заселенная опухоль также может вернуться более агрессивным образом.
Введение цитотоксических лекарственных средств часто приводит к первоначальной усадке опухоли. Это представляет собой разрушение исходных неустойчивых субклональных популяций в гетерогенной опухоли, оставляя только устойчивые клоны. Эти устойчивые клоны теперь обладают селективным преимуществом и могут реплицироваться для повторного заселения опухоли. Репликация, вероятно, будет происходить в результате эволюции ветвления, что способствует гетерогенности опухоли. Повторно заселенная опухоль может оказаться более агрессивной. Это объясняется селективным преимуществом опухолевых клеток в отношении устойчивости к лекарственным средствам.
 Медикаментозное лечение вызывает эффект «узкого места», при котором устойчивые субклоны выживут и будут размножаться, чтобы повторно сформировать гетерогенную опухоль.
Медикаментозное лечение вызывает эффект «узкого места», при котором устойчивые субклоны выживут и будут размножаться, чтобы повторно сформировать гетерогенную опухоль. Из-за генетических различий внутри и между опухолями биомаркеры, которые могут предсказать ответ на лечение или прогноз, могут не иметь широкого применения. Однако было высказано предположение, что уровень гетерогенности сам по себе может использоваться в качестве биомаркера, поскольку более гетерогенные опухоли могут с большей вероятностью содержать устойчивые к лечению субклоны. Дальнейшие исследования по разработке биомаркеров, объясняющих неоднородность, все еще продолжаются.
В современных модельных системах обычно отсутствует гетерогенность, наблюдаемая при раке человека. Чтобы точно изучить неоднородность опухоли, мы должны разработать более точные доклинические модели. Одна из таких моделей, ксенотрансплантат опухоли, полученный от пациента, продемонстрировала отличную полезность в сохранении неоднородности опухоли, в то же время позволяя детально изучить движущие силы клональной приспособленности. Однако даже эта модель не может охватить всю сложность рака.
Хотя проблема выявления, характеристики и лечения неоднородности опухоли все еще активно исследуется, были предложены некоторые эффективные стратегии, включая как экспериментальные, так и вычислительные решения.