 | |
 | |
| Имена | |
|---|---|
| Название IUPAC Хлорид титана (IV) | |
| Другие названия Тетрахлорид титана. Тетрахлоротитан | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.028.584 |
| Номер ЕС |
|
| MeSH | Титан + тетрахлорид |
| PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Номер ООН | 1838 |
| Панель управления CompTox (EPA ) | |
InChI
| |
УЛЫБКИ
| |
| Свойства | |
| Химическая формула | TiCl. 4 |
| Молярная масса | 189,679 г / моль |
| Внешний вид | Бесцветная жидкость |
| Запах | пронизывающий кислотный запах |
| Плотность | 1,726 г / см |
| Температура плавления | -24,1 ° C (-11,4 ° F; 249,1 K) |
| Температура кипения | 136,4 ° C (277,5 ° F; 409,5 K) |
| Растворимость в воде | реагирует (экзотермический гидролиз) |
| Растворимость | растворим в дихлорметане, толуол, пентан |
| Давление пара | 1,3 кПа (20 ° C) |
| Магнитная восприимчивость (χ) | -54,0 · 10 см / моль |
| Показатель преломления (nD) | 1,61 (10,5 ° C) |
| Вязкость | 827 мкПа · с |
| Структура | |
| Координационная геометрия | Тетрагональная |
| Молекулярная форма | Тетраэдрическая |
| Дипольный момент | 0 D |
| Термохимия | |
| Стандартная молярная. энтропия (S 298) | 355 Дж · моль · K |
| Стандартная энтальпия образования. (ΔfH298) | −763 кДж · моль |
| Опасности | |
| Паспорт безопасности | MSDS |
| Пиктограммы GHS |    |
| Сигнальное слово GHS | Опасно |
| Краткая характеристика опасности GHS | H314, H317, H318, H330, H335, H370, H372 |
| Меры предосторожности GHS | P280, P301 + 330 + 331, P304 + 340, P305 + 351 + 338, P308 + 310 |
| NFPA 704 (огненный алмаз) |  0 3 2 0 3 2 |
| Родственные соединения | |
| Другие анионы | Бромид титана (IV). Фторид титана (IV). Иодид титана (IV) |
| Другое катионы | Хлорид гафния (IV). Хлорид циркония (IV) |
| Родственные соединения | Хлорид титана (II). Хлорид титана (III) |
| Если не указано иное, данные приведены для материалы в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
 Кристаллы замороженного тетрахлорида титана, плавящегося в жидкости
Кристаллы замороженного тетрахлорида титана, плавящегося в жидкости Тетрахлорид титана представляет собой неорганическое соединение с формулой TiCl 4. Он является важным промежуточным продуктом в производстве металлического титана и пигмента диоксида титана. TiCl 4 представляет собой летучую жидкость. При контакте с влажным воздухом он образует впечатляющие непрозрачные облака диоксида титана (TiO 2) и гидратированного хлористого водорода. Его иногда называют «щекотать» или «щекотать 4» из-за фонетического сходства его молекулярной формулы (TiCl 4) со словом.
TiCl 4 представляет собой плотную бесцветную перегоняемую жидкость, хотя неочищенные образцы могут быть желтыми или даже красно-коричневыми. Это один из редких галогенидов переходных металлов, который при комнатной температуре является жидкостью, другим примером является VCl 4. Это свойство отражает тот факт, что молекулы TiCl 4 слабо самоассоцируются. Большинство хлоридов металлов представляют собой полимеры, в которых атомы хлоридов являются мостами между металлами. Его точки плавления и кипения аналогичны таковым у CCl 4.
Ti имеет "закрытую" электронную оболочку с тем же количеством электронов, что и инертный газ аргон. Тетраэдрическая структура TiCl 4 согласуется с его описанием как d-металлический центр (Ti), окруженный четырьмя идентичными лигандами. Эта конфигурация приводит к высоко симметричным структурам, следовательно, к тетраэдрической форме молекулы. TiCl 4 имеет структуру, аналогичную TiBr 4 и TiI 4 ; три соединения имеют много общего. TiCl 4 и TiBr 4 реагируют с образованием смешанных галогенидов TiCl 4-x Brx, где x = 0, 1, 2, 3, 4. Также измерения магнитного резонанса указывают на то, что галогенидный обмен между TiCl 4 и VCl 4.
TiCl 4 растворим в толуоле и хлороуглеродах. Некоторые арены образуют комплексы типа [(C 6R6) TiCl 3 ]. TiCl 4 реагирует экзотермически с донорными растворителями, такими как THF, с образованием гексакоординированных аддуктов. Более объемные лиганды (L) дают пентакоординированные аддукты TiCl 4 L.
TiCl 4 производится с помощью хлоридного процесса, который включает восстановление руд оксида титана, обычно ильменит (FeTiO 3) с углеродом в потоке хлора при 900 ° C. Примеси удаляются отгонкой.
Совместное производство FeCl 3 нежелательно, что побудило к развитию альтернативных технологий. Вместо прямого использования ильменита используется «рутиловый шлак». Этот материал, нечистая форма TiO 2, получают из ильменита путем удаления железа с использованием восстановления углерода или экстракции серной кислотой. Неочищенный TiCl 4 содержит множество других летучих галогенидов, включая ванадилхлорид (VOCl 3), тетрахлорид кремния (SiCl 4) и тетрахлорид олова (SnCl 4), которые необходимо разделить.
Мировые поставки металлического титана, около 250 000 тонн в год, производятся из TiCl 4. Превращение включает восстановление тетрахлорида металлическим магнием. Эта процедура известна как процесс Кролла :
В процессе Хантера, жидкий натрий является восстановителем вместо магния.
Около 90% производимого TiCl 4 используется для изготовления пигмента диоксида титана (TiO 2). Преобразование включает гидролиз TiCl 4, процесс, в результате которого образуется хлористый водород :
В некоторых случаях TiCl 4 окисляется непосредственно кислородом :
Он использовался для производства дымовых завес, так как он дает тяжелый белый дым, который не имеет тенденции к образованию дыма.
Тетрахлорид титана - универсальный реагент, который образует различные производные, включая те, что показаны ниже.
Наиболее примечательной реакцией TiCl 4 является его легкий гидролиз, о чем свидетельствует высвобождение хлористого водорода и образование оксидов титана и оксихлоридов, как описано выше для получения TiO 2. Тетрахлорид титана использовался для создания морских дымовых завес. Хлороводород немедленно поглощает воду с образованием аэрозоля соляной кислоты, который эффективно рассеивает свет. Кроме того, диоксид титана с высокой рефракцией также является эффективным светорассеивателем. Однако этот дым вызывает коррозию.
Спирты реагируют с TiCl 4 с образованием соответствующих алкоксидов с формулой [Ti (OR) 4]n(R = алкил, n = 1, 2, 4). Как указано в их формуле, эти алкоксиды могут принимать сложные структуры, варьирующиеся от мономеров до тетрамеров. Такие соединения полезны в материаловедении, а также в органическом синтезе. Хорошо известным производным является изопропоксид титана, который является мономером.
Органические амины реагируют с TiCl 4 с образованием комплексов, содержащих амидо (R 2 N-содержащий) и имидо (RN-содержащий) комплексы. С аммиаком образуется нитрид титана. Иллюстративной реакцией является синтез тетракис (диметиламидо) титана Ti (NMe 2)4, желтой растворимой в бензоле жидкости: эта молекула является тетраэдрической с плоскими азотными центрами.
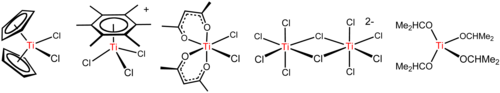
TiCl 4 представляет собой кислоту Льюиса, о чем свидетельствует его склонность к гидролизу. С простым эфиром THF TiCl 4 реагирует с образованием желтых кристаллов TiCl 4 (THF) 2. С хлоридными солями TiCl 4 вступает в реакцию с последовательным образованием [Ti 2Cl9], [Ti 2Cl10] (см. Рисунок выше) и [TiCl 6 ]. Реакция хлорид-ионов с TiCl 4 зависит от противоиона. NBu 4 Cl и TiCl 4 дает пятикоординированный комплекс NBu 4 TiCl 5, тогда как меньший NEt. 4дает (NEt 4)2Ti2Cl10. Эти реакции подчеркивают влияние электростатики на структуру соединений с высокой ионной связью.
Восстановление TiCl 4 с алюминием приводит к одноэлектронному восстановлению. Трихлорид (TiCl 3 ) и тетрахлорид обладают противоположными свойствами: трихлорид представляет собой твердое вещество, являющееся координационным полимером, и является парамагнитным. Когда восстановление проводят в растворе THF, продукт Ti (III) превращается в голубой аддукт TiCl 3 (THF) 3.
Металлоорганическая химия титана обычно начинается с TiCl 4. Важная реакция включает циклопентадиенил натрия с образованием дихлорида титаноцена, TiCl 2(C5H5)2. Это соединение и многие его производные являются предшественниками катализаторов Циглера-Натта. Реагент Теббе, применяемый в органической химии, представляет собой алюминийсодержащее производное титаноцена, которое образуется в результате реакции дихлорида титаноцена с триметилалюмием. Он используется для реакций «олефинирования».
Арены, такие как C 6 (CH 3)6, реагируют с образованием комплексов фортепиано-стул [Ti (C 6R6) Cl 3 ] (R = H, CH 3 ; см. Рисунок выше). Эта реакция иллюстрирует высокую кислотность Льюиса соединения TiCl. 3, которая образуется при отщеплении хлорида из TiCl 4 на AlCl 3.
TiCl 4 время от времени находит применение в органическом синтезе, используя от его кислотности Льюиса, его оксофильности и свойств переноса электрона его восстановленных галогенидов титана. Он используется в катализируемом кислотой Льюиса присоединении альдола Ключом к этому применению является тенденция TiCl 4 активировать альдегиды (RCHO) путем образования аддуктов, таких как (RCHO) TiCl 4 OC (H) R.
Опасности, создаваемые тетрахлоридом титана, обычно возникают в результате выделения хлористого водорода (HCl). TiCl 4 сильный Льюис кислота, экзотермически образующая аддукты даже с слабыми основаниями, такими как THF, и взрывоопасно с водой, выделяя HCl.