| Тиоредоксин-дисульфидредуктаза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 Кристаллическая структура тиоредоксинредуктазы 1 человека ; рендеринг на основе PDB : 2OHV . Кристаллическая структура тиоредоксинредуктазы 1 человека ; рендеринг на основе PDB : 2OHV . | |||||||||
| Идентификаторы | |||||||||
| Номер EC | 1.8.1.9 | ||||||||
| Номер CAS | 9074-14-0 | ||||||||
| Базы данных | |||||||||
| IntEnz | IntEnz view | ||||||||
| BRENDA | BRENDA entry | ||||||||
| ExPASy | NiceZyme view | ||||||||
| KEGG | KEGG entry | ||||||||
| MetaCyc | метаболический путь | ||||||||
| PRIAM | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| Онтология генов | AmiGO / QuickGO | ||||||||
| |||||||||
| Тиоредоксинредуктаза | |
|---|---|
| Идентификаторы | |
| Символ | ? |
| InterPro | IPR005982 |
| PROSITE | PS00573 |
| SCOPe | 1zof / SUPFAM |
Тиоредоксинредуктазы (TR, TrxR ) (EC 1.8.1.9 ) - единственные известные ферменты, восстанавливающие тиоредоксин (Trx). Были идентифицированы два класса тиоредоксинредуктазы: один класс у бактерий и некоторых эукариот и один у животных. Оба класса представляют собой флавопротеины, которые функционируют как гомодимеры. Каждый мономер содержит простетическую группу FAD, связывающий домен NADPH и активный сайт, содержащий редокс-активную дисульфидную связь.
Тиоредоксинредуктаза - единственный известный фермент, который катализирует восстановление тиоредоксина и, следовательно, является центральным компонент тиоредоксиновой системы. Вместе с тиоредоксином (Trx) и НАДФН наиболее общее описание этой системы - это метод образования восстановленных дисульфидных связей в клетках. Электроны отбираются от НАДФН через TrxR и переносятся в активный центр Trx, который продолжает восстанавливать дисульфиды белка или другие субстраты. Система Trx существует во всех живых клетках и имеет эволюционную историю, связанную с ДНК как генетическим материалом, защитой от окислительного повреждения из-за метаболизма кислорода и редокс-сигнализацией с использованием таких молекул, как перекись водорода и оксид азота.
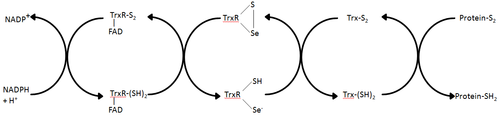 Схематическая диаграмма клетки TrxR роль По материалам Holmgren et al.
Схематическая диаграмма клетки TrxR роль По материалам Holmgren et al. Два класса тиоредоксинредуктазы развились независимо:
Эти два класса TrxR имеют только ~ 20% идентичности последовательностей в участке первичной последовательности, где они могут быть надежно выровнены. Итоговая реакция обоих классов TrxR идентична, но механизм действия каждого различен.
Люди экспрессируют три изофермента тиоредоксинредуктазы: тиоредоксинредуктазу 1 (TrxR1, цитозольный), тиоредоксинредуктазу 2 (TrxR2, митохондриальная), тиоредоксинредуктаза 3 (TrxR3, специфична для семенников). Каждый изозим кодируется отдельным геном:
|
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
В E.coli ThxR есть два связывающих домена: один для FAD, а другой - для NADPH. Связь между этими двумя доменами представляет собой двухцепочечный антипараллельный β-лист. Каждый домен в отдельности очень похож на аналогичные домены в глутатионредуктазе и липоамиддегидрогеназе, но их относительная ориентация этих доменов в ThxR повернута на 66 градусов. Это становится важным в механизме действия фермента, который описан ниже. ThxR гомо-димеризуется с границей раздела между двумя мономерами, образованной тремя альфа-спиралями и двумя петлями. Каждый мономер может отдельно связывать молекулу тиоредоксина.

Структура тиоредоксина, связанного димером ThxR E. coli

Структура ThxR E.coli с простетическими группами FAD и NADPH, помеченными
Структура TrxR млекопитающих сходна с E. coli. Он содержит связывающий домен FAD и NADPH и интерфейс между двумя мономерными субъединицами. В ThxR млекопитающих имеется вставка в связывающем домене FAD между двумя альфа-спиралями, которая образует небольшую пару бета-цепей. Активный дисульфид в ферменте расположен на одной из этих спиралей, и, таким образом, активная дисульфидная связь расположена в домене FAD, а не в домене NADPH, как в E. coli и других прокариоты.
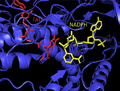
Структура простетических групп ThxR FAD и NADPH человека
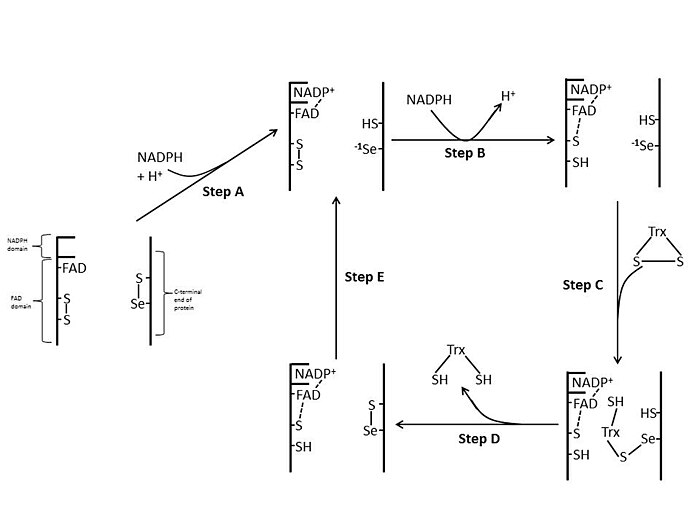 Предлагаемый механизм у млекопитающих и, предположительно, людей: Исходя из полностью окисленной формы, реакция начинается с восстановления селененилсульфида до селенолят-анион (Se (-1)) с электронами, полученными от НАДФН через FAD (этап A). Из-за низкого значения pKa селенола селенолят-анион является преобладающей формой в физиологических условиях. Второй перенос электрона от второй молекулы NADPH восстанавливает тихиоловые связи активного центра с одним остатком Cys, стабилизированным взаимодействием с FAD (стадия B). Затем селенолят-анион атакует дисульфидные связи Trx и образующийся фермент-Trx смешанный селененилсульфид (стадия C), который затем подвергается атаке соседнего остатка Cys для регенерации селененилсульфида (стадия D). Затем этот селененилсульфид восстанавливается тиолатом активного центра другой субъединицы (стадия E). По материалам Zhong et al. Это согласуется с выводами о том, что комплексы (2,2 ‘: 6‘, 2 ’‘ - терпиридин) платины (II) ингибируют TrxR человека.
Предлагаемый механизм у млекопитающих и, предположительно, людей: Исходя из полностью окисленной формы, реакция начинается с восстановления селененилсульфида до селенолят-анион (Se (-1)) с электронами, полученными от НАДФН через FAD (этап A). Из-за низкого значения pKa селенола селенолят-анион является преобладающей формой в физиологических условиях. Второй перенос электрона от второй молекулы NADPH восстанавливает тихиоловые связи активного центра с одним остатком Cys, стабилизированным взаимодействием с FAD (стадия B). Затем селенолят-анион атакует дисульфидные связи Trx и образующийся фермент-Trx смешанный селененилсульфид (стадия C), который затем подвергается атаке соседнего остатка Cys для регенерации селененилсульфида (стадия D). Затем этот селененилсульфид восстанавливается тиолатом активного центра другой субъединицы (стадия E). По материалам Zhong et al. Это согласуется с выводами о том, что комплексы (2,2 ‘: 6‘, 2 ’‘ - терпиридин) платины (II) ингибируют TrxR человека. В E. coli ThxR пространственная ориентация доменов FAD и NADPH такова, что окислительно-восстановительные кольца FAD и NADPH не находятся в непосредственной близости друг от друга. Когда домен FAD E. coli поворачивается на 66 градусов, при этом домен NADPH остается фиксированным, две простетические группы переходят в тесный контакт, позволяя электронам переходить от NADPH к FAD, а затем к дисульфидной связи активного центра. Консервативные остатки активного сайта в E. coli представляют собой -Cys-Ala-Thr-Cys-.
TrxR млекопитающих имеют гораздо более высокую гомологию последовательности с глутатионредуктазой, чем E. coli. Остатки Cys активного центра в домене FAD и связанном домене NADPH находятся в непосредственной близости, что исключает необходимость поворота на 66 градусов для переноса электронов, обнаруженного в E. coli. Дополнительной особенностью механизма у млекопитающих является наличие остатка селеноцистеина на С-конце белка, который необходим для каталитической активности. Консервативные остатки в активном центре млекопитающих представляют собой -Cys-Val-Asn-Val-Gly-Cys-.
Поскольку активность этого фермента необходим для роста и выживания клеток, он является хорошей мишенью для противоопухолевой терапии. Кроме того, активность фермента повышается при нескольких типах рака, включая злокачественную мезотелиому. Например, мотексафин гадолиний (MGd) - это новый химиотерапевтический агент, который избирательно воздействует на опухолевые клетки, что приводит к их гибели и апоптозу посредством ингибирования тиоредоксинредуктазы и рибонуклеотидредуктазы.
Дилатационная кардиомиопатия (DCM ) - частый диагноз в случаях застойной сердечной недостаточности. Тиоредоксинредуктазы являются важными белками для регулирования клеточного окислительно-восстановительного баланса и смягчения повреждений, вызываемых активными формами кислорода, генерируемыми в результате окислительного фосфорилирования в митохондриях. Инактивация митохондриального TrxR2 у мышей приводит к истончению стенок желудочков сердца и неонатальной смерти. Кроме того, две мутации в гене TrxR2 обнаруживаются у пациентов с диагнозом DCM, а не в контрольной популяции. Предполагается, что патологическим влиянием этих мутаций является нарушение способности контролировать окислительное повреждение сердечных миоцитов.
Недавно были проведены некоторые исследования, показывающие, что низкомолекулярная тиоредоксинредуктаза может быть мишень для новых антибиотиков (таких как ауранофин или эбселен). Это особенно верно в отношении Mycobacterium Haemophilum и может быть использовано для бактерий, устойчивых к антибиотикам.