 | |
 | |
| Имена | |
|---|---|
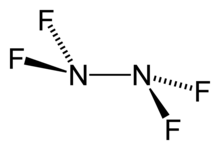
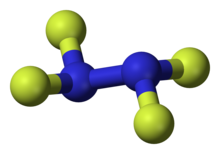
| Название ИЮПАК 1,1,2, 2-Тетрафторгидразин | |
| Другие наименования Тетрафторид диазота, перфторгидразин, ООН 1955 | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.030.091 |
| PubChem CID | |
| CompTox Dashboard (EPA ) | |
InChI
| |
SMILES
| |
| Свойства | |
| Химическая формула | N2F4 |
| Молярная масса | 104,01 г моль |
| Температура плавления | –164,5 ° C (–264,1 ° F; 108,6 K) |
| Температура кипения | -73 ° C (-99 ° F; 200 K) |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
Тетрафторгидразин или тетрафторид диазота, N 2F 4, является бесцветный реакционноспособный неорганический газ. Это фторированный аналог гидразина. Это очень опасное химическое вещество, которое взрывается в присутствии органических материалов.
Тетрафторгидразин получают из трифторида азота с использованием катализатора железа или фторида железа (II). Он используется в некоторых химических синтезах, в качестве предшественника или катализатора.
Тетрафторгидразин рассматривался для использования в качестве высокоэнергетического жидкого окислителя в некоторых никогда не используемых ракетное топливо формулы 1959 года.
Тетрафторгидразин находится в равновесии со своим радикальным мономером дифторидом азота.
При комнатной температуре N 2F4в основном связан только с 0,7% в форме NF 2 при давлении 5 мм рт. Когда температура повышается до 225 ° C, он в основном диссоциирует на 99% в форме NF 2.
. Энергия, необходимая для разрыва связи NN в N 2F4, составляет 20,8 ккал / моль, с изменением энтропии 38,6 ЕС. Для сравнения, энергия диссоциации связи N-N составляет 14,6 ккал / моль в N2O4, 10,2 ккал / моль в N2O2 и 60 ккал / моль в N2H4. Энтальпия образования N 2F4(ΔH f) составляет 34,421 кДж / моль.