| Пептидаза S8, связанная с субтилизином | |||||||||
|---|---|---|---|---|---|---|---|---|---|
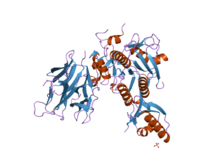 S8 + I9 (внизу справа), Bacillus subtilis ( PDB : 2pmw ) S8 + I9 (внизу справа), Bacillus subtilis ( PDB : 2pmw ) | |||||||||
| Идентификаторы | |||||||||
| Символ | Пептидаза_S8 | ||||||||
| Pfam | PF00082 | ||||||||
| ИнтерПро | IPR015500 | ||||||||
| PROSITE | PDOC00125 | ||||||||
| CATH | 1cse | ||||||||
| SCOP2 | 1cse / SCOPe / SUPFAM | ||||||||
| CDD | cd07477 | ||||||||
| |||||||||
| Субтилизин БПН | |||||||
|---|---|---|---|---|---|---|---|
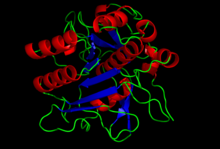 Кристаллическая структура домена S8 субтилизина. Кристаллическая структура домена S8 субтилизина. | |||||||
| Идентификаторы | |||||||
| Организм | Bacillus amyloliquefaciens | ||||||
| Символ | апр | ||||||
| Количество CAS | 9014-01-1 | ||||||
| Entrez | 5712479 | ||||||
| PDB | 1st2 Больше структур | ||||||
| UniProt | P00782 | ||||||
| Прочие данные | |||||||
| Номер ЕС | 3.4.21.62 | ||||||
| |||||||
| GO: 0004252 | |||||||
Субтилизин - это протеаза ( фермент, переваривающий белок ), первоначально полученный из Bacillus subtilis.
Субтилизины принадлежат к субтилазам, группе сериновых протеаз, которые, как и все сериновые протеазы, инициируют нуклеофильную атаку на пептидную (амидную) связь через остаток серина в активном центре. Субтилизины обычно имеют молекулярную массу 27 кДа. Их можно получить из определенных типов почвенных бактерий, например, Bacillus amyloliquefaciens, из которых они секретируются в больших количествах.
Субтилизин также коммерчески известный как алкалаз, ALK-фермент, bacillopeptidase, Bacillus зиЫШз щелочной протеиназа bioprase, bioprase AL, colistinase, genenase я, Esperase®, Максатаз, протеаза XXVII, thermoase, superase, субтилизин DY, subtilopeptidase, SP 266, Savinase ®, kazusase, протеазы VIII, protin 3 л, Savinase®, orientase 10B, протеазы С. это тип серин эндопептидазы из Merops семьи S8.
Структура субтилизина определена методом рентгеновской кристаллографии. Зрелая форма представляет собой глобулярный белок из 275 остатков с несколькими альфа-спиралями и большим бета-листом. N-конец содержит пропетидный домен I9 ( InterPro : IPR010259 ), который способствует сворачиванию субтилизина. Протеолитическое удаление домена активирует фермент. Он структурно не связан с химотрипсиновым кланом сериновых протеаз, но использует тот же тип каталитической триады в активном центре. Это делает его классическим примером конвергентной эволюции.
Активный центр имеет сеть реле заряда, включающую Asp-32, His-64 и активный центр Ser-221, организованные в каталитическую триаду. Сеть реле заряда функционирует следующим образом: карбоксилатная боковая цепь Asp-32 водородными связями с азотсвязанным протоном на имидазольном кольце His-64. Это возможно, потому что Asp отрицательно заряжен при физиологическом pH. Другой азот на His-64 водородных связях с протоном ОН Ser-221. Это последнее взаимодействие приводит к разделению заряда ОН, при этом атом кислорода становится более нуклеофильным. Это позволяет атому кислорода Ser-221 атаковать входящие субстраты (например, пептидные связи) с помощью соседней карбоксиамидной боковой цепи Asn-155.
Хотя Asp-32, His-64 и Ser-221 последовательно далеко друг от друга, они сходятся в трехмерной структуре, чтобы сформировать активный сайт.
Подводя итог описанным выше взаимодействиям, Ser-221 действует как нуклеофил и расщепляет пептидные связи своим частично отрицательным атомом кислорода. Это возможно из-за природы участка ретрансляции заряда субтилизина.
В молекулярной биологии, использующей B. subtilis в качестве модельного организма, ген, кодирующий субтилизин ( aprE ), часто является вторым после amyE геном выбора для интеграции репортерных конструкций из-за его необязательности.
Субтилизины, созданные на основе белков, широко используются в коммерческих продуктах (природный фермент легко инактивируется моющими средствами и высокими температурами) и также называется пятновыводителем, например, в средствах для стирки и мытья посуды, косметике, пищевой промышленности, мазях для ухода за кожей, контакте очистители линз, а также для исследований в области синтетической органической химии.
Люди могут подвергнуться воздействию субтилизина на рабочем месте при вдыхании, глотании, контакте с кожей и глазами. Национальный институт профессиональной безопасности и здоровья (NIOSH) установила предел рекомендованной экспозиции (REL) от 0,00006 мг / м 3 в течение 60-минутного периода.
Субтилизин может вызвать «ферментно-детергентную астму». Люди, чувствительные к субтилизину (алькалазе), обычно также имеют аллергию на бактерии Bacillus subtilis.