 | |
 | |
 | |
| Имена | |
|---|---|
| Другие имена D-Ox. Гидролин. Редуктон. Гидросульфит натрия. Сульфоксилат натрия. Сульфоксилат. Ватролит. Virtex L | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.028.991 |
| Номер EC |
|
| PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Номер ООН | 1384 |
| CompTox Панель управления (EPA ) | |
InChI
| |
УЛЫБКА
| |
| Pro perties | |
| Химическая формула | Na2S2O4 |
| Молярная масса | 174,107 г / моль (безводный). 210,146 г / моль (дигидрат) |
| Внешний вид | кристаллический порошок от белого до сероватого цвета. светлый - хлопья лимонного цвета |
| Запах | слабый запах серы |
| Плотность | 2,38 г / см (безводный). 1,58 г / см (дигидрат) |
| Точка плавления | 52 ° C ( 126 ° F; 325 K) |
| Температура кипения | Разлагается |
| Растворимость в воде | 18,2 г / 100 мл (безводный, 20 ° C). 21,9 г / 100 мл (дигидрат, 20 ° C) |
| Растворимость | мало растворим в спирте |
| Опасности | |
| Классификация ЕС (DSD) (устарело) | Вредно (Xn) |
| R-фразы (устарело) | R7, R22, R31 |
| S-фразы (устарело) | (S2), S7 / 8, S26, S28, S43 |
| NFPA 704 (огненный алмаз) |  3 2 1 3 2 1 |
| Температура вспышки | 100 ° C (212 ° F; 373 K) |
| Температура самовоспламенения. | 200 ° C (392 ° F; 473 K) |
| Родственные соединения | |
| Другие анионы | Сульфит натрия. Сульфат натрия |
| Родственные соединения | Тиосульфат натрия. Бисульфит натрия. Метабисульфит натрия. Натрий бисульфат |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на ink | |
Дитионит натрия (также известный как гидросульфит натрия ) представляет собой белый кристаллический порошок r со слабым сернистым запахом. Хотя он стабилен в отсутствие воздуха, он разлагается в горячей воде и в кислых растворах.
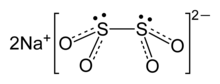
Рамановская спектроскопия и исследования дифракции рентгеновских лучей на монокристаллах показывают, что геометрия дитионит-аниона является гибкой. Дианион дитионита имеет симметрию C. 2 с почти затмеваемым углом кручения 16 ° O-S-S-O. В дигидратированной форме (Na. 2S. 2O. 4· 2H. 2O) дитионитовый анион имеет более короткую длину связи SS и крутильный угол гош 56 ° OSSO.
На слабую связь SS указывает расстояние SS, равное 239 пм. Поскольку эта связь является хрупкой, дитионитовый анион диссоциирует в растворе на анион-радикал [SO 2 ], что было подтверждено спектроскопией ЭПР. Также наблюдается, что S подвергается быстрому обмену между S 2O4и SO 2 в нейтральном или кислотном растворе, что соответствует слабой связи SS в анионе.
Дитионит натрия получают промышленным способом путем восстановления диоксида серы. Используют несколько методов, включая восстановление цинковым порошком, борогидридом натрия и формиатом. В 1990 году было произведено около 300 000 тонн.
Дитионит натрия стабилен в сухом состоянии, но водные растворы портятся из-за следующей реакции:
Такое поведение согласуется с нестабильностью дитионовой кислоты. Таким образом, растворы дитионита натрия нельзя хранить в течение длительного периода времени.
Безводный дитионит натрия разлагается на сульфат натрия и диоксид серы при температуре выше 90 ° C в воздух. В отсутствие воздуха он быстро разлагается при температуре выше 150 ° C до сульфита натрия, тиосульфата натрия, диоксида серы и следовых количеств серы.
Дитионит натрия является восстановителем. При pH = 7 потенциал составляет -0,66 В относительно NHE. Редокс происходит с образованием сульфита:
Дитионит натрия реагирует с кислородом:
Эти реакции демонстрируют сложное рН-зависимое равновесие с участием бисульфита, тиосульфата и диоксида серы.
В присутствии альдегидов дитионит натрия реагирует либо с образованием α-гидроксисульфинатов при комнатной температуре, либо с восстановлением альдегида до соответствующего спирта при температуре выше 85 ° С. С. Некоторые кетоны также восстанавливаются в аналогичных условиях.
Это соединение представляет собой водорастворимую соль и может использоваться в качестве восстановителя в водные растворы. Он используется как таковой в некоторых промышленных процессах окрашивания, в первую очередь тех, которые включают серные красители и кубовые красители, где нерастворимый в воде краситель может быть преобразован в водорастворимый соль щелочного металла (например, краситель индиго ). Восстановительные свойства дитионита натрия также устраняют избыток красителя, остаточного оксида и нежелательных пигментов, тем самым улучшая общее качество цвета.
Дитионит натрия также может использоваться для водоподготовки, газоочистки, очистки и отпарки. Его также можно использовать в промышленных процессах в качестве сульфирующего агента или источника ионов натрия. Помимо текстильной промышленности, этот состав используется в отраслях, связанных с кожей, продуктами питания, полимерами, фотографией и многими другими. Его широкое использование связано с его низкой токсичностью LD50 при 5 г / кг и, следовательно, с его широким спектром применения. Он также используется в качестве обесцвечивающего агента в органических реакциях.
Дитионит натрия часто используется в физиологических экспериментах как средство снижения окислительно-восстановительного потенциала растворов (E -0,66 V vs SHE при pH 7). Феррицианид калия обычно используется в качестве окисляющего химического вещества в таких экспериментах (E ~ 0,436 V при pH 7). Кроме того, дитионит натрия часто используется в опытах химии почвы для определения количества железа, которое не входит в состав первичных силикатных минералов. Следовательно, железо, экстрагированное дитионитом натрия, также называют «свободным железом». Сильное сродство дитионит-иона к двух- и трехвалентным катионам металлов (M, M) позволяет ему повышать растворимость железа, и, следовательно, дитионит является полезным хелатирующим агентом.
Натрий дитионит использовался в химическом увеличении нефтеотдачи для стабилизации полиакриламидных полимеров против радикального разложения в присутствии железа. Он также использовался в экологических приложениях для распространения фронта с низким E h в геологической среде с целью снижения таких компонентов, как хром.
Используется в проявителе тумана Kodak, FD-70. Это используется на втором этапе обработки черно-белых позитивных изображений для создания слайдов. Он является частью оборудования Kodak Direct Positive Film Developing Outfit.
В основном дитионит натрия в домашних условиях используется в качестве обесцвечивающего средства для белого белья, когда на него случайно попали пятна. окрашенного предмета, переходящего в цикл стирки при высокой температуре. Обычно он выпускается в 5-граммовых пакетиках, которые называются гидросульфитом после устаревшего названия соли.
Водные растворы дитионита натрия когда-то использовались для производства «раствора Физера для удаления кислорода из газового потока. Пиритион может быть получен двухстадийным синтезом из 2-бромпиридина путем окисления до N-оксида подходящей надкислотой с последующим замещением с использованием дитионита натрия для введения тиол функциональная группа.