A силоксан - это функциональная группа в кремнийорганической химии с связь Si-O-Si. Исходные силоксаны включают олигомерные и полимерные гидриды с формулами H (OSiH 2)nOH и (OSiH 2)n. Силоксаны также включают разветвленные соединения, Определяющей особенностью которого является то, что каждая пара кремниевых центров разделена одним атомом кислорода. Силоксановая функциональная группа образует основную цепь силиконов, главным примером которых является полидиметилсилоксан. функциональная группа R3SiO- (где три R могут быть разными) называется силокси . Силоксаны производятся искусственно и имеют множество коммерческих и промышленных применений из-за гидрофобности соединений, низкой теплопроводности, и высокая гибкость.

Силоксаны обычно принимают структуры, ожидаемые для связанных тетраэдров (" sp-like ") центры. Связь Si-O составляет 1,64 Å (по сравнению с расстоянием Si-C, равным 1,92 Å), а угол Si-O-Si довольно открыт при 142,5 °. Напротив, расстояние C-O в типичном диалкиловом эфире намного короче и составляет 1,414 (2) Å с более острым углом C-O-C, равным 111 °. Можно понять, что силоксаны будут иметь низкие барьеры для вращения вокруг связей Si-O как следствие низкого стерического затруднения. Это геометрическое соображение является основой полезных свойств некоторых силоксансодержащих материалов, таких как их низкие температуры стеклования.
 Диметилдихлорсилан (Si (CH 3)2Cl2) является ключевой предшественник циклических (D 3, D 4 и т. д.) и линейных силоксанов.
Диметилдихлорсилан (Si (CH 3)2Cl2) является ключевой предшественник циклических (D 3, D 4 и т. д.) и линейных силоксанов. Основным путем к силоксановой функциональной группе является гидролиз хлориды кремния:
Реакция протекает через начальное образование силанолов (R3Si-OH):
Затем может образоваться силоксановая связь по пути силанол + силанол или пути силанол + хлорсилан:
Гидролиз силилдихлорида может давать линейные или циклические продукты. Линейные продукты оканчиваются силанольными группами:
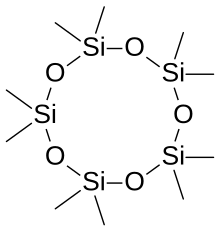
Циклические продукты не имеют силанольных концов:
Линейные продукты, полидиметилсилоксан (PDMS), имеют большую коммерческую ценность. Для их производства требуется производство дихлорида диметилкремния.
. Начиная с трисиланолов, возможны клетки, такие как частицы с формулой (RSi) nO3n / 2 с кубической (n = 8) и гексагональной призматические (n = 12) конструкции. Кубические клетки представляют собой кластеры кубанового типа, с центрами кремния в углах кубических центров кислорода, охватывающими каждый из двенадцати краев.
Окисление кремнийорганических соединений, включая силоксаны, дает диоксид кремния. Это превращение проиллюстрировано горением гексаметилциклотрисилоксана:
Сильное основание разлагает силоксановую группу, часто давая силоксид соли :
Эта реакция протекает с образованием силанолов. Подобные реакции используются в промышленности для превращения циклических силоксанов в линейные полимеры.
Полисилоксаны при сгорании в инертной атмосфере обычно подвергаются пиролизу с образованием оксикарбида кремния или карбида кремния (SiC). Используя эту реакцию, полисилоксаны используются в качестве прекерамических полимеров в различных процессах, включая аддитивное производство. Использование предшественника полисилоксана в керамике на основе полимера позволяет формировать керамические тела сложной формы, хотя необходимо учитывать значительную усадку при пиролизе.
Циклометико прочие, представляют собой группу метилсилоксанов, класс жидких силиконов (циклических полидиметилсилоксановых полимеров), которые обладают характеристиками низкой вязкости и высокой летучести, а также являются смягчающими веществами для кожи и в некоторых случаях полезны чистящие растворители. В отличие от диметиконов, которые представляют собой линейные силоксаны, которые не испаряются, циклометиконы являются циклическими: обе группы состоят из полимера, содержащего мономер основная цепь из одного кремния и двух атомов кислорода, связанных вместе, но вместо очень длинной «линейной» основной цепи, окруженной серией метил (которые производят прозрачную, нереактивную, нелетучую жидкость в диапазоне от низкой до высокой вязкости ), циклометиконы имеют короткие скелеты, которые образуют замкнутые или почти замкнутые кольца или «циклы» со своими метильными группами, что придает им многие из свойств диметиконов, но делает их гораздо более летучими. Они используются во многих косметических продуктах, где в конечном итоге желательно полное испарение силоксановой жидкости-носителя. Таким образом, они полезны для таких продуктов, как дезодоранты и антиперспиранты, которые должны покрывать кожу, но не оставаться липкими после этого. Большая часть циклометикона производится Dow Corning. Было показано, что циклометиконы вызывают появление силанолов во время биодеструкции у млекопитающих. Полученные силанолы способны ингибировать гидролитические ферменты, такие как термолизин, ацетилхолинэстераза, однако дозы, необходимые для ингибирования, на порядки выше, чем дозы, полученные в результате накопленного воздействия на потребительские товары. содержащие циклометиконы.
 Декаметилциклопентасилоксан, или D 5, циклический силоксан
Декаметилциклопентасилоксан, или D 5, циклический силоксан Слово «силоксан» образовано от слов sil icon, ox ygen и alkane. В некоторых случаях силоксановые материалы состоят из нескольких различных типов силоксановых групп; они помечены в соответствии с количеством связей Si-O:
| Циклические силоксаны (циклометиконы) | CAS | Линейные силоксаны | CAS |
|---|---|---|---|
| L2, MM: гексаметилдисилоксан | 107-46-0 | ||
| D3: гексаметилциклотрисилоксан | 541-05-9 | L3, MDM: октаметилтрисилоксан | 107-51-7 |
| D4: октаметилциклотетрасилоксан | 556-67-2 | L4, MD 2 M: декаметилтетрасилоксан | 141-62-8 |
| D5: декаметилциклопентасилоксан | 541-02-6 | L5, MD 3 M: додекаметилпентасилоксан | 141-63-9 |
| D6: додекаметилциклогексасилоксан | 540-97-6 | L6, MD 4 M: тетрадекаметилгексасилоксан | 107-52-8 |
Поскольку силиконы широко используются в биомедицинских и косметических целях, их токсикология интенсивно изучается. "Инертность силикона силиконы в отношении теплокровных животных были продемонстрированы в количество тестов ». При LD 50 у крыс>50 г / кг они практически нетоксичны. Однако остаются вопросы о хронической токсичности или последствиях биоаккумуляции, поскольку силоксаны могут быть долгоживущими.
Выводы о биоаккумуляции в значительной степени основаны на лабораторных исследованиях. Полевые исследования биоаккумуляции не достигли консенсуса. "Даже если концентрации силоксанов, которые мы обнаружили в рыбе, высоки по сравнению с концентрациями классических загрязнителей, таких как ПХБ, несколько других исследований в Осло-фьорде в Норвегии, озере Пепин в США и озеро Эри в Канаде показали, что концентрации силоксанов снижаются на более высоких уровнях пищевой цепи. Это открытие вызывает вопросы о том, какие факторы влияют на потенциал биоаккумуляции силоксанов ».
Циклометиконы распространены повсеместно, потому что они широко используются в биомедицинских и косметических целях. Их можно найти на высоких уровнях в американских городах. Они могут быть токсичными для водных животных в концентрациях, часто встречающихся в окружающей среде. Согласно одному отчету, циклометиконы D4 и D5 обладают биоаккумуляцией в некоторых водных организмах.
В Европейском Союзе D 4, D 5 и D 6 были признаны опасными в соответствии с правилами REACH. Они были охарактеризованы как вещества, вызывающие очень большую озабоченность (SVHC) из-за их PBT и свойств. Канада регулирует D 4 в соответствии с планом предотвращения загрязнения. В научном обзоре, проведенном в Канаде в 2011 году, сделан вывод, что «Силоксан D5 не представляет опасности для окружающей среды».