| Эпоксидирование по Шарплесу | |
|---|---|
| Названо в честь | Карла Барри Шарплесса |
| Тип реакции | Реакция образования кольца |
| Идентификаторы | |
| Organic Chemistry Portal | эпоксидирование Sharpless |
| RSC ID онтологии | RXNO: 0000141 |
Реакция эпоксидирования Sharpless является энантиоселективной химическая реакция для получения 2,3-эпоксиспиртов из первичных и вторичных аллильных спиртов.
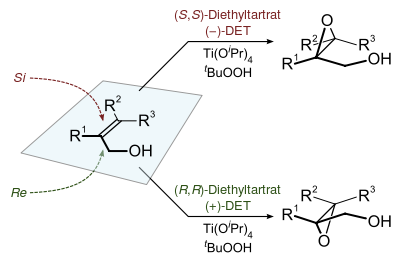
Стереохимия полученного эпоксида определяется энантиомером хирального диэфира тартрата (обычно диэтилтартрата или диизопропилтартрат ), используемые в реакции. Окислитель представляет собой трет-бутилгидропероксид. Энантиоселективность достигается с помощью катализатора, образованного из тетра (изопропоксида) титана и диэтилтартрата. Необходимо всего 5–10 мол.% Катализатора в присутствии 3Å молекулярных сит (3Å MS).
Успех эпоксидирования по Шарплесу можно отнести к пяти основным аспектам. Во-первых, эпоксиды можно легко превратить в диолы, аминоспирты и простые эфиры, поэтому образование хиральных эпоксидов важно в синтезе природных продуктов. Во-вторых, объем субстрата велик, включая множество первичных и вторичных аллиловых спиртов. В-третьих, продукты эпоксидирования Шарплесса часто имеют энантиомерные избытки более 90%. В-четвертых, предсказуемы продукты эпоксидирования Шарплесса. Наконец, реагенты для эпоксидирования Шарплесса коммерчески доступны и относительно недороги.
Было опубликовано несколько обзоров.
K. Барри Шарплесс разделил Нобелевскую премию по химии 2001 года за свою работу по асимметричному окислению. Приз был разделен с Уильямом С. Ноулзом и Рёдзи Нойори.
Структура катализатора не определена. Несмотря на это, все исследования пришли к выводу, что катализатор представляет собой димер [Ti (тартрат) (OR) 2 ]. Предполагаемый катализатор был определен с использованием рентгеноструктурных определений модельных комплексов, которые имеют необходимые структурные компоненты для катализа эпоксидирования Шарплесса.

Хиральность продукта эпоксидирования Шарплесса иногда прогнозируется с помощью после мнемоника. Прямоугольник обведен вокруг двойной связи в той же плоскости, что и атомы углерода двойной связи (плоскость xy), с аллиловым спиртом в правом нижнем углу и другими заместителями в соответствующих углах. В этой ориентации тартрат (-) сложного диэфира предпочтительно взаимодействует с верхней половиной молекулы, а тартрат (+) сложного диэфира предпочтительно взаимодействует с нижней половиной молекулы. Эта модель кажется верной, несмотря на замену олефина. Селективность уменьшается с увеличением R, но увеличивается с увеличением R и R (см. Введение).

Однако этот метод неверно предсказывает продукт аллильных 1,2-диолов.

Метод Шарплесса эпоксидирование также может дать кинетическое разрешение рацемической смеси вторичных 2,3-эпоксидных спиртов. Хотя выход процесса кинетического разделения не может превышать 50%, энантиомерный избыток в некоторых реакциях приближается к 100%.

Эпоксидирование по Шарплесу жизнеспособно при большом ассортимент первичных и вторичных алкеновых спиртов. Кроме того, за исключением, указанным выше, данный диалкилтартрат предпочтительно будет присоединяться к той же поверхности независимо от замещения в алкене. Чтобы продемонстрировать синтетическую полезность эпоксидирования Шарплесса, группа Шарплесса создала синтетические промежуточные продукты различных природных продуктов: метимицин, эритромицин, лейкотриен C-1 и (+) - диспарлюр. 170>В качестве одной из немногих высокоэнантиоселективных реакций в свое время было разработано множество манипуляций с 2,3-эпокси-спиртами.
Эпоксидирование по Шарплесу использовалось для полного синтеза различных сахаридов, терпены, лейкотриены, феромоны и антибиотики.
Основным недостатком этого протокола является необходимость наличия аллиловый спирт. Эпоксидирование Якобсена, альтернативный метод энантиоселективного окисления алкенов, преодолевает эту проблему и допускает более широкий набор функциональных групп.
Ранние исследования показали что аллиловые спирты придают лицевую селективность при использовании м-CPBA в качестве окислителя. Эта селективность менялась, когда аллиловый спирт был ацетилирован. Это открытие приводит к выводу, что водородная связь играет ключевую роль в селективности, и была предложена следующая модель.

Для циклических аллильных спиртов большая селективность наблюдается, когда спирт заблокирован в псевдоэкваториальное положение, а не псевдоосевое положение. Однако было обнаружено, что для систем с металлическими катализаторами, таких как системы на основе ванадия, скорость реакции увеличивалась, когда гидроксильная группа находилась в аксиальном положении, в 34 раза. Было показано, что субстраты, которые были заблокированы в псевдоэкваториальном положении, подвергались окислению. чтобы сформировать ene-one. В обоих случаях эпоксидирования, катализируемого ванадием, эпоксидированный продукт показал превосходную селективность в отношении синдиастереомера.

. В отсутствие водородных связей стерические эффекты прямое добавление пероксида на противоположную сторону. Однако перфтористые перкислоты все еще способны образовывать водородные связи с защищенными спиртами и обеспечивать нормальную селективность по водороду, присутствующему в перкислоте.

Хотя присутствие аллилового спирта действительно приводит к повышенной стереоселективности, скорости образования эти реакции протекают медленнее, чем в системах без спиртов. Однако скорость реакции субстратов с водородной связующей группой все же выше, чем у эквивалентных защищенных субстратов. Это наблюдение объясняется балансом двух факторов. Первый - это стабилизация переходного состояния в результате водородной связи. Во-вторых, это электроноакцепторная природа кислорода, которая отводит электронную плотность от алкена, снижая его реакционную способность.

Ациклические аллиловые спирты также обладают хорошей селективностью. В этих системах учитываются как A (стерические взаимодействия с винилом ), так и штамм A. Было показано, что двугранный угол , равный 120, лучше всего направляет подложки, которые связываются водородом с направляющей группой. Эта геометрия позволяет правильно расположить перекись, а также обеспечить минимальное пожертвование от C-C pi в сигма-звезду C-O. Это пожертвование снизит электронную плотность алкена и дезактивирует реакцию. Однако комплексы ванадия не образуют водородной связи со своими субстратами. Вместо этого они согласуются с алкоголем. Это означает, что двугранный угол 40 обеспечивает идеальное положение орбитали пероксидной сигма-звезды.

В системах с водородными связями деформация играет большую роль, поскольку требуемая геометрия вынуждает любые аллильные заместители иметь серьезные A-взаимодействия, но позволяет избежать А. Это приводит к син-добавлению полученного эпоксида. В случае ванадия требуемая геометрия приводит к сильным взаимодействиям A, но позволяет избежать A, что приводит к образованию эпоксида, направленного против направляющей группы. Было показано, что эпоксидирование, катализируемое ванадием, очень чувствительно к стерической массе винильной группы.

Гомоаллиловые спирты являются эффективными направляющими группами для эпоксидирования как в циклических, так и в ациклических системах для субстратов, которые демонстрируют водородные связи. Однако эти реакции, как правило, имеют более низкие уровни селективности.

В то время как субстраты, связывающие водородные связи, дают одинаковый тип селективности в аллильных и гомоаллильных случаях, для ванадиевых катализаторов верно противоположное.

Переходное состояние, предложенное Михеличом, показывает, что для этих реакций движущей силой селективности является минимизация деформации А в структуре псевдокресла.
Предлагаемое переходное состояние показывает, что субстрат будет пытаться принять конформацию, которая минимизирует аллическую деформацию. Для этого наименее объемная группа R будет вращаться, чтобы занять положение R4.
Хотя перкислоты и катализируемые металлами воздействия показывают разную селективность в ациклических системах, они показывают относительно одинаковую селективность в циклических системах. Для циклических кольцевых систем, которые меньше семи или меньше или 10 или больше, наблюдаются аналогичные модели избирательности. Однако было показано, что для средних колец (восемь и девять) надкислотные окислители показывают обратную селективность, в то время как реакции, катализируемые ванадием, продолжают показывать образование синэпоксида.

Хотя это наименее реактивный металлический катализатор для эпоксидирования, ванадий очень селективен к алкенам с аллиловыми спиртами. Ранняя работа Шарплесса показывает, что он предпочитает реакцию алкенов с аллильными спиртами над более замещенными электронно-плотными алкенами. В этом случае ванадий показал обратную региоселективность как по отношению к м-CPBA, так и по отношению к более реакционноспособным видам молибдена. Хотя ванадий обычно менее реакционноспособен, чем комплексы других металлов, в присутствии аллиловых спиртов скорость реакции выше, чем у молибдена, наиболее реактивного металла для эпоксидирования.
