В биохимии рибонуклеотид - это нуклеотид, содержащий рибозу в качестве пентозного компонента. Считается молекулярным предшественником нуклеиновых кислот. Нуклеотиды - это основные строительные блоки ДНК и РНК. Сам мономер из рибонуклеотидов образует основные строительные блоки РНК. Однако восстановление рибонуклеотида ферментом рибонуклеотидредуктазой (RNR) образует дезоксирибонуклеотид, который является важным строительным блоком для ДНК. Есть несколько различий между дезоксирибонуклеотидами ДНК и рибонуклеотидами РНК. Последовательные нуклеотиды связаны между собой фосфодиэфирными связями 3'-5 '.
Рибонуклеотиды также используются в других клеточных функциях. Эти специальные мономеры используются как в регуляции клеток, так и в передаче клеточных сигналов, как показано в аденозинмонофосфате ( АМФ ). Кроме того, рибонуклеотиды могут быть преобразованы в аденозинтрифосфат ( АТФ ), энергетическую валюту организмов. Рибонуклеотиды могут быть преобразованы в циклический аденозинмонофосфат ( циклический АМФ ) для регулирования гормонов в организмах. В живых организмах наиболее распространенными основаниями для рибонуклеотидов являются аденин (A), гуанин (G), цитозин (C) или урацил (U). Азотистые основания подразделяются на два исходных соединения: пурин и пиримидин.
 Общая структура рибонуклеотидов: фосфатная группа, рибоза, нуклеиновое основание.
Общая структура рибонуклеотидов: фосфатная группа, рибоза, нуклеиновое основание. 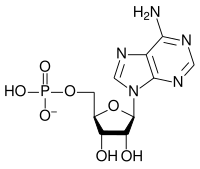 Структура аденозин-5'-монофосфата (АМФ)
Структура аденозин-5'-монофосфата (АМФ) 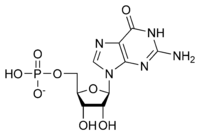 Структура гуанозин-5'-монофосфата (GMP)
Структура гуанозин-5'-монофосфата (GMP)  Структура уридин-5'-монофосфата (UMP)
Структура уридин-5'-монофосфата (UMP)  Структура цитидин-5'-монофосфата (CMP)
Структура цитидин-5'-монофосфата (CMP) Общая структура рибонуклеотида состоит из фосфатной группы, сахарной группы рибозы и азотистого основания, в котором нуклеотидным основанием может быть аденин, гуанин, цитозин или урацил. Без фосфатной группы состав азотистых оснований и сахара известен как нуклеозид. Взаимозаменяемые азотистые азотистые основания являются производными двух исходных соединений, пурина и пиримидина. Нуклеотиды представляют собой гетероциклические соединения, то есть они содержат по крайней мере два различных химических элемента в качестве членов своих колец.
И РНК, и ДНК содержат два основных пуриновых основания, аденин (A) и гуанин (G), а также два основных пиримидина. И в ДНК, и в РНК одним из пиримидинов является цитозин (C). Однако ДНК и РНК различаются вторым основным пиримидином. ДНК содержит тимин (T), а РНК содержит урацил (U). В некоторых редких случаях тимин действительно присутствует в РНК, а урацил - в ДНК.
Вот 4 основных рибонуклеотида (рибонуклеозид-5'-монофосфат), которые являются структурными единицами РНК.
| Нуклеотид | Символы | Нуклеозид |
|---|---|---|
| Аденилат (аденозин-5'-монофосфат) | A, AMP | Аденозин |
| Гуанилат (гуанозин-5'-монофосфат) | G, GMP | Гуанозин |
| Уридилат (уридин-5'-монофосфат) | U, UMP | Уридин |
| Цитидилат (цитидин 5'-монофосфат) | C, CMP | Цитидин |
В рибонуклеотидах сахарный компонент представляет собой рибозу, а в дезоксирибонуклеотидах сахарный компонент представляет собой дезоксирибозу. Вместо гидроксильной группы у второго атома углерода в кольце рибозы она заменена атомом водорода.
Оба типа пентоз в ДНК и РНК находятся в форме β-фуранозы (замкнутое пятичленное кольцо), и они определяют идентичность нуклеиновой кислоты. ДНК определяется содержанием нуклеиновой кислоты 2'-дезоксирибозы, в то время как РНК определяется содержанием нуклеиновой кислоты рибозы.
В некоторых случаях ДНК и РНК могут содержать некоторые второстепенные основания. Метилированные формы основных оснований наиболее распространены в ДНК. В вирусной ДНК некоторые основания могут быть гидроксиметилированы или глюкозилированы. В РНК чаще встречаются минорные или модифицированные основания. Некоторые примеры включают гипоксантин, дигидроурацил, метилированные формы урацила, цитозина и гуанина, а также модифицированный нуклеозид псевдоуридин. Также наблюдались нуклеотиды с фосфатными группами в положениях, отличных от 5'-углерода. Примеры включают рибонуклеозидные 2 ', 3'-циклические монофосфаты, которые являются выделяемыми промежуточными продуктами, и рибонуклеозид-3'-монофосфаты, которые являются конечными продуктами гидролиза РНК определенными рибонуклеазами. Другие варианты включают аденозин 3 ', 5'-циклический монофосфат (цАМФ) и гуанозин 3', 5'-циклический монофосфат (цГМФ).
Рибонуклеотиды связаны вместе с образованием цепей РНК через фосфодиэфирные связи. 5'-фосфатная группа одного нуклеотида связана с 3'-гидроксильной группой следующего нуклеотида, создавая основу из чередующихся фосфатных и пентозных остатков. На каждом конце полинуклеотида нет фосфодиэфирной связи. Фосфодиэфирные связи образуются между рибонуклеотидами ферментом РНК-полимеразой. Цепь РНК синтезируется от 5'-конца к 3'-концу, поскольку 3'-гидроксильная группа последнего рибонуклеотида в цепи действует как нуклеофил и запускает гидрофильную атаку на 5'-трифосфат входящего рибонуклеотида, высвобождая пирофосфат как побочный продукт. Благодаря физическим свойствам нуклеотидов основа РНК очень гидрофильна и полярна. При нейтральном pH нуклеиновые кислоты сильно заряжены, поскольку каждая фосфатная группа несет отрицательный заряд.
И ДНК, и РНК построены из нуклеозид-фосфатов, также известных как мононуклеотидные мономеры, которые термодинамически менее склонны к объединению, чем аминокислоты. При гидролизе фосфодиэфирные связи выделяют значительное количество свободной энергии. Следовательно, нуклеиновые кислоты имеют тенденцию к спонтанному гидролизу до мононуклеотидов. Предшественниками РНК являются GTP, CTP, UTP и ATP, который является основным источником энергии в реакциях группового переноса.
Ученые считают, что РНК возникла раньше ДНК.
Восстановление рибонуклеотидов до дезоксирибонуклеотидов катализируется рибонуклеотидредуктазой. Рибонуклеотидредуктаза (RNR) - важный фермент для всех живых организмов, поскольку он отвечает за последний этап синтеза четырех дезоксирибонуклеотидов (dNTP), необходимых для репликации и репарации ДНК. Для реакции также требуются два других белка: тиоредоксин и тиоредоксинредуктаза. Рибонуклеозиддифосфат (NDP) восстанавливается тиоредоксином до дезоксирибонуклеозиддифосфата (dNTP).
Общая реакция: рибонуклеозиддифосфат + NADPH + H + -gt; дезоксирибонуклеозиддифосфат + NADP + + H 2 O.
Чтобы проиллюстрировать это уравнение, dATP и dGTP синтезируются из ADP и GDP соответственно. Сначала они восстанавливаются с помощью RNR, а затем фосфорилируются нуклеозиддифосфаткиназами до dATP и dGTP. Рибонуклеотидредуктаза контролируется аллостерическими взаимодействиями. Как только dATP связывается с рибонуклеотидредуктазой, общая каталитическая активность фермента снижается, поскольку это означает обилие дезоксирибонуклеотидов. Это подавление обратной связи отменяется после связывания АТФ.
Во время синтеза ДНК ДНК-полимеразы должны селектировать против рибонуклеотидов, которые присутствуют на гораздо более высоких уровнях по сравнению с дезоксирибонуклеотидами. Крайне важно, чтобы была избирательность, поскольку репликация ДНК должна быть точной для поддержания генома организма. Было показано, что активные центры ДНК-полимераз Y-семейства ответственны за поддержание высокой селективности в отношении рибонуклеотидов. Большинство ДНК-полимераз также оснащены таким образом, чтобы исключать рибонуклеотиды из их активного сайта через объемный остаток боковой цепи, который может стерически блокировать 2'-гидроксильную группу рибозного кольца. Однако многие ядерные репликативные и репаративные ДНК-полимеразы включают рибонуклеотиды в ДНК, что позволяет предположить, что механизм исключения несовершенен.
Рибонуклеотиды могут синтезироваться в организмах из более мелких молекул посредством пути de novo или рециркулироваться посредством пути спасения. В случае пути de novo и пурины, и пиримидины синтезируются из компонентов, полученных из предшественников аминокислот, рибозо-5-фосфатов, CO2 и NH3.
 Синтез IMP. Цветовая гамма следующая: ферменты, коферменты, названия субстратов, ионы металлов, неорганические молекулы.
Синтез IMP. Цветовая гамма следующая: ферменты, коферменты, названия субстратов, ионы металлов, неорганические молекулы. 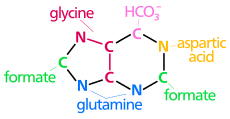 | В биосинтетическом происхождении пуринового кольца атомов N 1 возникает из амина группы Asp С 2 и С 8 происходят из формиата N 3 и N 9, предоставлено амидной группой Gln C 4, C 5 и N 7 получают из Gly C 6 происходит из HCO 3 - (CO 2) |
Биосинтез пуриновых нуклеотидов de novo довольно сложен и состоит из нескольких ферментативных реакций. Используя в качестве основы структуру сахара из пяти колец, пуриновое кольцо строится из нескольких атомов за один раз в одиннадцатиступенчатом процессе, который приводит к образованию инозината (IMP). По сути, IMP превращается в пуриновые нуклеотиды, необходимые для синтеза нуклеиновых кислот.
Путь начинается с превращения рибозо-5-фосфата (R5P) в фосфорибозилпирофосфат (PRPP) ферментом рибозо-фосфатдифосфокиназой (PRPS1). PRPP затем превращается в 5-фосфорибозиламин (5-PRA), поскольку глутамин отдает аминогруппу C-1 PRPP. В реакции конденсации фермент GAR-синтетаза вместе с глицином и АТФ активирует группу глицинкарбоксилазы 5-PRA с образованием глицинамидрибонуклеотида (GAR). Коэнзим N10-формил-THF вместе с ферментом GAR трансформилазой затем отдает одноуглеродную единицу аминогруппе на глицин GAR с последующим добавлением глутамина ферментом FGAR амидотрансферазой, что приводит к образованию рибонуклеотида формилглицинамидина (FGAM). Дегидратация FGAM ферментом FGAM циклазой приводит к замыканию имидазольного кольца, как 5-аминоимидазол-рибонуклеотид (AIR). Карбоксильная группа присоединяется к AIR с помощью N5-CAIR-синтетазы с образованием N5-карбоксаминоимидазол-рибонуклеотида (N5-CAIR), который затем превращается в карбоксамино-имидазол-рибонуклеотид (CAIR) с помощью фермента N5-CAIR-мутазы. Фермент SAICAR-синтетаза вместе с аминогруппой аспартата образует амидную связь с образованием N-сукцинил-5-аминоимидазал-4-карбоксамидрибонуклеотида (SAICAR). Продолжая этот путь, удаление углеродного скелета аспартата лиазой SAICAR приводит к 5-аминоимидазол-4-карбоксамид рибонуклеотиду (AICAR). Фермент AICAR трансформилаза способствует окончательному переносу углерода от N10-формилтетрагидрофолата, образуя N-формиламиноимидазол-4-карбоксамидрибонуклеотид (FAICAR). Наконец, закрытие второй кольцевой структуры осуществляется IMP-синтазой с образованием IMP, где судьба IMP должна приводить к образованию пуринового нуклеотида.
 Путь пиримидина де Ново
Путь пиримидина де Ново Синтез пиримидиновых нуклеотидов - гораздо более простой процесс. Образование пиримидинового кольца начинается с превращения аспартата в N-карбамоиласпартат в результате реакции конденсации с карбамоилфосфатом. Дигидрооротаза и дигидрооротаза дегидрогеназа затем превращают N-карбамоиласпартат в оротат. Оротат ковалентно связан с фосфорибозилпирофосфатом (PRPP) с помощью оротатфосфорибизол-трансферазы с образованием оротидинмонофосфата (OMP). OMP следует за декарбоксилированием оротидилатдекарбоксилазой с образованием рибонуклеотидной структуры уридилата (UMP). Затем UMP можно превратить в уридин-5'-трифосфат (UTP) посредством реакции двух киназ. Образование цитидин-5'-трифосфата (CTP) из UTP может быть достигнуто цитидилатсинтетазой с помощью промежуточного ацилфосфата.
Чтобы понять, как возникла жизнь, необходимы знания о химических путях, которые позволяют формировать ключевые строительные блоки жизни в вероятных пребиотических условиях. Согласно гипотезе мира РНК, в примитивном бульоне присутствовали свободно плавающие рибонуклеотиды. Это были основные молекулы, которые последовательно соединялись в РНК. Такие сложные молекулы, как РНК, должны были возникнуть из небольших молекул, реакционная способность которых определялась физико-химическими процессами. РНК состоит из пуриновых и пиримидиновых нуклеотидов, которые необходимы для надежной передачи информации и, следовательно, для дарвиновского естественного отбора и эволюции. Нам и др. продемонстрировали прямую конденсацию азотистых оснований с рибозой с образованием рибонуклеозидов в водных микрокаплях, что является ключевым этапом, ведущим к образованию РНК. Кроме того, правдоподобный пребиотический процесс для синтеза пиримидиновых и пуриновых рибонуклеотидов с использованием циклов «влажный-сухой» был представлен Becker et al.
 Фебус Левен
Фебус Левен До Джеймс Уотсон и Фрэнсис Крик в эпохальной статье, которая подробно структуру ДНК из Розалинд Франклин «s рентгеновской кристаллографии изображения, было несколько исторических ученых, которые также внесли вклад в его открытие. Фридрих Мишер, швейцарский врач, который в 1869 году первым выделил и идентифицировал нуклеиновое вещество из ядер белых кровяных телец, которое он позже назвал «нуклеином», проложив путь к открытию ДНК. Вслед за работой Мишера был немецкий биохимик Альбрехт Коссель, который в 1878 году выделил небелковые компоненты «нуклеина» и открыл пять нуклеиновых оснований, присутствующих в нуклеиновых кислотах: аденин, цитозин, гуанин, тимин и урацил. Хотя благодаря этим ранним открытиям были известны некоторые фундаментальные факты о нуклеиновых кислотах, их структура и функция оставались загадкой.
Только после открытия нуклеотидов в 1919 году Фебусом Левене, российско-литовским биохимиком, ворота открылись заново. Левен первым определил, что углеводный компонент, присутствующий в дрожжевой РНК, на самом деле был рибозой. Однако только после его открытия, что углеводный компонент в нуклеиновой кислоте тимуса также является сахаром, но не имеет одного атома кислорода, называемого дезоксирибозой, его открытие было широко оценено научным сообществом. В конце концов, Левен смог определить правильный порядок, в котором компоненты РНК и ДНК собраны вместе, - фосфатно-сахарная основа, которую он позже назвал нуклеотидом. Хотя Левен хорошо понимал порядок расположения нуклеотидных компонентов, структура расположения нуклеотидов в пространстве и ее генетический код все еще оставались загадкой в первые годы его карьеры.