| Протеиназа K | |||||||||
|---|---|---|---|---|---|---|---|---|---|
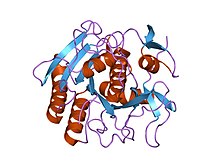 Структура протеиназы K. Структура протеиназы K. | |||||||||
| Идентификаторы | |||||||||
| Номер EC | 3.4.21.64 | ||||||||
| Базы данных | |||||||||
| IntEnz | IntEnz view | ||||||||
| BRENDA | BRENDA entry | ||||||||
| ExPASy | NiceZyme view | ||||||||
| KEGG | KEGG entry | ||||||||
| MetaCyc | метаболический путь | ||||||||
| PRIAM | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| |||||||||
| Протеиназа К | |||||||
|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||
| Организм | Engyodontium album | ||||||
| Символ | PROK | ||||||
| UniProt | P06873 | ||||||
| |||||||
В молекулярной биологии Протеиназа K (EC 3.4.21.64, протеаза K, эндопептидаза K, щелочная протеиназа Tritirachium, сериновая протеиназа Tritirachium album, протеиназа Tritirachium album K) представляет собой сериновую протеазу широкого спектра действия. Фермент был обнаружен в 1974 году в экстрактах из альбома fungus Engyodontium (бывший альбом). Протеиназа К способна переваривать волосы (кератин ), отсюда и название «Протеиназа К». Преобладающим сайтом расщепления является пептидная связь, прилегающая к карбоксильной группе алифатической и ароматической аминокислот с заблокированной альфа аминогруппы. Он обычно используется из-за его широкой специфичности. Этот фермент принадлежит к семейству пептидаз S8 (субтилизин ). Молекулярная масса протеиназы К составляет 28 900 дальтон (28,9 кДа).
Активированный кальцием, фермент переваривает белки предпочтительно после гидрофобных аминокислот (алифатических, ароматических и других гидрофобных аминокислот). Хотя ионы кальция не влияют на активность фермента, они вносят вклад в его стабильность. Белки будут полностью переварены, если время инкубации будет продолжительным и концентрация протеазы достаточно высока. После удаления ионов кальция стабильность фермента снижается, но протеолитическая активность сохраняется. Протеиназа К имеет два сайта связывания для Са, которые расположены близко к активному центру, но не участвуют напрямую в каталитическом механизме. Остаточной активности достаточно для переваривания белков, которые обычно загрязняют препараты нуклеиновых кислот. Следовательно, расщепление протеиназой К для очистки нуклеиновых кислот обычно проводят в присутствии ЭДТА (ингибирование ферментов, зависимых от ионов металлов, таких как нуклеазы).
Протеиназа К также стабильна в широком диапазоне pH (4–12) с оптимумом pH 8,0. Повышение температуры реакции с 37 ° C до 50–60 ° C может увеличить активность в несколько раз, например при добавлении 0,5–1% додецилсульфата натрия (SDS) или хлорида гуанидиния (3 M), тиоцианат гуанидиния (1 M) и мочевина (4 M). Вышеупомянутые условия усиливают активность протеиназы К, делая сайты расщепления субстрата более доступными. При температуре выше 65 ° C трихлоруксусная кислота (TCA) или ингибиторы сериновой протеазы AEBSF, PMSF или DFP подавляют активность. Протеиназа K не ингибируется гуанидин хлоридом, тиоцианатом гуанидиния, мочевиной, саркозилом, тритоном X-100, Твин 20, SDS, цитрат, йодуксусная кислота, ЭДТА или другими ингибиторами сериновой протеазы, такими как Nα-тозил-Lys хлорметилкетон (TLCK) и Nα-тозил-Phe хлорметилкетон (TPCK).
Активность протеазы K в обычно используемых буферах
| Буфер (pH = 8,0, 50 ° C, 1,25 мкг / мл протеазы K, 15 мин инкубации) | Активность протеиназы K (%) |
|---|---|
| 30 мМ Трис · Cl | 100 |
| 30 мМ Трис · Cl; 30 мМ ЭДТА; 5% Твин 20 ; 0,5% Тритон Х-100 ; 800 мМ GuHCl | 313 |
| 36 мМ Трис · Cl; 36 мМ ЭДТА; 5% Твин 20 ; 0,36% Тритон Х-100 ; 735 мМ GuHCl | 301 |
| 10 мМ Трис · Cl; 25 мМ ЭДТА; 100 мМ NaCl; 0,5% SDS | 128 |
| 10 мМ Трис · Cl; 100 мМ ЭДТА; 20 мМ NaCl; 1% саркозил | 74 |
| 10 мМ трис · Cl; 50 мМ KCl; 1,5 мМ MgCl 2 ; 0,45% Твин 20 ; 0,5% Тритон X-100 | 106 |
| 10 мМ трис · Cl; 100 мМ ЭДТА; 0,5% SDS | 120 |
| 30 мМ Трис · Cl; 10 мМ ЭДТА; 1% SDS | 203 |
Протеиназа K обычно используется в молекулярной биологии для расщепления белка и удаления загрязнений с препаратов нуклеиновой кислоты. Добавление протеиназы К к препаратам нуклеиновых кислот быстро инактивирует нуклеазы, которые в противном случае могли бы разрушить ДНК или РНК во время очистки. Он очень подходит для этого применения, поскольку фермент активен в присутствии химических веществ, которые денатурируют белки, такие как SDS и мочевина, хелатирует агенты, такие как реагенты EDTA, сульфгидрил, а также ингибиторы трипсина или химотрипсина. Протеиназа К используется для разрушения белков в лизатах клеток (ткани, клетки культур клеток) и для высвобождения нуклеиновых кислот, так как она очень эффективно инактивирует ДНКазы и РНКазы. Некоторые примеры применения: Протеиназа К очень полезна для выделения высоконативных, неповрежденных ДНК или РНК, поскольку большинство ДНКаз и РНКаз микробов или млекопитающих быстро инактивируются ферментом, особенно в присутствии 0,5–1% SDS. Очистка геномной ДНК от бактерий (минипреп): бактерии из насыщенной жидкой культуры лизируются и белки удаляются путем гидролиза 100 мкг / мл протеиназы К в течение 1 ч при 37 ° C;
Активность фермента в отношении нативных белков стимулируется денатурантами, такими как SDS. Напротив, при измерении с использованием субстратов пептида денатуранты ингибируют фермент. Причина этого результата в том, что денатурирующие агенты разворачивают белковые субстраты и делают их более доступными для протеазы.
Протеиназа K имеет две дисульфидные связи, но проявляет более высокую протеолитическую активность в присутствие восстанавливающих агентов (например, 5 мМ DTT ), что позволяет предположить, что предполагаемое восстановление его собственных дисульфидных связей не приводит к его необратимой инактивации. Протеиназа K ингибируется ингибиторами сериновой протеазы, такими как фенилметилсульфонилфторид (PMSF ), диизопропилфторфосфат (DFP ) или 4- (2-аминоэтил) бензолсульфонилфторид (AEBSF ). На активность протеиназы K не влияют реагенты, модифицирующие сульфгидрил: пара-хлормеркурибензойная кислота (PCMB ), N-альфа-тозил-L-лизил-хлорметилкетон () или N-альфа-тозил-1- фенилаланин-хлорметилкетон (TPCK ), хотя предположительно, если бы эти реагенты были включены вместе с реагентами, восстанавливающими дисульфид, которые обнажали обычно недоступные тиолы протеиназы K, он мог бы затем ингибироваться.
.