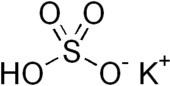 | |
 | |
 | |
| Наименования | |
|---|---|
| Название IUPAC Гидросульфат калия | |
| Другие названия Кислый сульфат калия | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.028.722 |
| Номер EC |
|
| Номер E | E515 (ii) (регуляторы кислотности,...) |
| PubChem CID | |
| номер RTECS |
|
| UNII | |
| Номер ООН | 2509 |
| Панель управления CompTox (EPA ) | |
InChI
| |
УЛЫБКИ
| |
| Правильно связи | |
| Химическая формула | KHSO 4 |
| Молярная масса | 136,169 г / моль |
| Внешний вид | бесцветное твердое вещество |
| Запах | без запаха |
| Плотность | 2,245 г / см |
| Температура плавления | 197 ° C (387 ° F; 470 K) |
| Температура кипения | 300 ° C (572 ° F; 573 K) (разлагается) |
| Растворимость в воде | 36,6 г / 100 мл (0 ° C). 49 г / 100 мл (20 ° C). 121,6 г / 100 мл (100 ° C) |
| Растворимость | растворим в ацетоне, этаноле. |
| Магнитная восприимчивость ( χ) | -49,8 · 10 см / моль |
| Термохимия | |
| Стандартная энтальпия. образования (ΔfH298) | -1163,3 кДж / моль |
| Опасности | |
| Паспорт безопасности | Внешний паспорт безопасности материала |
| Классификация ЕС (DSD) (устаревшая) | Коррозионная (C) |
| R-фразы (устаревшие) | R34, R36, R37, R38 |
| S-фразы (устаревшие) | (S1 / 2), S26, S36 / 37/39, S45 |
| Летальная доза или концентрация ( LD, LC): | |
| LD50(средняя доза ) | 2340 мг * кг |
| Родственные соединения | |
| Родственные соединения | Сульфат калия. Бисульфат натрия |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на ink | |
Бисульфат калия является неорганическим ic соединение с химической формулой KHSO 4 и представляет собой калиевую кислотную соль серной кислоты. Это белое водорастворимое твердое вещество.
В 1985 году было произведено более 1 миллиона тонн начальная стадия мангеймского процесса производства сульфата калия. Соответствующее преобразование - это экзотермическая реакция хлорида калия и серной кислоты:
Бисульфат калия является побочным продуктом при производстве азотной кислоты из нитрат калия и серная кислота:
Термическое разложение бисульфата калия образует пиросульфат калия :
При температуре выше 600 ° C пиросульфат калия превращается в сульфат калия и триоксид серы :
Бисульфат калия обычно используется для получения битартрата калия для виноделия. Бисульфат калия также используется в качестве дезинтегрирующего агента в аналитической химии или в качестве прекурсора для получения персульфата калия, мощного окислителя.
, минералогическая форма бисульфата калия, встречается очень редко. является еще одной более сложной формой бисульфата калия с формулой K 8H6(SO 4)7.
.