| |||
| Имена | |||
|---|---|---|---|
| Имена ИЮПАК Трифторид фосфора. Фторид фосфора (III). Трифторфосфан. Трифторидофосфор. Перфторфосфан | |||
| Другие названия Трифторфосфин. Фторид фосфора | |||
| Идентификаторы | |||
| Номер CAS | |||
| 3D-модель (JSmol ) | |||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard | 100.029.098 | ||
| PubChem CID | |||
| номер RTECS |
| ||
| UNII | |||
| CompTox Dashboard (EPA ) | |||
InChI
| |||
SMIL
| |||
| Свойства | |||
| Химическая формула | PF3 | ||
| Молярная масса | 87,968971 г / моль | ||
| Внешний вид | бесцветный газ | ||
| Плотность | 3,91 г / Л, газ | ||
| Точка плавления | −151,5 ° C (−240,7 ° F; 121,6 K) | ||
| Температура кипения | -101,8 ° C (-151,2 ° F; 171,3 K) | ||
| Растворимость в воде | медленный гидролиз | ||
| Структура | |||
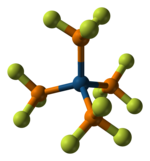
| Молекулярная форма | Тригонально-пирамидальная | ||
| Дипольный момент | 1,03 D | ||
| Опасности | |||
| Паспорт безопасности | См.: страница данных | ||
| NFPA 704 (огненный алмаз) |  0 3 1 0 3 1 | ||
| Температура вспышки | Невоспламеняющиеся | ||
| Родственные соединения | |||
| Другие анионы | Трихлорид фосфора. Трибромид фосфора. Трииодид фосфора. Фосфан | ||
| Другие катионы | Трехфтористый азот. Трифторид мышьяка. Трифторид сурьмы. Трифторид висмута | ||
| Связанные лиганды | Окись углерода | ||
| Родственные соединения | Пентафторид фосфора | ||
| Страница дополнительных данных | |||
| Структура и. свойства | Показатель преломления (n),. Диэлектрическая проницаемость (εr) и т.д. | ||
| Термодинамические. данные | Фазовое поведение. твердое тело– жидкость – газ | ||
| Спектральные данные | UV, IR, ЯМР, MS | ||
| Если не указано иное, данные для материалов приведены в их стандарте состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки в ink | |||
Трифторид фосфора (формула P F 3), представляет собой газ без цвета и запаха . Он очень токсичен и медленно вступает в реакцию с водой. Его основное применение - в качестве лиганда в металлических комплексах. В качестве лиганда он аналогичен окиси углерода в карбонилам металлов, и, действительно, его токсичность обусловлена его связыванием с железом в крови гемоглобином Аналогично угарному газу.
Трифторид фосфора имеет валентный угол F-P-F приблизительно 96,3 °. Газообразный PF3имеет стандартную энтальпию образования -945 кДж / моль (-226 ккал / моль ). Атом фосфора имеет химический сдвиг ядерного магнитного резонанса 97 ppm (слабое поле H3PO4 ).
Трифторид фосфора гидролизуется особенно при высоком pH, но он менее чувствителен к гидролизу, чем трихлорид фосфора. Он не повреждает стекло, за исключением высоких температур, и безводный гидроксид калия можно использовать для его сушки с небольшими потерями. С горячими металлами образуются фосфиды и фториды. С основаниями Льюиса, такими как аммиак, образуются продукты присоединения (аддукты), и PF 3 окисляется окислителями, такими как бром или перманганат калия.
В качестве лиганда для переходных металлов PF 3 является сильным π-акцептором. Он образует различные комплексы металлов с металлами в низких степенях окисления. PF 3 образует несколько комплексов, для которых соответствующие производные CO (см. карбонил металла ) нестабильны или отсутствуют. Таким образом, Pd (PF 3)4известен, а Pd (CO) 4 - нет. Такие комплексы обычно получают непосредственно из соединения родственного карбонила металла с потерей CO. Однако никель металл непосредственно реагирует с PF 3 при 100 ° C и давлении 35 МПа с образованием Ni. (PF 3)4, который аналогичен Ni (CO) 4. Cr (PF 3)6, аналог Cr (CO) 6, может быть получен из дибензолхрома :
 |  |
Трифторид фосфора обычно получают из трихлорида фосфора путем галогенового обмена с использованием различных фторидов, таких как фтористый водород, фторид кальция, трифторид мышьяка, трифторид сурьмы или фторид цинка :
Трифторид фосфора аналогичен монооксид углерода в том смысле, что это газ, который прочно связывается с железом в гемоглобине, предотвращая поглощение кислородом крови.
PF3очень токсичен, сравним с фосгеном.