| Фосфоглицераткиназа | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 | |||||||||
| Идентификаторы | |||||||||
| Номер ЕС | 2.7.2.3 | ||||||||
| Номер CAS | 9001- 83-6 | ||||||||
| Базы данных | |||||||||
| IntEnz | Представление IntEnz | ||||||||
| BRENDA | Запись BRENDA | ||||||||
| ExPASy | Представление NiceZyme | ||||||||
| KEGG | Запись KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| PRIAM | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| Онтология гена | AmiGO / QuickGO | ||||||||
| |||||||||
| Фосфоглицераткиназа | |||||||||
|---|---|---|---|---|---|---|---|---|---|
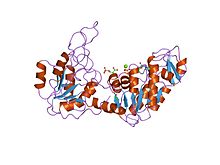 Структура дрожжевой фосфоглицераткиназы. Структура дрожжевой фосфоглицераткиназы. | |||||||||
| Идентификаторы | |||||||||
| Символ | PGK | ||||||||
| Pfam | PF00162 | ||||||||
| InterPro | IPR001576 | ||||||||
| PROSITE | PDOC00102 | ||||||||
| SCOPe | 3pgk / SUPFAM | ||||||||
| |||||||||
Фосфоглицераткиназа (EC 2.7.2.3 ) (PGK 1) - это фермент, который катализирует обратимый перенос фосфатной группы от 1,3-бисфосфоглицерата (1,3-BPG) к ADP с образованием 3-фосфоглицерата (3-PG) и АТФ :
Как и все киназы, это трансфераза. PGK является основным ферментом, используемым в гликолизе, на первом этапе выработки АТФ гликолитического пути. В глюконеогенезе реакция, катализируемая PGK, протекает в противоположном направлении, генерируя АДФ и 1,3-BPG.
У людей к настоящему времени идентифицированы два изофермента PGK: PGK1 и PGK2. Изоферменты имеют 87-88% идентичность последовательностей аминокислот, и хотя они структурно и функционально похожи, они имеют разную локализацию: PGK2, кодируемый аутосомным геном, уникален для мейоза и постмейотические сперматогенные клетки, тогда как PGK1, кодируемый на Х-хромосоме, повсеместно экспрессируется во всех клетках.
 Диаграмма, показывающая гликолитические и глюконеогенные пути. Обратите внимание, что фосфоглицераткиназа используется в обоих направлениях.
Диаграмма, показывающая гликолитические и глюконеогенные пути. Обратите внимание, что фосфоглицераткиназа используется в обоих направлениях. PGK присутствует во всех живых организмах как один из двух ферментов, генерирующих АТФ при гликолизе. В глюконеогенном пути PGK катализирует обратную реакцию. В биохимических стандартных условиях гликолитическое направление является предпочтительным.
В цикле Кальвина в фотосинтетических организмах PGK катализирует фосфорилирование 3- PG, продуцирующий 1,3-BPG и ADP, как часть реакций, регенерирующих рибулозо-1,5-бисфосфат.
PGK, как сообщается, проявляет активность тиол редуктазы на плазмин, приводящий к образованию ангиостатина, который ингибирует ангиогенез и рост опухоли. Было также показано, что фермент участвует в репликации ДНК и репарации в ядрах клеток млекопитающих .
. Было показано, что человеческий изофермент PGK2, который экспрессируется только во время сперматогенеза, необходим для функции сперматозоидов у мышей..
Нажмите на гены, белки и метаболиты ниже, чтобы ссылаться на соответствующие статьи.
[[File: [[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]]
[[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]][[]] | {{{bSize}}} px | alt = Гликолиз и глюконеогенез редактировать ]] Гликолиз и глюконеогенез редактировать
| {{{bSize}}} px | alt = Гликолиз и глюконеогенез редактировать ]] Гликолиз и глюконеогенез редактировать PGK обнаружен во всех живых организмах, и его последовательность высококонсервативный на протяжении всей эволюции. Фермент существует в виде 415- остатков мономера, содержащего два домена почти одинакового размера, которые соответствуют N- и C-концам белка. 3-фосфоглицерат (3-PG) связывается с N-концом, тогда как нуклеотидные субстраты, MgATP или MgADP, связываются с C-концевым доменом фермента. Эта расширенная двухдоменная структура связана с крупномасштабными конформационными изменениями «шарнирного изгиба», аналогичными тем, которые обнаруживаются в гексокиназе. Два домена белка разделены щелью и связаны двумя альфа-спиралями. В основе каждого домена лежит 6-ти нитевой параллельный бета-лист, окруженный альфа-спиралями. Две доли способны сворачиваться независимо, что согласуется с присутствием промежуточных продуктов на пути сворачивания с одним сложенным доменом. Хотя связывание любого из субстратов вызывает конформационное изменение, закрытие домена происходит только в результате связывания обоих субстратов, что приводит к переносу фосфатной группы.
Фермент имеет тенденцию к существуют в открытой конформации с короткими периодами закрытия и катализа, которые делают возможной быструю диффузию субстрата и продуктов через сайты связывания; открытая конформация PGK более конформационно стабильна из-за экспонирования гидрофобной области белка при закрытии домена.
Ионы магния обычно образуют комплексы к фосфатным группам нуклеотидных субстратов PGK. Известно, что в отсутствие магния ферментативная активность отсутствует. двухвалентный металл помогает ферменту лигандам экранировать отрицательные заряды связанной фосфатной группы, обеспечивая возможность нуклеофильной атаки ; такая стабилизация заряда является типичной характеристикой реакции фосфопереноса. Предполагается, что ион может также способствовать закрытию домена, когда PGK связывает оба субстрата.
 Механизм фосфоглицераткиназы в гликолизе.
Механизм фосфоглицераткиназы в гликолизе. Не связанный ни с одним из субстратов, PGK существует в «открытом» соответствие. После связывания как триозного, так и нуклеотидного субстратов с N- и С-концевыми доменами, соответственно, происходит обширное движение изгиба шарнира, сближающее домены и связанные с ними субстраты и приводящее к «закрытой» конформации. Затем, в случае прямой гликолитической реакции, бета-фосфат АДФ инициирует нуклеофильную атаку на 1-фосфат 1,3-BPG. Lys219 на ферменте направляет фосфатную группу к субстрату.
PGK проходит через переходное состояние со стабилизированным зарядом , которое предпочтительнее по сравнению с расположением связанного субстрата в замкнутом ферменте, потому что в переходном состоянии все три фосфатных атома кислорода стабилизируются лиганды, в отличие от только двух стабилизированных атомов кислорода в исходном связанном состоянии.
В гликолитическом пути 1,3-BPG представляет собой донор фосфата и имеет высокий потенциал переноса фосфорила. Катализируемый PGK перенос фосфатной группы от 1,3-BPG к ADP с образованием АТФ может привести в действие реакцию окисления углерода на предыдущей стадии гликолиза (преобразование глицеральдегид-3-фосфат в 3- фосфоглицерат ).
Фермент активируется низкими концентрациями различных поливалентных анионов, таких как пирофосфат, сульфат, фосфат и цитрат. Высокие концентрации MgATP и 3-PG активируют PGK, тогда как Mg2 + в высоких концентрациях неконкурентно ингибирует фермент.
PGK проявляет широкую специфичность в отношении нуклеотидных субстратов. Его активность подавляется салицилатами, которые, по-видимому, имитируют нуклеотидный субстрат фермента.
Макромолекулярное скопление увеличивает активность PGK как в компьютерном моделировании, так и в in vitro средах, имитирующих внутреннюю часть клетки; в результате скопления фермент становится более ферментативно активным и более компактным.
Дефицит фосфоглицераткиназы (PGK) - это Х-сцепленный рецессивный признак, связанный с гемолитической анемией, психические расстройства и миопатия у человека в зависимости от формы - существует гемолитическая форма и миопатическая форма. Поскольку признак X-сцеплен, он обычно полностью выражается у мужчин, у которых есть одна X-хромосома; пораженные женщины обычно протекают бессимптомно. Состояние является результатом мутаций в Pgk1, гене, кодирующем PGK1, и было идентифицировано двадцать мутаций. На молекулярном уровне мутация в Pgk1 ухудшает термическую стабильность и подавляет каталитическую активность фермента. PGK - единственный фермент в непосредственном гликолитическом пути, кодируемый X-связанным геном. В случае гемолитической анемии дефицит PGK возникает в эритроцитах. В настоящее время не существует окончательного лечения дефицита PGK.
Сверхэкспрессия PGK1 связана с раком желудка и, как было обнаружено, увеличивает инвазивность клеток рака желудка in vitro. Фермент секретируется опухолевыми клетками и участвует в ангиогенном процессе, что приводит к высвобождению ангиостатина и ингибированию роста кровеносных сосудов опухоли.
Благодаря своему Имея широкую специфичность в отношении нуклеотидных субстратов, PGK, как известно, участвует в фосфорилировании и активации HIV антиретровирусных препаратов, которые основаны на нуклеотидах.
|
| ||||||||||||||||||||||||||||||||||||||||||||
.