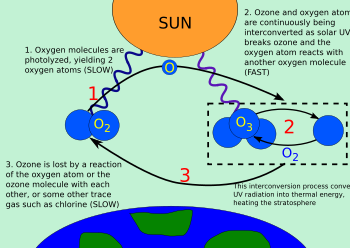
 Озон-кислородный цикл в озоновом слое : 1. Кислород фотолизируется до атомарного кислорода 2. Кислород и озон непрерывно взаимопревращаются. Солнечное УФ расщепляет кислород; молекулярный и атомарный кислород вместе образуют озон. 3. Озон теряется при реакции с атомарным кислородом (плюс другие следовые атомы).
Озон-кислородный цикл в озоновом слое : 1. Кислород фотолизируется до атомарного кислорода 2. Кислород и озон непрерывно взаимопревращаются. Солнечное УФ расщепляет кислород; молекулярный и атомарный кислород вместе образуют озон. 3. Озон теряется при реакции с атомарным кислородом (плюс другие следовые атомы). Озон кислородного цикл представляет собой процесс, посредством которого озон непрерывно регенерирует в Землях «ы стратосфере, превращая ультрафиолетовое излучение (УФ) в теплый. В 1930 году Сидней Чепмен решил проблему химии. Атмосферные ученые обычно называют этот процесс циклом Чепмена.
Большая часть производства озона происходит в тропических верхних слоях стратосферы и мезосферы. Общая масса озона, производимого в день на земном шаре, составляет около 400 миллионов метрических тонн. Глобальная масса озона относительно постоянна и составляет около 3 миллиардов метрических тонн, что означает, что Солнце производит около 12% озонового слоя каждый день.
| Часть серии по |
| Биогеохимические циклы |
|---|
 |
| Круговорот воды |
| Углеродный цикл |
| Питательный цикл |
| Рок-цикл |
| Морской цикл |
| Метановый цикл |
| Другие циклы |
| похожие темы |
| Исследовательские группы |
|
Общее количество озона в стратосфере определяется балансом между производством за счет солнечной радиации и удалением. Скорость удаления низкая, так как концентрация свободных атомов O очень мала.
В дополнение к только что упомянутым реакциям некоторые свободные радикалы, наиболее важными из которых являются гидроксил (ОН), оксид азота (NO) и атомы хлора (Cl) и брома (Br), катализируют реакцию рекомбинации, приводя к образованию озонового слоя, который тоньше, чем было бы без катализаторов.
Большая часть ОН и NO естественным образом присутствует в стратосфере, но деятельность человека, особенно выбросы хлорфторуглеродов ( ХФУ ) и галонов, значительно увеличила концентрации Cl и Br, что привело к истощению озонового слоя. Каждый атом Cl или Br может катализировать десятки тысяч реакций разложения, прежде чем он будет удален из стратосферы.