
Осмос в U-образной трубке
Осмотическое давление - это минимальное давление, которое необходимо наносится на раствор для предотвращения попадания внутрь потока его чистого растворителя через полупроницаемую мембрану. Он также определяется как мера способности раствора впитывать чистый растворитель при осмосе. Потенциальное осмотическое давление - это максимальное осмотическое давление, которое могло бы развиться в растворе, если бы он был отделен от чистого растворителя полупроницаемой мембраной.
Осмос происходит, когда два раствора, содержащие разные концентрации растворенного вещества, разделены селективно проницаемой мембраной. Молекулы растворителя проходят предпочтительно через мембрану из раствора с низкой концентрацией в раствор с более высокой концентрацией растворенного вещества. Перенос молекул растворителя будет продолжаться до тех пор, пока не будет достигнуто равновесие.
Содержание
- 1 Теория и измерения
- 2 Приложения
- 3 Вывод формулы Ван 'т Гоффа
- 4 См. Также
- 5 Ссылки
- 6 Внешние ссылки
Теория и измерения

A
Ячейка Пфеффера, использованная для ранних измерений осмотического давления
Якобус ван'т-Хофф обнаружил количественную зависимость между осмотическим давлением и концентрацией растворенных веществ выражается в следующем уравнении:

, где  - осмотическое давление, i - безразмерное индекс Ван 'т-Гоффа, c - молярная концентрация растворенного вещества, R - постоянная идеального газа, а T - температура в кельвинах. Эта формула применяется, когда концентрация растворенного вещества достаточно мала, чтобы раствор можно было рассматривать как идеальный раствор. Пропорциональность концентрации означает, что осмотическое давление является коллигативным свойством. Обратите внимание на сходство этой формулы с законом идеального газа в форме
- осмотическое давление, i - безразмерное индекс Ван 'т-Гоффа, c - молярная концентрация растворенного вещества, R - постоянная идеального газа, а T - температура в кельвинах. Эта формула применяется, когда концентрация растворенного вещества достаточно мала, чтобы раствор можно было рассматривать как идеальный раствор. Пропорциональность концентрации означает, что осмотическое давление является коллигативным свойством. Обратите внимание на сходство этой формулы с законом идеального газа в форме  где n - общее количество молей молекул газа в объеме V, а n / V - молярная концентрация молекул газа. Хармон Нортроп Морс и Фрейзер показали, что уравнение применимо к более концентрированным растворам, если единица измерения концентрации была моль, а не моляр ; поэтому при использовании моляльности это уравнение было названо уравнением Морса .
где n - общее количество молей молекул газа в объеме V, а n / V - молярная концентрация молекул газа. Хармон Нортроп Морс и Фрейзер показали, что уравнение применимо к более концентрированным растворам, если единица измерения концентрации была моль, а не моляр ; поэтому при использовании моляльности это уравнение было названо уравнением Морса .
. Для более концентрированных растворов уравнение Ван'т-Гоффа может быть расширено в виде степенного ряда по концентрации растворенного вещества c. В первом приближении

, где  - идеальное давление, а A - эмпирический параметр. Значение параметра A (и параметров из приближений более высокого порядка) можно использовать для вычисления параметров Питцера. Эмпирические параметры используются для количественной оценки поведения растворов ионных и неионных растворенных веществ, которые не являются идеальными растворами в термодинамическом смысле.
- идеальное давление, а A - эмпирический параметр. Значение параметра A (и параметров из приближений более высокого порядка) можно использовать для вычисления параметров Питцера. Эмпирические параметры используются для количественной оценки поведения растворов ионных и неионных растворенных веществ, которые не являются идеальными растворами в термодинамическом смысле.
Ячейка Пфеффера была разработана для измерения осмотического давления.
Применения
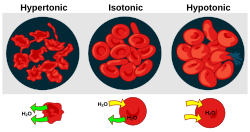
Осмотическое давление на эритроциты
Измерение осмотического давления может использоваться для определения молекулярных масс.
Осмотическое давление является важным фактором, влияющим на клетки. Осморегуляция - это механизм гомеостаза организма для достижения баланса осмотического давления.
- Гипертоничность - это наличие раствора, вызывающего сокращение клеток.
- Гипотоничность - это присутствие раствора, вызывающего набухание клеток.
- Изотоничность - наличие раствор, не вызывающий изменения объема клетки.
Когда биологическая клетка находится в гипотонической среде, внутри клетки накапливается вода, вода течет через клеточную мембрану в ячейку, заставляя ее расширяться. В растительных клетках клеточная стенка ограничивает расширение, что приводит к давлению на клеточную стенку изнутри, называемому тургорным давлением. Давление тургора позволяет травянистым растениям стоять вертикально. Это также определяющий фактор того, как растения регулируют апертуру своих устьиц. В клетках животных чрезмерное осмотическое давление может приводить к цитолизу.
Осмотическое давление является основой фильтрации («обратный осмос »), процесса, обычно используемого при очистке воды. Очищаемая вода помещается в камеру и подвергается давлению, превышающему осмотическое давление, оказываемое водой и растворенными в ней растворенными веществами. Часть камеры открывается для дифференциально проницаемой мембраны, которая пропускает молекулы воды, но не растворенные частицы. Осмотическое давление океанской воды составляет около 27 атм. Обратный осмос опресняет пресную воду из морской соленой воды.
Вывод формулы Ван 'т Гоффа
Рассмотрим систему в точке, когда она достигла равновесия. Условием для этого является то, что химический потенциал растворителя (так как только он может свободно течь в направлении равновесия) на обеих сторонах мембраны. Отделение, содержащее чистый растворитель, имеет химический потенциал  , где
, где  - давление. С другой стороны, в отделении, содержащем растворенное вещество, химический потенциал растворителя зависит от мольной доли растворителя,
- давление. С другой стороны, в отделении, содержащем растворенное вещество, химический потенциал растворителя зависит от мольной доли растворителя,
- μ v 0 (p) = μ v (xv, p + Π) {\ displaystyle \ mu _ {v} ^ {0} (p) = \ mu _ {v} (x_ {v}, p + \ Pi)}
 .
.
Здесь разница в давлении двух отсеков Π ≡ p '- p {\ displaystyle \ Pi \ Equiv p'-p} определяется как осмотическое давление, оказываемое растворенными веществами. Удерживая давление, добавление растворенного вещества снижает химический потенциал (энтропийный эффект ). Таким образом, давление раствора необходимо увеличить, чтобы компенсировать потерю химического потенциала.
определяется как осмотическое давление, оказываемое растворенными веществами. Удерживая давление, добавление растворенного вещества снижает химический потенциал (энтропийный эффект ). Таким образом, давление раствора необходимо увеличить, чтобы компенсировать потерю химического потенциала.
Чтобы найти Π {\ displaystyle \ Pi} , осмотическое давление, мы рассматриваем равновесие между раствором, содержащим растворенное вещество, и чистой водой.
, осмотическое давление, мы рассматриваем равновесие между раствором, содержащим растворенное вещество, и чистой водой.
- μ v (xv, p + Π) = μ v 0 (p) {\ displaystyle \ mu _ {v} (x_ {v}, p + \ Pi) = \ mu _ {v} ^ {0} ( p)}
 .
.
Мы можем записать левую часть как:
- μ v (xv, p + Π) = μ v 0 (p + Π) + RT ln (γ vxv) {\ displaystyle \ mu _ {v} (x_ {v}, p + \ Pi) = \ mu _ {v} ^ {0} (p + \ Pi) + RT \ ln (\ gamma _ {v} x_ {v})}
 ,
,
где γ v {\ displaystyle \ gamma _ {v}} - коэффициент активности растворителя. Произведение γ vxv {\ displaystyle \ gamma _ {v} x_ {v}}
- коэффициент активности растворителя. Произведение γ vxv {\ displaystyle \ gamma _ {v} x_ {v}} также известно как активность растворителя, которая для воды является активностью воды aw {\ displaystyle a_ {w}}
также известно как активность растворителя, которая для воды является активностью воды aw {\ displaystyle a_ {w}} . Дополнение к давлению выражается выражением для энергии расширения:
. Дополнение к давлению выражается выражением для энергии расширения:
- μ vo (p + Π) = μ v 0 (p) + ∫ pp + Π V m (p ′) dp ′ {\ displaystyle \ mu _ {v} ^ {o} (p + \ Pi) = \ mu _ {v} ^ {0} (p) + \ int _ {p} ^ {p + \ Pi} \! V_ {m} (p ') \, \ mathrm {d} p '}
 ,
,
где V m {\ displaystyle V_ {m}} - молярный объем (м³ / моль). Вставив выражение, представленное выше, в уравнение химического потенциала для всей системы и перегруппировав, получим:
- молярный объем (м³ / моль). Вставив выражение, представленное выше, в уравнение химического потенциала для всей системы и перегруппировав, получим:
- - RT ln (γ vxv) = ∫ pp + Π V m (p ′) dp ′ {\ displaystyle -RT \ ln (\ gamma _ {v} x_ {v}) = \ int _ {p} ^ {p + \ Pi} \! V_ {m} (p ') \, \ mathrm {d} p'}
 .
.
Если жидкость несжимаема, молярный объем постоянен, V m (p ') ≡ V m {\ displaystyle V_ {m} (p') \ Equiv V_ {m}} , а интеграл становится Π V m {\ displaystyle \ Pi V_ {m}}
, а интеграл становится Π V m {\ displaystyle \ Pi V_ {m}} . Таким образом, мы получаем
. Таким образом, мы получаем
- Π = - (RT / V m) ln (γ vxv) {\ displaystyle \ Pi = - (RT / V_ {m}) \ ln (\ gamma _ {v} x_ {v})}
 .
.
Коэффициент активности является функцией концентрации и температуры, но в случае разбавленных смесей он часто очень близок к 1,0, поэтому
- Π = - (RT / V m) ln (xv) {\ displaystyle \ Pi = - (RT / V_ {m}) \ ln (x_ {v})}
 .
.
мольная доля растворенного вещества, xs {\ displaystyle x_ {s}} , равно 1 - xv {\ displaystyle 1-x_ {v}}
, равно 1 - xv {\ displaystyle 1-x_ {v}} , поэтому ln (xv) {\ displaystyle \ ln (x_ {v})}
, поэтому ln (xv) {\ displaystyle \ ln (x_ {v})} можно заменить на ln (1 - xs) {\ displaystyle \ ln (1-x_ {s})}
можно заменить на ln (1 - xs) {\ displaystyle \ ln (1-x_ {s})} , что при xs {\ displaystyle x_ { s}}
, что при xs {\ displaystyle x_ { s}} маленький, может быть приблизительно равен - xs {\ displaystyle -x_ {s}}
маленький, может быть приблизительно равен - xs {\ displaystyle -x_ {s}} .
.
- Π = (RT / V m) xs {\ displaystyle \ Pi = (RT / V_ {m}) x_ {s}}
 .
.
Мольная доля xs {\ displaystyle x_ {s}} равна ns / (ns + nl) {\ displaystyle n_ {s} / (n_ {s} + n_ {l})}
равна ns / (ns + nl) {\ displaystyle n_ {s} / (n_ {s} + n_ {l})} . Когда xs {\ displaystyle x_ {s}}
. Когда xs {\ displaystyle x_ {s}} мало, его можно приблизительно оценить как xs = ns / nl {\ displaystyle x_ {s} = n_ {s} / n_ { l}}
мало, его можно приблизительно оценить как xs = ns / nl {\ displaystyle x_ {s} = n_ {s} / n_ { l}} . Кроме того, молярный объем V m {\ displaystyle V_ {m}}
. Кроме того, молярный объем V m {\ displaystyle V_ {m}} может быть записан как объем на моль, V m = V / nl {\ displaystyle V_ {m} = V / n_ {l}}
может быть записан как объем на моль, V m = V / nl {\ displaystyle V_ {m} = V / n_ {l}} . Их объединение дает следующее.
. Их объединение дает следующее.
- Π = c R T {\ displaystyle \ Pi = cRT}
 .
.
Для водных растворов солей необходимо учитывать ионизацию. Например, 1 моль NaCl ионизируется до 2 моль ионов.
См. Также
Ссылки
Внешние ссылки
 Осмос в U-образной трубке
Осмос в U-образной трубке  A Ячейка Пфеффера, использованная для ранних измерений осмотического давления
A Ячейка Пфеффера, использованная для ранних измерений осмотического давления 




 Осмотическое давление на эритроциты
Осмотическое давление на эритроциты 

 .
.

 .
. ,
,


 ,
,
 .
.

 .
. .
.





 .
.





 .
.