
Химия никельорганического происхождения - это раздел металлоорганической химии, посвященный органическим соединениям со связями никель - углерод. Они используются в качестве катализатора, в качестве строительного материала в органической химии и химическом осаждении из паровой фазы. Никелевоорганические соединения также являются короткоживущими промежуточными продуктами в органических реакциях. Первым никелевоорганическим соединением был тетракарбонил никеля Ni (CO) 4, о котором было сообщено в 1890 году и которое быстро применялось в процессе Монда для очистки никеля. Никелевоорганические комплексы используются во многих промышленных процессах, включая карбонилирование, гидроцианирование и процесс получения высших олефинов Shell.

Существует множество комплексов никеля, координированных с алкеном. В этих соединениях никель формально является нульвалентным Ni, и связывание описывается с помощью модели Дьюара – Чатта – Дункансона. Одним из распространенных представителей является бис (циклооктадиен) никель (0) (Ni (COD) 2), который содержит два циклооктадиеновых лиганда. Это соединение 18VE с 10 электронами, обеспечиваемыми самим никелем, и еще 4x2 электронами за счет двойных связей. Это твердое вещество, плавящееся при 60 ° C, используется в качестве катализатора и в качестве предшественника для многих других соединений никеля.

Аллил галогениды реагируют с Ni (CO) 4 с образованием пи-аллильных комплексов, (аллил) 2Ni2Cl2. Эти соединения, в свою очередь, являются источниками аллильных нуклеофилов. В (аллил) 2Ni2Br2и (аллил) Ni (C 5H5) никелю присвоена степень окисления +2, а количество электронов составляет 16 и 18 соответственно.

Никелоцен NiCp 2 со степенью окисления +2 Ni и 20 валентными электронами являются основным металлоценом никеля. Его можно окислить одним электроном. Соответствующие палладоцен и платиноцен неизвестны. Из никелоцена получают множество производных, например CpNiLCl, CpNiNO и Cp 2Ni2(CO) 3.
Никель образует карбеновые комплексы, формально содержащие двойные связи C = Ni.
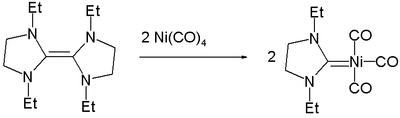
Известны разнообразные алкильные и арильные комплексы Ni (II). Примеры включают [(dppf) Ni (циннамил) Cl)], транс- (PCy 2 Ph) 2 Ni (о-толил) Cl]], (dppf) Ni (o -толил) Cl]], (TMEDA) Ni (о-толил) Cl и (TMEDA) NiMe 2.
 Синтез [(TMEDA) Ni (о-толил) Cl].
Синтез [(TMEDA) Ni (о-толил) Cl]. Соединения никеля типа NiR 2 также существуют всего с 12 валентными электронами. Однако в растворе растворитель всегда взаимодействует с атомом металла, увеличивая количество электронов. Одно соединение 12 VE представляет собой ди (мезитил) никель, полученный из (аллила) 2Ni2Br2и соответствующего реактива Гриньяра.
Соединения никеля катализируют олигомеризацию алкенов и алкины. Это свойство подтвердило результаты исследований и разработок катализаторов Циглера-Натта в 1950-х годах. Об этом открытии свидетельствуют примеси никеля, происходящие из автоклава, которые убили реакция распространения (Aufbau) в пользу реакции обрыва до концевого алкена : полимеризация этилена внезапно остановилась на 1-бутен. Этот так называемый эффект никеля побудил к поиску других катализаторов, способных к этой реакции, что привело к обнаружению новых катализаторов, которые технически производили полимеры с высокой молярной массой, такие как современные катализаторы Циглера. –Катализаторы Натта.
Один практический инструмент олигомеризация алкинов представляет собой Reppe Synthesis ; например, при синтезе циклооктатетраена :
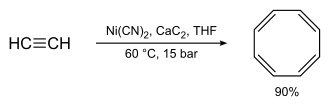
это формальное [2 + 2 + 2 + 2] циклоприсоединение. Олигомеризация бутадиена с этиленом в транс-1,4-гексадиен одно время была промышленным процессом.
Формальные [2 + 2 + 2] циклоприсоединения также имеют место при тримеризации алкина. Эта расширяемая тримеризация обычно может включать бензин. Бензин образуется in situ из соединения бензола, присоединенного к трифлату и триметилсилил заместителю в орто- положений и реагирует с диином, таким как 1,7-октадиин, вместе с каталитической системой бромид никеля (II) / цинк (NiBr 2бис (дифенилфосфино) этан / Zn) для синтеза соответствующего производного нафталина.

В каталитическом цикле элементарный цинк служит для восстановления никеля (II) до никеля (0), который затем может координировать две алкиновые связи. Стадия циклометаллирования следует за промежуточным никельциклопентадиеном и затем координированием бензина, что дает реакцию внедрения C-H в соединение никельциклогептатриена. Восстановительное отщепление высвобождает тетрагидроантраценовое соединение.
Образование никелевых органических соединений в этом типе реакции не всегда очевидно, но в тщательно разработанном эксперименте два таких промежуточных продукта образуются количественно:
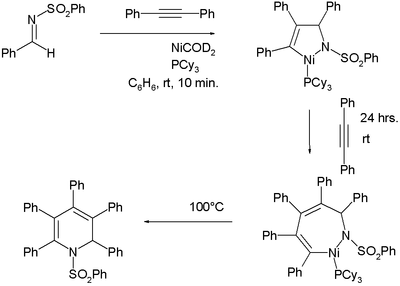
В одном исследовании отмечено, что эта реакция работает только с самим ацетиленом. или с простыми алкинами из-за плохой региоселективности. От концевого алкина 7 изомеров, возможно, различаются положением заместителей или положениями двойной связи. Одна из стратегий решения этой проблемы использует определенные диины:

Выбранные условия реакции также минимизируют количество образовавшегося конкурирующего продукта [2 + 2 + 2] циклоприсоединения к соответствующему замещенному арену.
Соединения никеля вызывают реакцию связывания между аллилом и арил галогенидами. Другими реакциями сочетания с участием никеля в каталитических количествах являются сочетание Кумада и сочетание Негиши.

Ni катализирует добавление оксид углерода на алкены и алкины. Промышленное производство акриловой кислоты когда-то состояло из объединения ацетилена, оксида углерода и воды при 40-55 атм и 160-200 ° C с бромид никеля (II) и галогенид меди.
