 | |
| Имена | |
|---|---|
| Название IUPAC Сульфид никеля (II) | |
| Другие названия сульфид никеля, моносульфид никеля, сульфид никеля | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.037.113 |
| Номер EC |
|
| PubChem CID | |
| Номер RTECS |
|
| Панель управления CompTox (EPA ) | |
УЛЫБКА
| |
| Свойства | |
| Химическая формула | NiS |
| Молярная масса | 90,7584 г · моль |
| Внешний вид | твердое вещество черного цвета |
| Запах | Без запаха |
| Плотность | 5,87 г / см |
| Температура плавления | 797 ° C (1467 ° F; 1070 K) |
| Точка кипения | 1388 ° C (2530 ° F; 1,661 K) |
| Растворимость в воде | нерастворимый |
| Растворимость | растворимый в азотной кислоте |
| Магнитный восприимчивость (χ) | + 190,0 · 10 см / моль |
| Структура | |
| Кристаллическая структура | гексагональная |
| Опасности | |
| Основные опасности | может вызвать рак при вдыхании |
| Пиктограммы GHS |  |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
Сульфид никеля представляет собой неорганическое соединение с формулой NiS. Это твердое вещество черного цвета, которое получают обработкой солей никеля (II) с помощью сероводорода. Известно много сульфидов никеля, включая минерал миллерит, который также имеет формулу NiS. Помимо полезных руд, сульфиды никеля являются продуктами реакций обессеривания и иногда используются в качестве катализаторов. Известны нестехиометрические формы сульфида никеля, например, Ni 9S8и Ni 3S2.
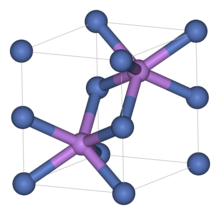
Подобно многим родственным материалам, сульфид никеля использует мотив арсенида никеля. В этой структуре никель является октаэдрическим, а сульфидные центры находятся в тригонально-призматических узлах.
Сульфид никеля имеет два полиморфа. Α-фаза имеет гексагональную элементарную ячейку, а β-фаза - ромбоэдрическую ячейку. Α-фаза стабильна при температурах выше 379 ° C (714 ° F) и превращается в β-фазу при более низких температурах. Этот фазовый переход вызывает увеличение объема на 2-4%.
Осаждение твердого черного сульфида никеля является основой традиционного качественного неорганического анализ схемы, который начинается с разделения металлов по растворимости их сульфидов. Такие реакции записываются:
Было разработано множество других более контролируемых методов, включая реакции метатезиса в твердом состоянии (из NiCl 2 и Na 2 S) и высокотемпературные реакции элементов.
Минерал миллерит также является сульфидом никеля с молекулярной формулой NiS, хотя его структура отличается от синтетического стехиометрического NiS из-за условий, в которых он образуется. Он встречается в естественных условиях в низкотемпературных гидротермальных системах, в полостях карбонатных пород и как побочный продукт других никелевых минералов.
 Кристаллы миллерита
Кристаллы миллерита Флоат-стекло содержит небольшое количество сульфида никеля, образованного из серы в осветляющем агенте Na. 2SO. 4и никеле, содержащемся в загрязнителях металлических сплавов.
Включения сульфида никеля представляют собой проблему для применения в закаленном стекле. После отпуска включения сульфида никеля находятся в метастабильной альфа-фазе. В конечном итоге включения переходят в бета-фазу (стабильную при низкой температуре), увеличиваясь в объеме и вызывая трещины в стекле. В середине закаленного стекла материал находится под растяжением, что вызывает распространение трещин и приводит к самопроизвольному разрушению стекла. Это самопроизвольное разрушение происходит спустя годы или десятилетия после изготовления стекла.