| NAD-киназа | |||||||||
|---|---|---|---|---|---|---|---|---|---|
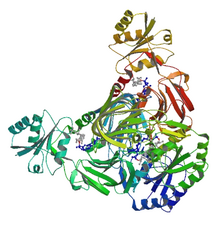 Ленточная диаграмма NAD-киназы в комплексе с субстратами. Ленточная диаграмма NAD-киназы в комплексе с субстратами. | |||||||||
| Идентификаторы | |||||||||
| Номер ЕС | 2.7.1.23 | ||||||||
| Номер CAS | 9032-66-0 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| BRENDA | Запись BRENDA | ||||||||
| ExPASy | Обзор NiceZyme | ||||||||
| KEGG | Запись KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| PRIAM | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| Онтология генов | AmiGO / QuickGO | ||||||||
| |||||||||
киназа NAD (EC 2.7.1.23, NADK) - это фермент, который превращает никотинамид адениндинуклеотид (НАД) в НАДФ посредством фосфорилирования кофермента НАД . НАДФ представляет собой незаменимый кофермент, который восстанавливается до НАДФН, главным образом, с помощью пентозофосфатного пути, чтобы обеспечить снижение мощности в процессах биосинтеза, таких как биосинтез жирных кислот и синтез нуклеотидов. Структура NADK из архей Archaeoglobus fulgidus была определена.
У человека гены NADK и MNADK кодируют локализованные киназы NAD в цитозоле и митохондриях соответственно. Точно так же дрожжи имеют как цитозольные, так и митохондриальные изоформы, а митохондриальная изоформа дрожжей принимает как НАД, так и НАДН в качестве субстратов для фосфорилирования.
НАДК фосфорилирует НАД в положении 2 'рибозного кольца, несущего адениновую составляющую. Он очень селективен в отношении своих субстратов, НАД и АТФ, и не допускает модификаций ни акцептора фосфорила, НАД, ни пиридиновой части донора фосфорила, АТФ. NADK также использует ионы металлов для координации АТФ в активном центре. Исследования in vitro с различными ионами двухвалентных металлов показали, что цинк и марганец предпочтительнее магния, в то время как медь и никель вообще не принимаются ферментом. Предлагаемый механизм включает 2'-кислород спирта, действующий как нуклеофил, чтобы атаковать гамма-фосфорил АТФ, высвобождая АДФ.
 Предлагаемый механизм действия для фосфорилирования NAD с помощью NADK
Предлагаемый механизм действия для фосфорилирования NAD с помощью NADK NADK сильно регулируется окислительно-восстановительным состоянием клетки. В то время как НАД преимущественно находится в окисленном состоянии НАД, фосфорилированный НАДФ в основном присутствует в восстановленной форме, как НАДФН. Таким образом, NADK может модулировать ответы на окислительный стресс, контролируя синтез NADP. Показано, что бактериальный НАДК аллостерически ингибируется как НАДФН, так и НАДН. Сообщается также, что NADK стимулируется связыванием кальция / кальмодулина в определенных типах клеток, таких как нейтрофилы. Было обнаружено, что киназы NAD в растениях и яйцах морских ежей связывают кальмодулин.
Из-за важной роли NADPH в биосинтезе липидов и ДНК и гиперпролиферативной природы большинства видов рака, НАДК является привлекательной мишенью для лечения рака. Кроме того, НАДФН необходим для антиоксидантной активности тиоредоксинредуктазы и глутаредоксина. Тионикотинамид и другие аналоги никотинамида являются потенциальными ингибиторами NADK, и исследования показывают, что лечение раковых клеток толстой кишки тионикотинамидом подавляет цитозольный пул NADPH, увеличивая окислительный стресс и синергетически с химиотерапией.
Хотя роль NADK в увеличении пула NADPH, по-видимому, обеспечивает защиту от апоптоза, также есть случаи, когда активность NADK, по-видимому, усиливает гибель клеток. Генетические исследования, проведенные на линиях гаплоидных клеток человека, показывают, что отключение NADK может защищать от некоторых неапоптотических стимулов.