 Различные типы гликанов, продуцируемых разными организмами.
Различные типы гликанов, продуцируемых разными организмами. N-связанное гликозилирование, представляет собой присоединение олигосахарид, углевод, состоящий из нескольких молекул сахара, иногда также называемый гликаном, с атомом азота (амидный азот аспарагина (Asn) остаток белка ) в процессе, называемом N-гликозилирование, изученном в биохимии. Этот тип связи важен как для структуры, так и для функции некоторых эукариотических белков. Процесс N-связанного гликозилирования происходит у эукариот и широко у архей, но очень редко у бактерий. Природа N-связанных гликанов, прикрепленных к гликопротеину, определяется белком и клеткой, в которой он экспрессируется. Он также варьируется у видов. Разные виды синтезируют разные типы N-связанного гликана.
В гликопротеине задействованы два типа связей: связи между сахаридными остатками в гликане и связь между цепью гликана и молекулой белка.
Сахарные части связаны друг с другом в гликановой цепи через гликозидные связи. Эти связи обычно образуются между атомами углерода 1 и 4 молекул сахара. Образование гликозидной связи энергетически невыгодно, поэтому реакция связана с гидролизом двух молекул ATP.
С другой стороны, присоединение гликана Остаток белка требует распознавания консенсусной последовательности . N-связанные гликаны почти всегда присоединены к атому азота боковой цепи аспарагина (Asn), которая присутствует как часть Asn – X– Ser / Thr консенсусная последовательность, где X - любая аминокислота, кроме пролина (Pro).
В клетках животных гликан, присоединенный к аспарагину, почти неизбежно N-ацетилглюкозамин (GlcNAc) в β-конфигурации. Эта β-связь аналогична гликозидной связи между сахарными фрагментами в структуре гликана, как описано выше. Вместо того, чтобы быть присоединенным к сахарной гидроксильной группе, аномерный атом углерода присоединен к амидному азоту. Энергия, необходимая для этого связывания, поступает от гидролиза молекулы пирофосфата.
 Путь биосинтеза N-связанных гликопротеинов: синтез N- связанный гликан начинается в эндоплазматическом ретикулуме, продолжается в Гольджи и заканчивается на плазматической мембране, где N-связанные гликопротеины либо секретируются, либо внедряются в плазматическую мембрану.
Путь биосинтеза N-связанных гликопротеинов: синтез N- связанный гликан начинается в эндоплазматическом ретикулуме, продолжается в Гольджи и заканчивается на плазматической мембране, где N-связанные гликопротеины либо секретируются, либо внедряются в плазматическую мембрану. Биосинтез N-связанных гликанов происходит через 3 основных этапы:
Синтез, блочный перенос и начальная обрезка предшественника олигосахарид встречается в эндоплазматическом ретикулуме (ER). Последующая обработка и модификация олигосахаридной цепи осуществляется в аппарате Гольджи..
Таким образом, синтез гликопротеинов пространственно разделен в различных клеточных компартментах. Следовательно, тип синтезируемого N-гликана зависит от его доступности для различных ферментов, присутствующих в этих клеточных компартментах.
Однако, несмотря на разнообразие, все N-гликаны синтезируются общим путем с общей структурой гликана ядра. Структура гликана ядра по существу состоит из двух остатков N-ацетилглюкозамина и трех остатков маннозы. Затем этот сердцевинный гликан перерабатывается и модифицируется, что приводит к разнообразному диапазону структур N-гликанов.
Процесс N-связанного гликозилирования начинается с образования долихол -связанный GlcNAc сахар. Долихол представляет собой молекулу липида, состоящую из повторяющихся звеньев изопрена. Эта молекула прикреплена к мембране ER. Молекулы сахара присоединены к долихолу через пирофосфатную связь (один фосфат изначально был связан с долихолом, а второй фосфат произошел от нуклеотидного сахара). Затем цепь олигосахарида удлиняется путем добавления различных молекул сахара ступенчатым образом с образованием олигосахарида-предшественника.
Сборка этого олигосахарида-предшественника происходит в две фазы: фаза I и фаза II. Фаза I происходит на цитоплазматической стороне ER, а фаза II - на просветной стороне ER.
Молекула-предшественник, готовая к переносу в белок, состоит из 2 молекул GlcNAc, 9 молекул маннозы и 3 глюкозы.
 Поэтапный синтез предшественника олигосахарида в просвете ЭР во время N-связанного гликозилирования: диаграмма иллюстрирует этапы, происходящие как в фазе I, так и в фазе II, как описано в таблице.
Поэтапный синтез предшественника олигосахарида в просвете ЭР во время N-связанного гликозилирования: диаграмма иллюстрирует этапы, происходящие как в фазе I, так и в фазе II, как описано в таблице.
| |
| Фаза II | |
является донором остатка маннозы (образование: Dol-P + GDP-Man → Dol-P-Man + GDP), а Dol-P-Gluc является донором остатка глюкозы (образование: Dol-P + UDP-Glc → Dol-P-Glc + UDP).
| |
После образования олигосахарида-предшественника завершенный гликан переносится на возникающий полипептид в просвете мембраны ER. Эта реакция вызывается энергией, высвобождаемой при разрыве пирофосфатной связи между молекулой долихол-гликана. Перед переносом гликана на формирующийся полипептид необходимо выполнить три условия:
Олигосахарилтрансфераза - это фермент, ответственный за распознавание консенсусной последовательности и перенос предшественника гликана к акцептору полипептида, который транслируется в просвете эндоплазматического ретикулума. Таким образом, N-связанное гликозилирование является ко-трансляционным событием.
 Процессинг гликана в ER и Гольджи.
Процессинг гликана в ER и Гольджи. Процессинг N-гликана осуществляется в эндоплазматическом ретикулуме и теле Гольджи. Первоначальная обрезка молекулы-предшественника происходит в ER, а последующий процессинг происходит в Golgi.
После переноса завершенного гликана на формирующийся полипептид из структуры удаляются два остатка глюкозы. Ферменты, известные как гликозидазы, удаляют некоторые остатки сахара. Эти ферменты могут разрушать гликозидные связи с помощью молекулы воды. Эти ферменты являются экзогликозидазами, поскольку они работают только с моносахаридными остатками, расположенными на невосстанавливающем конце гликана. Считается, что этот начальный этап обрезки действует как этап контроля качества в ER для мониторинга сворачивания белка.
. После того, как белок свернут правильно, два остатка глюкозы удаляются с помощью глюкозидазы I и II. Удаление последнего третьего остатка глюкозы сигнализирует о том, что гликопротеин готов к переходу из ER в цис-Гольджи.. ER маннозидаза катализирует удаление этой конечной глюкозы. Однако, если белок не свернут должным образом, остатки глюкозы не удаляются, и, следовательно, гликопротеин не может покинуть эндоплазматический ретикулум. Белок шаперон (калнексин / кальретикулин ) связывается с развернутым или частично свернутым белком, чтобы способствовать укладке белка.
Следующий этап включает дальнейшее добавление и удаление остатков сахара в цис-Гольджи. Эти модификации катализируются гликозилтрансферазами и гликозидазами соответственно. В цис-Гольджи серия маннозидаз удаляет некоторые или все четыре остатка маннозы в α-1,2-связях. В то время как в медиальной части Гольджи гликозилтрансферазы добавляют остатки сахара к структуре гликанов ядра, давая начало трем основным типам гликанов: высокоманнозным, гибридным и сложным гликанам.
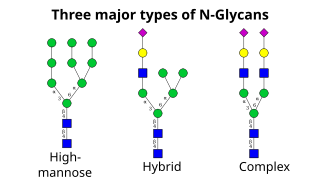 Три основных типа гликанов.
Три основных типа гликанов. Порядок добавления сахаров к растущим гликановым цепям определяется субстратной специфичностью ферментов и их доступом к субстрату при их движении через секреторный путь. Таким образом, организация этого механизма внутри клетки играет важную роль в определении того, какие гликаны производятся.
Ферменты Гольджи играют ключевую роль в определении синтеза различных типов гликанов. Порядок действия ферментов отражается в их положении в стеке Гольджи:
| Ферменты | Расположение внутри Гольджи |
|---|---|
| Маннозидаза I | цис-Гольджи |
| трансферазы GlcNAc | медиальный Гольджи |
| Галактозилтрансфераза и Сиалилтрансфераза | транс-Гольджи |
Сходный путь биосинтеза N-гликанов был обнаружен у прокариот и Археи. Однако по сравнению с эукариотами конечная структура гликанов у эубактерий и архей, по-видимому, не сильно отличается от исходного предшественника, образующегося в эндоплазматическом ретикулуме. У эукариот исходный олигосахарид-предшественник значительно модифицируется на пути к поверхности клетки.
N-связанные гликаны имеют внутренние и внешние функции.
Внутри иммунной системы. N-связанные гликаны на поверхности иммунной клетки помогут определить эту модель миграции клетки, например иммунные клетки, которые мигрируют в кожу, имеют специфические гликозилирования, которые способствуют перемещению в этот участок. Паттерны гликозилирования различных иммуноглобулинов, включая IgE, IgM, IgD, IgA и IgG, наделяют их уникальными эффекторными функциями, изменяя их сродство к Fc и другим иммунным рецепторам. Гликаны также могут участвовать в различении «себя» и «не-сам», что может иметь отношение к патофизиологии различных аутоиммунных заболеваний.
| Внутренние |
|
| Внешнее |
|
Изменения в N-связанном гликозилировании были связаны с различными заболеваниями, включая ревматоидный артрит, диабет 1 типа, болезнь Крона и раковые заболевания.
Мутации в восемнадцати генах, участвующих в N-связанном гликозилировании, приводят к множеству заболеваний, большинство из которых связано с нервная система.
Многие терапевтические белки на рынке представляют собой антитела, wh ich представляют собой N-связанные гликопротеины. Например, этанерцепт, инфликсимаб и ритуксимаб представляют собой N-гликозилированные терапевтические белки.
 Разница между гликаном, продуцируемым клетками человека и животных. В человеческих клетках отсутствует кэп Neu5Gc.
Разница между гликаном, продуцируемым клетками человека и животных. В человеческих клетках отсутствует кэп Neu5Gc. Важность N-связанного гликозилирования становится все более очевидной в области фармацевтических препаратов. Хотя бактериальные или дрожжевые системы производства белка обладают значительными потенциальными преимуществами, такими как высокий выход и низкая стоимость, проблемы возникают, когда представляющий интерес белок представляет собой гликопротеин. Большинство прокариотических систем экспрессии, таких как E. coli не может выполнять посттрансляционные модификации. С другой стороны, эукариотические экспрессирующие хозяева, такие как клетки дрожжей и животных, имеют разные паттерны гликозилирования. Белки, продуцируемые в этих экспрессионных хозяевах, часто не идентичны человеческим белкам и, таким образом, вызывают иммуногенные реакции у пациентов. Например, S.cerevisiae (дрожжи) часто продуцируют гликаны с высоким содержанием маннозы, которые являются иммуногенными.
Экспрессионные системы млекопитающих, не относящиеся к человеку, такие как клетки CHO или NS0, имеют оборудование, необходимое для добавления сложных гликанов человеческого типа. Однако гликаны, продуцируемые в этих системах, могут отличаться от гликанов, продуцируемых в организме человека, поскольку они могут быть блокированы как N-гликолилнейраминовой кислотой (Neu5Gc), так и N-ацетилнейраминовой кислотой (Neu5Ac), тогда как клетки человека производят только гликопротеины, содержащие N-ацетилнейраминовую кислоту. Кроме того, животные клетки могут также продуцировать гликопротеины, содержащие эпитоп галактоза-альфа-1,3-галактоза, которые могут вызывать серьезные аллергические реакции, включая анафилактический шок, у людей с Аллергия на альфа-гал.
Эти недостатки были устранены с помощью нескольких подходов, таких как устранение путей, которые производят эти гликановые структуры, посредством генетического нокаута. Кроме того, с помощью генной инженерии были созданы другие системы экспрессии для производства терапевтических гликопротеинов с человеческими N-связанными гликанами. К ним относятся дрожжи, такие как Pichia pastoris, линии клеток насекомых, зеленые растения и даже бактерии.