| SMAD4 |
|---|
 |
|
| Идентификаторы |
|---|
| Псевдонимы | SMAD4, DPC4, JIP, MADH4, MYHRS, член семейства SMAD 4 |
| Внешние идентификаторы | OMIM : 600993 MGI : 894293 HomoloGene : 31310 GeneCard : SMAD4 |
|
| Расположение гена ( Мышь ) |
|---|
 | | Chr. | Хромосома 18 (мышь) |    | | Группа | 18 E2 | 18 49,51 см | Начинать | 73 639 009 б.п. | | Конец | 73 703 780 б.п. | |
|
| Онтология генов |
|---|
| Молекулярная функция | • белок гомодимеризация активность • белок гетеродимеризация активность • связывание РНК - полимеразы II, транскрипционный регул торный район последовательности специфических ДНК • ион металла связывания • ДНК связывания • GO: 0001131, GO: 0001151, GO: 0001130, GO: 0001204 ДНК-связывающий фактор активности транскрипции • Связывание ДНК, специфичное для последовательности • GO: 0001158, цис-регуляторной области Связывание ДНК, специфичное для последовательности • GO: 0001077, GO: 0001212, GO: 0001213, GO: 0001211, GO: 0001205, ДНК-связывающая активность активатора транскрипции, РНК-полимераза II-специфическая • I-СМАД связывание • коллаген связывание • GO: 0001948 связывание белка • ГО: 0000980 РНК - полимераза II цис-регуляторная область связывания последовательность специфических ДНК • R-СМАД связывание • связывания идентичных белковых • сульфата связывания • GO: 0001200, GO: 0001133, GO: 0001201 ДНК-связывающий фактор транскрипции, специфичность к РНК-полимеразе II • GO: 0001104 активность корегулятора транскрипции • регулятор молекулярных функций • связывание с хроматином | | Сотовый компонент | • ядро • цитоплазма • транскрипция регулятор комплекс • активин отзывчивого фактор комплекс • внутриклеточной анатомическая структура • РНК - полимераза II транскрипция регулятор комплекса • нуклеоплазма • центросома • цитозоль • SMAD белкового комплекс | | Биологический процесс | • негативная регуляция пролиферации клеточной популяции • сперматогенез • позитивная регуляция ограниченного путями фосфорилирования белка SMAD • позитивная регуляция секреции лютеинизирующего гормона • регуляция пролиферации клеточной популяции • развитие сердечной перегородки • негативная регуляция гибели клеток • регуляция развития волосяного фолликула • клеточная ответ на стимул BMP • переход эпителия в мезенхиму, участвующий в формировании эндокардиальной подушки • развитие ствола мозга • пролиферация клеточной популяции • регуляция связывания • сборка белкового комплекса SMAD • морфогенез метанефрической мезенхимы • позитивная регуляция перехода эпителия в мезенхиму • позитивная регуляция транскрипции с РНК-полимеразы II промотор участвует в клеточном ответе на химический стимул • регуляция транскрипции с помощью РНК-полимеразы II • ветвление участвует в морфогенезе зачатка мочеточника • регуляция транскрипции, ДНК-шаблон • морфогенез эмбрионального пальца • развитие матки пмент • управление аксонами • поддержание популяции соматических стволовых клеток • гаструляция • позитивная регуляция метилирования гистона H3-K4 • негативная регуляция транскрипции, ДНК-шаблон • ответ на трансформирующий фактор роста бета • активация эндотелиальных клеток • позитивная регуляция бета-рецептора трансформирующего фактора роста сигнальный путь • однократное оплодотворение • сигнальный путь бета-рецептора трансформирующего фактора роста • спецификация переднего / заднего паттернов • внутриутробное эмбриональное развитие • положительная регуляция пролиферации клеток, участвующих в морфогенезе сердечного клапана • формирование атриовентрикулярного клапана • внутриклеточная передача сигнала GO: 0007243 • рост в процессе развития • развитие энтодермы • клеточный гомеостаз ионов железа • развитие почек • формирование анатомической границы • позитивная регуляция ацетилирования гистона H3-K9 • регуляция продукции трансформирующего фактора роста бета2 • опосредованный интерлейкином-6 сигнальный путь • негативная регуляция транскрипции с помощью R NA-полимераза II • развитие мужских гонад • развитие фолликулов яичников • дифференцировка эндокардиальных клеток • нефрогенный морфогенез мезенхимы • гаструляция с формированием ротовой полости второй • развитие женских гонад • передача сигнала белка SMAD • ответ на гипоксию • развитие атриовентрикулярного канала • развитие мезодермы • негативная регуляция клеток рост • позитивная регуляция транскрипции, ДНК-шаблон • сигнальный путь BMP • тканевый морфогенез • позитивная регуляция транскрипции с помощью РНК-полимеразы II • позитивная регуляция передачи сигнала белка SMAD • спецификация ростральной / каудальной оси сомитов • развитие сальных желез • позитивная регуляция фолликула -стимулирующая секреция гормона • положительная регуляция сигнального пути BMP • дифференцировка клеток нервного гребня • развитие семенных канальцев • морфогенез женских гонад • регуляция сигнального пути рецептора трансформирующего фактора роста бета • обязательство судьбы нейрона • транскрипция, ДНК-матрица д • пути оттока перегородки морфогенез • левого желудочка морфогенез сердечной мышечной ткани • негативной регуляции сердечной гипертрофии мышц • белка deubiquitination • желудочковой перегородки морфогенез • отрицательное регулирование ERK1 и ERK2 каскада • отрицательное регулирование сердечной миофибрилле сборки • Белок homotrimerization • PRI-микроРНК транскрипции РНК-полимеразой II • вторичное развитие неба • морфогенез анатомической структуры • дифференцировка клеток • развитие мезэндодермы | | Источники: Amigo / QuickGO | |
| Ортологи |
|---|
| Разновидность | Человек | Мышь |
| Entrez | | |
| Ансамбль | | |
| UniProt | | |
| RefSeq (мРНК) | | |
| RefSeq (белок) | | |
| Расположение (UCSC) | Chr 18: 51.03 - 51.09 Мб | Chr 18: 73,64 - 73,7 Мб |
| PubMed поиск | | |
| Викиданные |
|
SMAD4, также называемый членом семейства SMAD 4, Матери против декапентаплегического гомолога 4, или DPC4 (удаленный при раке поджелудочной железы-4) является высококонсервативным белком, присутствующим у всех многоклеточных животных. Он принадлежит к семейству белков факторов транскрипции SMAD, которые действуют как медиаторы передачи сигнала TGF-β. TGF - beta семейства цитокинов регулирует важнейшие процессы в течение всего жизненного цикла многоклеточных, причем важную роль в процессе развития эмбриона, гомеостаза тканей, регенерации и иммунной регуляции.
SMAD 4 принадлежит к группе co-SMAD ( общий медиатор SMAD), второму классу семейства SMAD. SMAD4 - единственный известный co-SMAD у большинства многоклеточных животных. Он также принадлежит к семейству белков Дарвина, которые модулируют членов суперсемейства белков TGFβ, семейства белков, которые все играют роль в регуляции клеточных ответов. Млекопитающие SMAD4 является гомологом из Drosophila белка « Матери против decapentaplegic » по имени Медея.
SMAD4 взаимодействует с R-Smads, такими как SMAD2, SMAD3, SMAD1, SMAD5 и SMAD8 (также называемым SMAD9), с образованием гетеротримерных комплексов. Попадая в ядро, комплекс SMAD4 и двух R-SMADS связывается с ДНК и регулирует экспрессию различных генов в зависимости от клеточного контекста. Внутриклеточные реакции с участием SMAD4 запускаются связыванием на поверхности клеток факторов роста из семейства TGFβ. Последовательность внутриклеточных реакций с участием SMADS называется путем SMAD или путем трансформирующего фактора роста бета (TGF-β), поскольку последовательность начинается с распознавания TGF-β клетками.
СОДЕРЖАНИЕ
- 1 Джин
- 2 белка
- 3 конструкции
- 3.1 Комплексы домена MH1 с мотивами ДНК
- 3.2 Доменные комплексы MH2
- 4 Номенклатура и происхождение названия
- 5 Функция и механизм действия
- 6 Клиническое значение
- 7 ссылки
- 8 Дальнейшее чтение
- 9 Внешние ссылки
Ген
У млекопитающих SMAD4 кодируется геном, расположенным на 18 хромосоме. У человека ген SMAD4 содержит 54 829 пар оснований и расположен от пары № 51 030 212 до пары 51 085 041 в области 21.1 хромосомы 18.

Структура 18-й хромосомы у Homo sapiens. Ген SMAD 4 расположен на длинном плече хромосомы в локусе 21.1. Этот локус соответствует черной полосе между областями 12.3 и 21.2.
Протеин
SMAD4 представляет собой полипептид из 552 аминокислот с молекулярной массой 60,439 Да. SMAD4 имеет два функциональных домена, известных как MH1 и MH2.
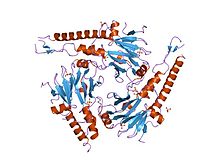
SMAD 4 состоит из трех основных доменов, включая MH1 (вверху), MH2 (вниз) и связывающий домен (справа).
Комплекс двух SMAD3 (или двух SMAD2) и одного SMAD4 связывается непосредственно с ДНК посредством взаимодействия их доменов MH1. Эти комплексы рекрутируются в сайты по всему геному факторами транскрипции, определяющими клеточный клон (LDTF), которые определяют контекстно-зависимую природу действия TGF-β. Раннее понимание специфичности связывания ДНК белков Smad было получено в результате скрининга связывания олигонуклеотидов, который идентифицировал палиндромный дуплекс 5'-GTCTAGAC-3 'как высокоаффинную связывающую последовательность для доменов SMAD3 и SMAD4 MH1. Другие мотивы также были идентифицированы в промоторах и энхансерах. Эти дополнительные сайты содержат мотив CAGCC и консенсусные последовательности GGC (GC) | (CG), последние также известны как сайты 5GC. Мотивы 5GC широко представлены в виде кластеров сайтов в SMAD-связанных областях по всему геному. Эти кластеры также могут содержать сайты CAG (AC) | (CC). Комплекс SMAD3 / SMAD4 также связывается с элементами промотора TPA-чувствительного гена, которые имеют мотив последовательности TGAGTCAG.
Структуры
Комплексы домена MH1 с мотивами ДНК
Первой структурой SMAD4, связанной с ДНК, был комплекс с палиндромным мотивом GTCTAGAC. Недавно также были определены структуры домена MH1 SMAD4, связанного с несколькими мотивами 5GC. Во всех комплексах взаимодействие с ДНК включает консервативную β-шпильку, присутствующую в домене MH1. Шпилька частично гибкая в растворе, а ее высокая степень конформационной гибкости позволяет распознавать различные последовательности из 5 п.н. Эффективные взаимодействия с GC-сайтами происходят только в том случае, если нуклеотид G расположен глубоко в большой рощице и устанавливает водородные связи с гуанидиниевой группой Arg81. Это взаимодействие способствует дополнительному поверхностному контакту между шпилькой, связывающей ДНК Smad, и большой бороздой ДНК. Другие прямые взаимодействия включают Lys88 и Gln83. Рентгеновская кристаллическая структура доменов Trichoplax adhaerens SMAD4 MH1, связанных с мотивом GGCGC, указывает на высокую сохранность этого взаимодействия у многоклеточных животных.

Домен MH1 Smad4, связанный с мотивом ДНК GGCT, из
PDB :
5MEZ

Увеличенное изображение домена Smad4 MH1, связанного с мотивом ДНК GGCGC, из
PDB :
5MEY

Домен MH1 Smad4, связанный с мотивом ДНК GGCGC, из
PDB :
5MEY
Доменные комплексы MH2
Домен MH2, соответствующий С-концу, отвечает за распознавание рецептора и ассоциацию с другими SMAD. Он взаимодействует с доменом MH2 R-SMADS и образует гетеродимеры и гетеротримеры. Некоторые опухолевые мутации, обнаруженные в SMAD4, усиливают взаимодействия между доменами MH1 и MH2.
Номенклатура и происхождение названия
SMAD являются высококонсервативными у разных видов, особенно в N-концевом домене MH1 и C-концевом домене MH2. Белки SMAD являются гомологами как белка MAD дрозофилы, так и белка SMA C. elegans. Название представляет собой комбинацию двух. Во время исследования дрозофилы было обнаружено, что мутация в гене MAD у матери репрессировала ген decapentaplegic в эмбрионе. Была добавлена фраза «Матери против», поскольку матери часто создают организации, выступающие против различных проблем, например, « Матери против вождения в нетрезвом виде» (MADD), что отражает «усиление материнского эффекта dpp »; и основан на традиции необычного именования в исследовательском сообществе. SMAD4 также известен как DPC4, JIP или MADH4.
Функция и механизм действия
SMAD4 - это белок, который определен как важный эффектор в пути SMAD. SMAD4 служит посредником между внеклеточными факторами роста из семейства TGFβ и генами внутри ядра клетки. Аббревиатура co в co-SMAD означает общий посредник. SMAD4 также определяется как преобразователь сигналов.
В пути TGF-β димеры TGF-β распознаются трансмембранным рецептором, известным как рецептор типа II. Как только рецептор типа II активируется связыванием TGF-β, он фосфорилирует рецептор типа I. Рецептор типа I также является рецептором клеточной поверхности. Затем этот рецептор фосфорилирует регулируемый внутриклеточным рецептором SMADS (R-SMADS), такой как SMAD2 или SMAD3. Затем фосфорилированный R-SMADS связывается с SMAD4. Ассоциация R-SMADs-SMAD4 представляет собой гетеромерный комплекс. Этот комплекс переместится из цитоплазмы в ядро: это транслокация. SMAD4 может образовывать гетеротримерные, гетерогексамерные или гетеродимерные комплексы с R-SMADS.
SMAD4 является субстратом киназы Erk / MAPK и GSK3. Стимуляция пути FGF ( фактора роста фибробластов ) приводит к фосфорилированию Smad4 с помощью Erk канонического сайта MAPK, расположенного на треонине 277. Это событие фосфорилирования оказывает двойное влияние на активность Smad4. Во-первых, он позволяет Smad4 достичь пика транскрипционной активности путем активации регулируемого фактором роста домена активации транскрипции, расположенного в линкерной области Smad4, SAD (Smad-Activation Domain). Во-вторых, MAPK праймирует Smad4 для GSK3- опосредованного фосфорилирования, которое вызывает ингибирование транскрипции, а также генерирует фосфодегрон, используемый в качестве места стыковки бета-трансдуцином, содержащим повторы убиквитина E3 ( бета-TrCP ), который полиубиквитинирует Smad4 и нацеливает его на деградацию в протеасоме.. Было высказано предположение, что фосфорилирование Smad4 GSK3 регулирует стабильность белка во время прогрессирования рака поджелудочной железы и толстой кишки.
В ядре гетеромерный комплекс связывает промоторы и взаимодействует с активаторами транскрипции. Комплексы SMAD3 / SMAD4 могут напрямую связывать SBE. Эти ассоциации слабые и требуют дополнительных факторов транскрипции, таких как члены семейства AP-1, TFE3 и FoxG1, для регулирования экспрессии генов.
Многие лиганды TGFβ используют этот путь, и впоследствии SMAD4 участвует во многих клеточных функциях, таких как дифференцировка, апоптоз, гаструляция, эмбриональное развитие и клеточный цикл.
Клиническое значение
Генетические эксперименты, такие как нокаут гена (KO), которые заключаются в модификации или инактивации гена, могут быть проведены для того, чтобы увидеть влияние дисфункционального SMAD 4 на исследуемый организм. Часто эксперименты проводят на домашней мыши ( Mus musculus ).
Было показано, что у мышей KO из SMAD4, в зернистых клетках, которые секретируют гормоны и факторы роста в течение ооцитов развития, подвергаются преждевременному лютеинизацию и выражать более низкие уровни фолликулостимулирующего гормона рецепторов (FSHR) и более высокие уровни лютеинизирующего гормона рецепторов (LHR). Это может быть частично связано с нарушением эффектов костного морфогенетического белка-7, поскольку BMP-7 использует сигнальный путь SMAD4.
Делеции в генах, кодирующих SMAD1 и SMAD5, также были связаны с метастазирующими опухолями гранулезных клеток у мышей.
SMAD4 часто мутирует при многих раковых заболеваниях. Мутация может быть унаследована или приобретена в течение жизни человека. В случае передачи по наследству мутация затрагивает как соматические клетки, так и клетки репродуктивных органов. Если мутация SMAD 4 приобретена, она будет существовать только в определенных соматических клетках. Действительно, SMAD 4 синтезируется не всеми клетками. Белок присутствует в клетках кожи, поджелудочной железы, толстой кишки, матки и эпителия. Он также продуцируется фибробластами. Функциональный SMAD 4 участвует в регуляции пути передачи сигнала TGF-β, который негативно регулирует рост эпителиальных клеток и внеклеточного матрикса (ECM). Когда структура SMAD 4 изменяется, экспрессия генов, участвующих в росте клеток, больше не регулируется, и пролиферация клеток может продолжаться без какого-либо подавления. Большое количество клеточных делений приводит к образованию опухолей, а затем к мультиплоидному колоректальному раку и карциноме поджелудочной железы. Он инактивирован как минимум в 50% случаев рака поджелудочной железы.
Было показано, что соматические мутации, обнаруженные при раке человека в домене MH1 SMAD 4, ингибируют ДНК-связывающую функцию этого домена.
СМАД 4 также обнаружили, мутировали в аутосомно - доминантным заболеванием синдром ювенильного полипоза (JPS). JPS характеризуется наличием гамартоматозных полипов желудочно-кишечного тракта. Эти полипы обычно доброкачественные, однако они подвержены большему риску развития рака желудочно-кишечного тракта, в частности рака толстой кишки. Идентифицировано около 60 мутаций, вызывающих JPS. Они были связаны с производством SMAD 4 меньшего размера с отсутствующими доменами, которые препятствуют связыванию белка с R-SMADS и образованию гетеромерных комплексов.
Мутации в SMAD4 (в основном замены) могут вызывать синдром Мюре, редкое наследственное заболевание, характеризующееся умственными недостатками, низким ростом, необычными чертами лица и различными костными аномалиями.
использованная литература
дальнейшее чтение
- Миязоно К. (2000). «Передача сигналов TGF-бета белками Smad». Обзоры цитокинов и факторов роста. 11 (1–2): 15–22. DOI : 10.1016 / S1359-6101 (99) 00025-8. PMID 10708949.
- Врана Дж. Л., Аттисано Л. (2000). «Путь Смада». Обзоры цитокинов и факторов роста. 11 (1–2): 5–13. DOI : 10.1016 / S1359-6101 (99) 00024-6. PMID 10708948.
- Verschueren K, Huylebroeck D (2000). «Замечательная универсальность белков Smad в ядре клеток, активированных трансформирующим фактором роста бета». Обзоры цитокинов и факторов роста. 10 (3–4): 187–99. DOI : 10.1016 / S1359-6101 (99) 00012-X. PMID 10647776.
- Massagué J (1998). «Передача сигнала TGF-бета». Ежегодный обзор биохимии. 67: 753–91. DOI : 10.1146 / annurev.biochem.67.1.753. PMID 9759503.
- Klein-Scory S, Zapatka M, Eilert-Micus C, Hoppe S, Schwarz E, Schmiegel W, Hahn SA, Schwarte-Waldhoff I (2008). «Высокий уровень индуцируемой реэкспрессии Smad4 в линии клеток рака шейки матки C4-II связан с профилем экспрессии гена, который предсказывает предпочтительную роль Smad4 в составе внеклеточного матрикса». BMC Рак. 7: 209. DOI : 10.1186 / 1471-2407-7-209. PMC 2186346. PMID 17997817.
- Kalo E, Buganim Y, Shapira KE, Besserglick H, Goldfinger N, Weisz L, Stambolsky P, Henis YI, Rotter V (декабрь 2007 г.). «Мутантный p53 ослабляет SMAD-зависимый путь передачи сигнала трансформирующего фактора роста бета1 (TGF-beta1) путем репрессии экспрессии рецептора TGF-бета типа II». Молекулярная и клеточная биология. 27 (23): 8228–42. DOI : 10.1128 / MCB.00374-07. PMC 2169171. PMID 17875924.
- Aretz S, Stienen D, Uhlhaas S, Stolte M, Entius MM, Loff S, Back W, Kaufmann A, Keller KM, Blaas SH, Siebert R, Vogt S, Spranger S, Holinski-Feder E, Sunde L, Propping P, Фридл В. (ноябрь 2007 г.). «Высокая доля крупных геномных делеций и обновление фенотипа генотипа в 80 неродственных семьях с синдромом ювенильного полипоза». Журнал медицинской генетики. 44 (11): 702–9. DOI : 10.1136 / jmg.2007.052506. PMC 2752176. PMID 17873119.
- Али С., Коэн С., Литтл СП, Секейра Дж. Х., Мосунжак МБ, Сиддики М.Т. (октябрь 2007 г.). «Применение SMAD4 в качестве диагностического иммуногистохимического маркера аденокарциномы поджелудочной железы и его экспрессия в других солидных опухолях». Диагностическая цитопатология. 35 (10): 644–8. DOI : 10.1002 / dc.20715. PMID 17854080. S2CID 36682992.
- Милет Дж, Дехаис В., Бургейн С., Жуаноль А.М., Моссер А., Перрин М., Морсет Дж., Бриссо П., Дэвид В., Дюнье Ю., Моссер Дж. (Октябрь 2007 г.). «Общие варианты генов BMP2, BMP4 и HJV пути регуляции гепсидина модулируют пенетрантность гемохроматоза HFE». Американский журнал генетики человека. 81 (4): 799–807. DOI : 10.1086 / 520001. PMC 2227929. PMID 17847004.
- Салек С., Бенесова Л., Заворал М., Носек В., Касперова Л., Рыска М., Стрнад Р., Трабулси Е., Минарик М. (июль 2007 г.). «Оценка клинической значимости исследования мутаций K-ras, p16 и p53 вместе с аллельными потерями на 9p и 18q в образцах тонкой иглы под контролем EUS у пациентов с хроническим панкреатитом и раком поджелудочной железы». Всемирный журнал гастроэнтерологии. 13 (27): 3714–20. DOI : 10,3748 / wjg.v13.i27.3714. PMC 4250643. PMID 17659731.
- Себастьен А., Хайду М., Кис Л., Барна Г., Коппер Л. (сентябрь 2007 г.). «Smad4-независимый, PP2A-зависимый апоптотический эффект экзогенного трансформирующего фактора роста бета 1 в клетках лимфомы». Экспериментальные исследования клеток. 313 (15): 3167–74. DOI : 10.1016 / j.yexcr.2007.05.028. PMID 17643425.
- Мартин М.М., Бакенбергер Дж. А., Цзян Дж., Малана Г. Э., Ноелл Д. Л., Фельдман Д. С., Элтон Т. С. (сентябрь 2007 г.). «TGF-beta1 стимулирует экспрессию человеческого рецептора AT1 в фибробластах легких посредством перекрестной связи между сигнальными путями Smad, p38 MAPK, JNK и PI3K». Американский журнал физиологии. Клеточная и молекулярная физиология легких. 293 (3): L790–9. DOI : 10,1152 / ajplung.00099.2007. PMC 2413071. PMID 17601799.
- Леви Л., Хауэлл М., Дас Д., Харкин С., Эпископу В., Хилл С.С. (сентябрь 2007 г.). «Аркадия активирует Smad3 / Smad4-зависимую транскрипцию, запуская индуцированную сигналом деградацию SnoN». Молекулярная и клеточная биология. 27 (17): 6068–83. DOI : 10.1128 / MCB.00664-07. PMC 1952 153. PMID 17591695.
- Grijelmo C, Rodrigue C, Svrcek M, Bruyneel E, Hendrix A, de Wever O, Gespach C (август 2007 г.). «Проинвазивная активность BMP-7 через SMAD4 / src-независимые и ERK / Rac / JNK-зависимые сигнальные пути в раковых клетках толстой кишки». Сотовая сигнализация. 19 (8): 1722–32. DOI : 10.1016 / j.cellsig.2007.03.008. PMID 17478078.
- Сонегава Х., Нукуи Т., Ли Д.В., Такаиси М., Сакагути М., Хах Нью-Хэмпшир (июль 2007 г.). «Участие ухудшения S100C / A11-опосредованного пути в устойчивости линий клеток плоскоклеточного рака человека к подавлению роста, индуцированному TGFbeta». Журнал молекулярной медицины. 85 (7): 753–62. DOI : 10.1007 / s00109-007-0180-7. PMID 17476473. S2CID 15667203.
- Шейх А.А., Вималачандран Д., Томпсон С.К., Дженкинс Р.Э., Неджади Т., Шекоу А., Кэмпбелл Ф., Додсон А., Прайм В., Црногорак-Юрчевич Т., Лемуан Н.Р., Костелло Е. (июнь 2007 г.). «Экспрессия S100A8 в моноцитах, связанных с раком поджелудочной железы, связана со статусом Smad4 раковых клеток поджелудочной железы». Протеомика. 7 (11): 1929–40. DOI : 10.1002 / pmic.200700072. PMID 17469085. S2CID 35648264.
- Попович Хадзия М., Королия М., Якич Разумович Дж., Павкович П., Хадзия М., Капитанович С. (апрель 2007 г.). «Мутации K-ras и Dpc4 при хроническом панкреатите: серия случаев». Хорватский медицинский журнал. 48 (2): 218–24. PMC 2080529. PMID 17436386.
- Лози Л., Бузурен Х., Бенхаттар Дж. (Май 2007 г.). «Потеря экспрессии Smad4 предсказывает метастазирование в печень при колоректальном раке человека». Отчеты онкологии. 17 (5): 1095–9. doi : 10.3892 / или 17.5.1095. PMID 17390050.
- Карлссон Г., Бланк Ю., Муди Дж. Л., Эхингер М., Сингбрант С., Дэн С. Х., Карлссон С. (март 2007 г.). «Smad4 имеет решающее значение для самообновления гемопоэтических стволовых клеток». Журнал экспериментальной медицины. 204 (3): 467–74. DOI : 10,1084 / jem.20060465. PMC 2137898. PMID 17353364.
- Такано С., Канаи Ф., Джазаг А., Иджичи Х., Яо Дж., Огава Х., Эномото Н., Омата М., Накао А. (март 2007 г.). «Smad4 необходим для подавления E-кадгерина, индуцированного TGF-бета, в линии клеток рака поджелудочной железы PANC-1». Журнал биохимии. 141 (3): 345–51. DOI : 10.1093 / Jb / mvm039. PMID 17301079.
внешние ссылки
 Структура 18-й хромосомы у Homo sapiens. Ген SMAD 4 расположен на длинном плече хромосомы в локусе 21.1. Этот локус соответствует черной полосе между областями 12.3 и 21.2.
Структура 18-й хромосомы у Homo sapiens. Ген SMAD 4 расположен на длинном плече хромосомы в локусе 21.1. Этот локус соответствует черной полосе между областями 12.3 и 21.2.  SMAD 4 состоит из трех основных доменов, включая MH1 (вверху), MH2 (вниз) и связывающий домен (справа).
SMAD 4 состоит из трех основных доменов, включая MH1 (вверху), MH2 (вниз) и связывающий домен (справа).  Домен MH1 Smad4, связанный с мотивом ДНК GGCT, из PDB : 5MEZ
Домен MH1 Smad4, связанный с мотивом ДНК GGCT, из PDB : 5MEZ  Увеличенное изображение домена Smad4 MH1, связанного с мотивом ДНК GGCGC, из PDB : 5MEY
Увеличенное изображение домена Smad4 MH1, связанного с мотивом ДНК GGCGC, из PDB : 5MEY  Домен MH1 Smad4, связанный с мотивом ДНК GGCGC, из PDB : 5MEY
Домен MH1 Smad4, связанный с мотивом ДНК GGCGC, из PDB : 5MEY