 | |
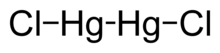 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Димеркурия дихлорид | |
| Другие имена Хлорид ртути (I) Хлорид ртути Каломель | |
| Идентификаторы | |
| Количество CAS | |
| 3D модель ( JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.030.266 |
| Номер ЕС | |
| PubChem CID | |
| Номер RTECS | |
| UNII | |
| Номер ООН | 3077 |
| Панель управления CompTox ( EPA) | |
ИнЧИ
| |
Улыбки
| |
| Характеристики | |
| Химическая формула | Hg 2 Cl 2 |
| Молярная масса | 472,09 г / моль |
| Появление | Белое твердое вещество |
| Плотность | 7,150 г / см 3 |
| Температура плавления | 383 ° С (721 ° F, 656 К) (сублимированные) |
| Растворимость в воде | 0,2 мг / 100 мл |
| Произведение растворимости ( K уд) | 1,43 × 10 −18 |
| Растворимость | не растворим в этаноле, эфире |
| Магнитная восприимчивость (χ) | −26,0 10 −6 см 3 / моль |
| Показатель преломления ( n D) | 1,973 |
| Опасности | |
| Паспорт безопасности | ICSC 0984 |
| Классификация ЕС (DSD) (устаревшая) | Токсично ( T) Вредно ( Xn) Опасно для окружающей среды ( N) |
| R-фразы (устаревшие) | R22, R36 / 37/38, R50 / 53 |
| S-фразы (устаревшие) | (S2), S13, S24 / 25, S46, S60, S61 |
| NFPA 704 (огненный алмаз) |  3 0 0 3 0 0 |
| точка возгорания | Не воспламеняется |
| Смертельная доза или концентрация (LD, LC): | |
| LD 50 ( средняя доза ) | 210 мг / кг (крыса, перорально) |
| Термохимия | |
| Стандартная мольная энтропия ( S | 196 Дж моль −1 K −1 |
| Std энтальпия формации (Δ F H ⦵298) | −265 кДж моль −1 |
| Родственные соединения | |
| Другие анионы | Фторид ртути (I) Бромид ртути (I) Йодид ртути (I) |
| Родственные соединения | Хлорид ртути (II) |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| | |
| Ссылки на инфобоксы | |
Хлорид ртути (I) представляет собой химическое соединение с формулой Hg 2 Cl 2. Это плотное белое или желтовато-белое твердое вещество без запаха, также известное как минеральная каломель (редкий минерал) или хлорид ртути, является основным примером соединения ртути (I). Это компонент электродов сравнения в электрохимии.
Считается, что название каломель происходит от греческого καλός красивый и μέλας черный ; или καλός и μέλι мед из-за его сладкого вкуса. Черное имя (несколько удивительны для белого соединения), вероятно, из - за его характерную диспропорционированию реакция с аммиаком, который дает «захватывающую» черную окраску из - за мелкодисперсной металлическую ртуть образуется. Его также называют минеральной ртутью или ртутью.
Каломель принимали внутрь и использовали как слабительное, например, для лечения Георга III в 1801 году, и дезинфицирующее средство, а также при лечении сифилиса до начала 20 века. До недавнего времени он также использовался в качестве фунгицида для садоводства, в первую очередь, как средство для окунания корней, чтобы предотвратить появление кайлы среди культур семейства Brassicaceae.
В эпоху « героической медицины » ртуть стала популярным средством от множества физических и психических недугов. Его использовали врачи в Америке на протяжении 18 века и во время революции, чтобы заставить пациентов срыгивать и освободить свое тело от «нечистот». Бенджамин Раш был одним из самых известных защитников ртути в медицине и использовал каломель для лечения больных желтой лихорадкой во время ее вспышки в Филадельфии в 1793 году. Каломель давали пациентам как слабительное или слабительное до тех пор, пока у них не началось слюноотделение, и часто его вводили. пациентов в таком большом количестве, что у них выпадали волосы и зубы.
Вскоре после того, как желтая лихорадка поразила Филадельфию, болезнь разразилась на Ямайке. В прессе разразилась война слов о лучшем лечении желтой лихорадки: кровотечении; или каломель. Неофициальные данные свидетельствуют о том, что каломель была более эффективной, чем кровотечение.
Старший брат мормонского пророка Джозефа Смита Элвин Смит умер в 1823 году от отравления ртутью из каломели.
Льюис и Кларк принесли с собой чудо-лекарство того времени, хлорид ртути (также известный как каломель) в виде пилюли, настойки и мази. Современные исследователи использовали ту же самую ртуть, найденную глубоко в выгребных ямах, чтобы проследить местоположение их соответствующих местоположений и кемпингов.
Ртуть является уникальной среди металлов группы 12 благодаря своей способности так легко образовывать связь M – M. Hg 2 Cl 2 представляет собой линейную молекулу. Минеральная каломель кристаллизуется в тетрагональной системе с пространственной группой I4 / м 2 / м 2 / м. Элементарная ячейка от кристаллической структуры показана ниже:
 | 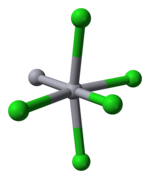 |
| ячейка | искаженная октаэдрическая координация Hg |
Длина связи Hg – Hg составляет 253 пм (Hg – Hg в металле составляет 300 пм), а длина связи Hg – Cl в линейном звене Hg 2 Cl 2 составляет 243 пм. Общая координация каждого атома Hg октаэдрическая, поскольку, помимо двух ближайших соседей, есть еще четыре атома Cl в 321 пм. Существуют более длинные поликатионы ртути.
Хлорид ртути образуется при реакции элементарной ртути и хлорида ртути:
Его можно получить с помощью реакции метатезиса с участием водного нитрата ртути (I) с использованием различных источников хлорида, включая NaCl или HCl.
Аммиак приводит к непропорциональности Hg 2 Cl 2:
Хлорид ртути широко используется в электрохимии, благодаря легкости его реакций окисления и восстановления. Каломельный электрод является электродом сравнения, особенно в более старых публикациях. За последние 50 лет на смену ему пришел электрод серебро / хлорид серебра (Ag / AgCl). Хотя от ртутных электродов повсеместно отказались из-за опасной природы ртути, многие химики считают, что они по-прежнему более точны и не опасны при правильном обращении. Различия экспериментальных потенциалов мало отличаются от литературных значений. Другие электроды могут варьироваться от 70 до 100 милливольт.
Хлорид ртути разлагается на хлорид ртути (II) и элементарную ртуть под воздействием УФ-излучения.
Образование Hg можно использовать для расчета количества фотонов в световом пучке методом актинометрии.
Используя легкую реакцию в присутствии хлорида ртути (II) и оксалата аммония, получают хлорид ртути (I), хлорид аммония и диоксид углерода.
Эта конкретная реакция была открыта Дж. М. Эдером (отсюда и название реакция Эдера) в 1880 году и повторно исследована У. Эйдером в 1929 году.
Бромид ртути (I), Hg 2 Br 2, имеет светло-желтый цвет, тогда как йодид ртути (I), Hg 2 I 2, имеет зеленоватый цвет. Оба плохо растворимы. Фторид ртути (I) нестабилен в отсутствие сильной кислоты.
Хлорид ртути токсичен, хотя из-за его низкой растворимости в воде он обычно менее опасен, чем его аналог хлорида ртути. Он использовался в медицине как мочегонное и слабительное (слабительное) средство в Соединенных Штатах с конца 1700-х до 1860-х годов. Каломель также был обычным ингредиентом порошков для прорезывания зубов в Великобритании вплоть до 1954 года, вызывая широко распространенное отравление ртутью в виде розовой болезни, смертность от которой в то время составляла 1 из 10. Эти медицинские применения были позже прекращены, когда токсичность соединения снизилась. обнаруженный.
Он также нашел применение в косметике в качестве мыла и кремов для осветления кожи, но эти препараты в настоящее время запрещены для производства или импорта во многих странах, включая США, Канаду, Японию и Европейский Союз. Исследование рабочих, участвовавших в производстве этих препаратов, показало, что натриевая соль 2,3-димеркапто-1-пропансульфоновой кислоты (DMPS) эффективна в снижении содержания ртути в организме и в снижении концентрации ртути в моче до нормального уровня.