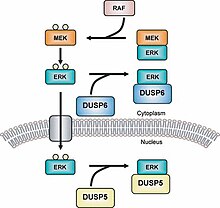
 На рисунке показано взаимодействие и кооперация MEK, DUSP5 и DUSP6 / MKP-3 в цитоплазматической области и ядре. РАФ активирует МЕК. Активированный MEK фосфорилирует ERK, который теперь может транспортироваться через клеточную мембрану с помощью транспортера. Дефосфорилированная ERK не может покинуть ядро.
На рисунке показано взаимодействие и кооперация MEK, DUSP5 и DUSP6 / MKP-3 в цитоплазматической области и ядре. РАФ активирует МЕК. Активированный MEK фосфорилирует ERK, который теперь может транспортироваться через клеточную мембрану с помощью транспортера. Дефосфорилированная ERK не может покинуть ядро. Фосфатазы MAPK (MKP) представляют собой самый большой класс фосфатаз, участвующих в подавлении передачи сигналов митоген-активируемых протеинкиназ (MAPK). Сигнальные пути MAPK регулируют множество характеристик развития и гомеостаза. Это может включать регуляцию генов, пролиферацию клеток, запрограммированную гибель клеток и стрессовые реакции. Таким образом, фосфатазы MAPK являются важными регуляторами этих путей.
 Когда активированный MAPK связывается с MKB, это вызывает конформационное изменение области DUSP, которое активирует MKP, а активированный MKP дефосфорилирует MAPK, тем самым инактивируя его.
Когда активированный MAPK связывается с MKB, это вызывает конформационное изменение области DUSP, которое активирует MKP, а активированный MKP дефосфорилирует MAPK, тем самым инактивируя его. Фосфатазы MAPK обнаруживаются только у эукариот и отрицательно регулируют киназы MAP, действуя как отрицательная обратная связь. MKPs также известен как двойная специфичность фосфатаз (DUSPs), потому что они дезактивируют MAPK с помощью dephosphorylating в Треонине и тирозин остатков проживающих в МАРК участке активации. MKP имеют каталитическую область на своем С-конце и регуляторную область на своем N-конце. Положение, где MAPK связывается с MKP, находится рядом с N-концом MKP. Связывание происходит из-за электростатических взаимодействий положительно заряженных остатков на участке связывания MKP с отрицательно заряженными остатками на участке связывания MAPK.
Существует 10 основных MKP, которые можно далее разбить на три подкласса, которые представляют либо их геномную структуру, либо тип субстрата (MAPK), с которым они связываются. К ним относятся DUSP1, DUSP2, DUSP4 и DUSP5, которые принадлежат к подгруппе 1. DUSP6, DUSP7, DUSP9 и DUSP10 относятся к подгруппе 2. DUSP8 и DUSP16 принадлежат к подгруппе 3, эти подгруппы основаны на геномной структуре MKP. Новейший MKP-8 доводит общее количество MKP до 11, MKP-8 играет роль в ингибировании киназы p38.
Фосфатазы двойной специфичности (DUSP) также принадлежат к семейству протеинтирозинфосфатаз. MKP подразделяются на типы I, II и III; в которых MKP типа I расположены в ядерной области, тип II - в цитоплазматической области, а тип III - как в ядерной, так и в цитоплазматической области. Различное расположение этих трех типов MKP позволяет им вызывать разные типы сигнализации. Например, MKP-1 (тип I MKP) контролирует экспрессию гена путем инактивации субклеточной группы MAPK. Обратите внимание, что без мотива LXXLL (GFP-MKP-1 47-367) MKP-1 не может локализоваться внутри ядра и находится перед доменом CH2A. Новейший MKP, MKP-8, принадлежит к группе I, потому что он расположен в ядерной области клетки. Недавнее исследование показывает, что изоформы гистондеацетилазы (HDAC1, -2 и -3) деацетилируют MKP-1 и что это пост- трансляционная модификация увеличивает передачу сигналов MAPK и врожденного иммунитета.
Хотя N-концевой участок является совершенно отличным для каждого MKP, все они обычно содержат домены CH2. В MKP-1 MAPK связывается с активным сайтом, который находится между доменами CH2A и CHB, расположенными на N-конце.
Примером MKP типа II является MKP-3, который регулирует активность ERK2, депонируя его и удерживая в цитоплазматической области. MKP-3 также связывается с ERK2 независимо от того, фосфорилирован он или нет. MKP-4 - это еще один MKP, который принадлежит к типу I и отличается от других MKP в этой подгруппе, поскольку он обнаруживается только в клетках плаценты, почек и эмбриональной печени. MKP-5 представляет собой MKP типа III, который специфически связывается с p38 и SPK / JNK и обнаруживается как в цитоплазматической, так и в ядерной областях клетки. MKP-5 находится только в клетках сердца, легких, печени, почек и скелетных мышц. Есть также MKP, которые принадлежат к группе под названием Atypical MKP. Например, Vaccina H1-related (VHR) является атипичным MKP, потому что он имеет только область DUSP. VHR обнаруживается только в лимфоидных и гемопоэтических клетках и инактивирует ERK1 / 2 и JNK в рецепторах Т-клеток. VHR также вызывает остановку клеточного цикла.
| Имя | Альт. название | Подгруппа |
|---|---|---|
| DUSP1 | МКП-1 | я |
| DUSP2 | я | |
| DUSP4 | МКП-2 | я |
| DUSP5 | я | |
| DUSP6 | МКП-3 | II |
| DUSP7 | II | |
| DUSP8 | III | |
| DUSP9 | МКП-4 | II |
| DUSP10 | МКП-5 | ? |
| DUSP14 | МКП-6 | ? |
| DUSP16 | МКП-7 | III |
| DUSP26 | МКП-8 | я |