 | |
 | |
 | |
| Имена | |
|---|---|
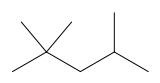
| Предпочтительное название IUPAC 2,2,4-триметилпентан | |
| Идентификаторы | |
| Количество CAS | |
| 3D модель ( JSmol ) | |
| Ссылка на Beilstein | 1696876 |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.007.964 |
| Номер ЕС | |
| MeSH | 2,2,4-триметилпентан |
| PubChem CID | |
| Номер RTECS | |
| UNII | |
| Номер ООН | 1262 |
| Панель управления CompTox ( EPA) | |
ИнЧИ
| |
Улыбки
| |
| Характеристики | |
| Химическая формула | С 8 Н 18 |
| Молярная масса | 114,232 г моль -1 |
| Появление | Бесцветная жидкость |
| Запах | нефтяной |
| Плотность | 0,692 г см −3 |
| Температура плавления | -107,38 ° С; -161,28 ° F; 165,77 К |
| Точка кипения | 99,30 ° С; 210,74 ° F; 372,45 К |
| журнал P | 4,373 |
| Давление газа | 5,5 кПа (при 21 ° C) |
| Константа закона Генри ( k H ) | 3,0 нмоль Па -1 кг -1 |
| УФ-видимый (λ макс. ) | 210 нм |
| Магнитная восприимчивость (χ) | -98,34 10 −6 см 3 / моль |
| Показатель преломления ( n D ) | 1,391 |
| Термохимия | |
| Теплоемкость ( C ) | 242,49 Дж -1 моль -1 |
| Стандартная мольная энтропия ( S | 328,03 Дж -1 моль -1 |
| Std энтальпия формации (Δ F H ⦵ 298 ) | От −260,6 до −258,0 кДж моль −1 |
| Std энтальпии сгорания (Δ с Н ⦵ 298 ) | От -5462,6 до -5460,0 кДж моль -1 |
| Опасности | |
| Пиктограммы GHS |     |
| Сигнальное слово GHS | Опасность |
| Положения об опасности GHS | H225, H304, H315, H336, H410 |
| Меры предосторожности GHS | P210, P261, P273, P301 + 310, P331 |
| NFPA 704 (огненный алмаз) |  1 3 0 1 3 0 |
| точка возгорания | -12 ° С (10 ° F, 261 К) |
| самовоспламенения температуру | 396 ° С (745 ° F, 669 К) |
| Пределы взрываемости | 1,1–6,0% |
| Родственные соединения | |
| Родственные алканы | |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| | |
| Ссылки на инфобоксы | |
2,2,4-триметилпентан, также известный как изооктан или изооктана, представляет собой органическое соединение с формулой (СН 3 ) 3 ССН 2 СН (СН 3 ) 2. Это один из нескольких изомеров из октана (С 8 Н 18 ). Этот конкретный изомер является стандартным 100 баллом по шкале октанового числа (нулевая точка - н- гептан ). Это важный компонент бензина, который часто используется в относительно больших количествах для повышения детонационной стойкости топлива.
Строго говоря, если следовать стандартному значению «изо», название изооктан следует зарезервировать для изомера 2-метилгептана. Однако 2,2,4-триметилпентан на сегодняшний день является наиболее важным изомером октана, и поэтому исторически ему было присвоено это название.
Изооктан производится в массовом масштабе в нефтяной промышленности путем алкилирования изобутана с изобутана. Процесс проводят в установках алкилирования в присутствии кислотных катализаторов.
 Переход к 2,2,4-триметилпентану из изобутена и изобутана
Переход к 2,2,4-триметилпентану из изобутена и изобутана Он также может быть получен из изобутилена путем димеризации с использованием Amberlyst катализатора с получением смеси изо-октены. Гидрирование этой смеси дает 2,2,4-триметилпентан.
Детонация двигателя - это нежелательный процесс, который может происходить при высоких степенях сжатия в двигателях внутреннего сгорания. Грэм Эдгар в 1926 году добавил к бензину различные количества н- гептана и 2,2,4-триметилпентана и обнаружил, что детонация прекращается при добавлении 2,2,4-триметилпентана. Эта работа положила начало шкале октанового числа. Испытательные двигатели с использованием 2,2,4-триметилпентана дали определенную производительность, которая была стандартизирована для октанового числа 100. Те же тестовые двигатели, работающие таким же образом, с использованием гептана, дали производительность, которая была стандартизирована как нулевое октановое число. Затем все остальные соединения и смеси соединений были оценены по этим двум стандартам и им присвоено октановое число.
Как и все углеводороды, 2,2,4-триметилпентан легко воспламеняется.