 . Структура безводного хлорида железа (Fe, Cl) . Структура безводного хлорида железа (Fe, Cl) | |||
| |||
| Названия | |||
|---|---|---|---|
| Названия IUPAC Хлорид железа (II). Дихлорид железа | |||
| Другие названия Хлорид железа. Рокюнит | |||
| Идентификаторы | |||
| Номер CAS |
| ||
| 3D-модель (JSmol ) | |||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard | 10 0,028.949 | ||
| Номер EC |
| ||
| PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Панель управления CompTox (EPA ) | |||
InChI
| |||
SMILES
| |||
| Свойства | |||
| Химическая формула | FeCl 2 | ||
| Молярная масса | 126,751 г / моль (безводный). 198,8102 г / моль (тетрагидрат) | ||
| Внешний вид | Желтовато-коричневое твердое вещество (безводное). Бледно-зеленое твердое вещество (дитетрагидрат) | ||
| Плотность | 3,16 г / см (безводный). 2,39 г / см (дигидрат). 1,93 г / см (тетрагидрат) | ||
| Температура плавления | 677 ° C (1251 ° F; 950 K) (безводный). 120 ° C (дигидрат). 105 ° C (тетрагидрат) | ||
| Точка кипения | 1023 ° C (1873 ° F; 1296 K) (безводный) | ||
| Растворимость в воде | 64,4 г / 100 мл (10 ° C),. 68,5 г / 100 мл (20 ° C),. 105,7 г / 100 мл (100 ° C) | ||
| Растворимость в ТГФ | Растворимый | ||
| log P | -0,15 | ||
| Магнитная восприимчивость (χ) | + 14750 · 10 см / моль | ||
| Структура | |||
| Кристаллическая структура | Моноклинная | ||
| Координационная геометрия | Октаэдрическая при Fe | ||
| Фармакология | |||
| Код ATC | B03AA05 (ВОЗ ) | ||
| Опасности | |||
| Паспорт безопасности | Железо ( II) хлорид MSDS | ||
| NFPA 704 (огненный алмаз) |  0 3 0 0 3 0 | ||
| NIOSH (пределы воздействия на здоровье США): | |||
| REL (рекомендуется) | TWA 1 мг / м | ||
| Родственные соединения | |||
| Другие анионы | Фторид железа (II). Бромид железа (II). Иодид железа (II) | ||
| Прочие катионы | Хлорид кобальта (II). Хлорид марганца (II). Хлорид меди (II) | ||
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на ink | |||
Хлорид железа (II), также известное как хлорид железа, представляет собой химическое соединение формулы FeCl 2. Это парамагнитное твердое вещество с высокой температурой плавления. Состав белый, но типичные образцы часто не совсем белые. FeCl 2кристаллизуется из воды в виде зеленоватого тетрагидрата, который является формой, которая наиболее часто встречается в торговле и лабораториях. Также есть дигидрат. Соединение хорошо растворяется в воде, давая бледно-зеленые растворы.
 Структура «FeCl 2 (thf) x », Fe 4Cl8(thf) 6, иллюстрирующие как тетраэдрическую, так и октаэдрическую координационные геометрии.
Структура «FeCl 2 (thf) x », Fe 4Cl8(thf) 6, иллюстрирующие как тетраэдрическую, так и октаэдрическую координационные геометрии. Гидратированные формы Хлорид железа образуется при обработке отходов производства стали с помощью соляной кислоты. Такие растворы называют «отработанной кислотой» или «травильным раствором», особенно когда соляная кислота не полностью израсходована:
Отработанная кислота требует обработки если он утилизируется. Хлорид железа используется при производстве хлорида железа. Хлорид железа также можно использовать для регенерации соляной кислоты. Это также побочный продукт производства титана, так как некоторые титановые руды содержат железо.
Хлорид железа получают путем добавления порошка железа к раствору соляной кислоты. кислота в метаноле. Эта реакция дает метанольный сольват дихлорида, который при нагревании в вакууме примерно при 160 ° C превращается в безводный FeCl 2. Показана результирующая реакция:
FeBr 2 и FeI 2 могут быть получены аналогично.
Альтернативный синтез безводного хлорида железа - это восстановление FeCl 3 с помощью хлорбензола :
В одном из двух классических синтезов ферроцена, Уилкинсон генерировал FeCl 2 in situ путем компропорционирования FeCl 3 с порошком железа в ТГФ. Хлорид железа разлагается до хлорида железа при высоких температурах.
Дигидрат FeCl 2(H2O)2кристаллизуется из концентрированной соляной кислоты. Дигидрат представляет собой координационный полимер . Каждый Fe-центр координирован с четырьмя дважды мостиковыми хлоридными лигандами. Октаэдр завершается парой взаимно транс акволигандов.
 Субъединица решетки FeCl 2(H2O)2.
Субъединица решетки FeCl 2(H2O)2. 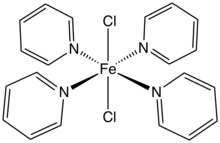 Тетра (пиридин) дихлорид железа получают обработкой хлорида железа пиридин.
Тетра (пиридин) дихлорид железа получают обработкой хлорида железа пиридин.FeCl 2 и его гидраты образуют комплексы со многими лигандами. Например, растворы гидратов реагируют с двумя молярными эквивалентами [(C 2H5)4N] Cl с образованием соли [(C 2H5)4N]2[FeCl 4].
Безводный FeCl 2, который растворим в тетрагидрофуране (THF), является стандартным предшественником в металлоорганическом синтезе. FeCl 2 используется для создания комплексов NHC in situ для реакции перекрестного сочетания.
В отличие от родственных сульфата железа и хлорида железа, хлорид железа имеет несколько коммерческих применений. Помимо использования в лаборатории При синтезе комплексов железа хлорид железа служит коагулятором и флокулянтом агентом при очистке сточных вод, особенно для отходов, содержащих хромат или сульфиды. Используется для контроля запаха при очистке сточных вод. Он используется в качестве прекурсора для производства различных сортов гематита, который может использоваться в различных пигментах. Он является прекурсором гидратированных оксидов железа (III), которые являются магнитными пигментами. FeCl 2 находит нас e в качестве реагента в органическом синтезе.