Кван механика - это наука о очень малых. Он объясняет поведение материи и ее поведение с энергией на шкале атомных и субатомных частиц. Напротив, классическая физика объясняет материю и энергию только в масштабе, знакомом человеческому опыту, включая поведение астрономических тел, таких как Луна. Классическая физика до сих пор используется в большей части современной науки и техники. Однако ближе к концу XIX века ученые открывают явления как в большом (макро ), так и в маленьком (микро ) мирах, которые классическая физика не объяснить. Стремление разрешить наблюдаемых и классических теорией привело к двум крупным революциям в физике, которые привели к сдвигу в исходной научной парадигме: теории относительности и развитию квантовой механики. В этой статье описывается, как физики открыли ограничения классической физики и разработали основные концепции квантовой теории, пришедшей на смену ей в первые десятилетия 20 века. Он использует эти концепции примерно в том порядке, в котором они были впервые обнаружены. Для более полной истории этого предмета см. История квантовой механики.
Свет в некоторых аспектах ведет себя как частицы, а в других аспектах как волны. Материя - "вещество" Вселенной, состоящее из таких частиц, как электроны и атомы - также демонстрирует волнообразное поведение. Некоторые источники света, такие как неоновые огни, излучают только частоты света, небольшой набор отдельных чистых цветов, определяемых атомной структурой неона. Квантовая механика показывает, что свет, наряду со всеми другими формами электромагнитного излучения, называемые фотонами, и предсказывает его спектральные энергии (соответствующие чистым цветов), и интенсивности его световых лучей. Одиночный фотон - это квант, или самая маленькая наблюдаемая часть электромагнитного поля. Частичный фотон экспериментально никогда не наблюдается. В более широком смысле квантовая механика показывает, что многие свойства объектов, такие как положение, скорость и угловой момент, которые казались непрерывными в масштабе классической механики, оказываются (в очень крошечных, увеличенная шкала квантовой механики) квантованы. Такие свойства элементов различных частиц должны одно из таких значений принимать невелик, неоднородности проявляются только в очень крошечных (атомных) масштабах..
Многие аспекты квантовой механики противоречат здравому смыслу и могут казаться парадоксальными, что они описывают поведение, совершенно отличное от того, что наблюдается в более крупных масштабах. По словам квантового физика Ричарда Фейнмана, квантовая механика имеет дело с «природой такой, какая она есть - абсурдной».
Например, принцип неопределенности квантовой механики означает что чем точнее одно измерение (например, положение частиц), тем менее точное другое дополнительное измерение, относящееся к той же части (например, ее скорость ) должен стать.
Другим примером является запутанность, в измерении любого двузначного состояния частиц (например, свет поляризовано вверх или вниз) производится на одном из двух "запутанных" частиц, которые находятся очень далеко друг от друга, приводят к тому, что последующее измерение на другой частице всегда будет другим из двух значений (например, поляризованным в противоположном направлении).
Последний пример - сверхтекучесть, в которой контейнер с жидким гелием, охлажденный до температуры, близкой к абсолютному нулю, самопроизвольно (медленно) течет вверх и над отверстием. контейнера против силы тяжести.
 Горячий металл rk. Желто-оранжевое свечение - это видимая часть теплового излучения, испускаемого из-за высокой температуры. Все остальное на картинке также светится тепловым излучением, но менее ярко и на более длинных волнах, чем может строительство человеческий глаз. Камера дальнего инфракрасного диапазона может наблюдать это излучение.
Горячий металл rk. Желто-оранжевое свечение - это видимая часть теплового излучения, испускаемого из-за высокой температуры. Все остальное на картинке также светится тепловым излучением, но менее ярко и на более длинных волнах, чем может строительство человеческий глаз. Камера дальнего инфракрасного диапазона может наблюдать это излучение. Тепловое излучение - это электромагнитное излучение, исходящее от поверхности объекта из-за внутренней энергии объекта. Если объект достаточно нагревается, он начинает излучать свет на красном фоне , поскольку он становится красным.
Нагревание приводит к изменению цвета красного на желтый, белый и синий, поскольку он излучает свет с более короткими длинами волн (более высокими частотами). Идеальный излучатель также является идеальным поглотителем: в холодном погоду такой объект выглядит совершенно черным, потому что он поглощает весь падающий на него свет и не излучает его. Следовательно, идеальное тепловое излучение известно как черное тело, испускаемое им излучение называется излучением черного тела.
 Прогноз количества теплового излучения различных частот, испускаемых телом.. Правильные значения, предсказанные законом Планка (зеленый), контрастируют с классическими значениями закона Рэлея-Джинса (красный) и аппроксимации Вина (синий).
Прогноз количества теплового излучения различных частот, испускаемых телом.. Правильные значения, предсказанные законом Планка (зеленый), контрастируют с классическими значениями закона Рэлея-Джинса (красный) и аппроксимации Вина (синий). В конце 19 века, тепловое излучение было достаточно хорошо охарактеризовано экспериментально. Классическая физика привела к закон Рэлея - Джинса, который, как показано на рисунке, хорошо согласуется с экспериментальными результатами на низких частотах, но сильно не согласуется с высокими частотами. Физики искали единую теорию, объясняющую все экспериментальные результаты.
Первая модель, которая могла объяснить полный спектр теплового излучения, была предложена Максом Планком в 1900 году. Он использует математическую модель, в которой тепловое излучение находилось в равновесии с набором гармонических осцилляторов. Чтобы воспроизвести экспериментальные результаты, он должен предположить, что каждый осциллятор излучает целое число единиц энергии на своей единственной характеристической частоте, а не может излучать любое произвольное количество энергии. Другими словами, энергия, излучаемая осциллятором, была квантована. Согласно Планку квант энергии для каждого осциллятора был пропорционален частот осциллятора; константа пропорциональности теперь известна как постоянная Планка. Постоянная Планка, обычно обозначаемая как h, имеет значение 6,63 · 10 Дж · с. Таким образом, энергия E осциллятора частоты f определяется выражением

Чтобы изменить цвет такого излучающего тела, необходимо изменить его температуру. Закон Планка объясняет, почему: увеличение температуры тела позволяет ему излучать больше энергии в целом и означает, что большая часть энергии направляется к фиолетовому концу.
Закон Планка был первой квантовой теорией в физике, и Планк получил Нобелевскую премию в 1918 году «в знак признания заслуг, который он оказал развитие физики своим открытием квантов энергии». Однако в то время Планкал квантование чисто эвристической математической конструкцией, а не (как сейчас считается) фундаментальным изменением в нашем понимании мира.
 Альберт Эйнштейн c.1905
Альберт Эйнштейн c.1905 В 1905 году Альберт Эйнштейн сделал дополнительный шаг. Это предположение, что квантование было не просто математической конструкцией, возникающими в отдельных пакетах, которые теперь называются фотонами. Энергия одного фотона света с кругом 


На протяжении веков ученые спорили между двумя возможными теориями света: была ли это волна или вместо этого была поток крошечных частиц ? К 19 веку споры в целом считанными в пользу волновой теории, поскольку она могла получить наблюдаемые эффекты, такие как рефракция, дифракция, интерференция и поляризация. Джеймс Клерк Максвелл показал, что электричество, магнетизм и свет проявления проявлениями одного и того же явления: электромагнитного поля. Уравнения Максвелла, которые имеют полный набор законов классического электромагнетизма, описывают свет как волны: комбинацию колеблющихся электрических и магнитных полей. Из-за преобладания доказательств в пользу волновой теории идеи Эйнштейна поначалу были встречены с большим скептицизмом. В конце концов, однако, предпочтение стало отдавать фотонной модели. Одним из наиболее значительных доказательств в его пользуется его способность объяснять несколько загадочных свойств фотоэлектрического эффекта, описанных в следующем разделе. Тем не менее, аналогия с волной оставалась незаменимой для понимания других характеристик света: дифракция, преломление и интерференция.
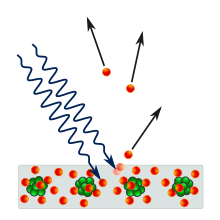 Свет падает на поверхность слева. Если частота света достаточно высока, т.е. если он обеспечивает достаточную энергию, отрицательные заряженные электроны выбрасываются из металла.
Свет падает на поверхность слева. Если частота света достаточно высока, т.е. если он обеспечивает достаточную энергию, отрицательные заряженные электроны выбрасываются из металла. В 1887 году Генрих Герц заметил, что когда свет с достаточной контрастностью падает на металлическую поверхность, поверхность испускает электроны. В 1902 году Филипп Ленард обнаружил, что максимально возможная энергия выброшенного электрона с размером света, а не с интенсивностью : если частота слишком мала, электроны не выбрасываются независимо от интенсивности. Сильные лучи света по направлению к красному концу должны быть электрические, в то время как слабые лучи света по направлению к фиолетовому концу будут все более и более высокие напряжения. Самая низкая частота света, которая может вызвать испускание электронов, называемая частота, различается для разных металлов. Это наблюдение противоречит классическому электромагнетизму, согласно которой энергия электрона должна быть пропорциональна падающего излучения. Таким образом, когда физики впервые появляются, демонстрирующие фотоэлектрический эффект, они получают более высокую интенсивность света к более высокому напряжению от фотоэлектрического устройства.
Эйнштейн объяснил эффект, постулировав, что луч света представляет собой поток частиц («фотонов ») и что представляет собой луч частоту f, то каждый фотон имеет энергию равно hf. Электрон может быть поражен только одиночным фотоном, который передает электрону максимум энергии hf. Следовательно, интенсивность луча не оказывает никакого влияния, и только его частота определяет максимальную энергию, которая может быть перед электрону.
Чтобы объяснить пороговый эффект, Эйнштейн утверждал, что для этого требуется определенное количество энергии, называемое выходом и обозначается φ для удаления электрона из металла. Это количество энергии разное для каждого металла. Если энергия фотона меньше работы выхода, то он не несет достаточной энергии для удаления электрона из металла. Пороговая частота f 0 - это частота фотона, энергия которой равна работе выхода:

Если f больше f 0, energy hf достаточно, чтобы удалить электрон. Выброшенный электрон имеет кинетическую энергию, E K, которая, самая большая, равна энергии фотона за вычетом энергии, необходимой для вытеснения электрона из металла:

Описание Эйнштейном света как состоящего из частиц расширило планковское представление о квантованной энергии, которое заключается в том, что отдельный фотон заданная частота f доставляет неизменное количество энергии hf. Другими словами, отдельные фотоны могут отдавать больше или меньше энергии, но только в зависимости от их частот. В природе одиночные фотоны встречаются редко. Солнце и излучение, используемое в 19 веке, каждую секунду излучают огромное количество фотонов. Идея Эйнштейна о том, что энергия, содержащиеаяся в отдельных частях света, зависит от их частоты, позволяет объяснить экспериментальные результаты, которые казались нелогичными. Однако, хотя фотон является частицей, он все еще описывался как обладающий волнообразным своим частотами. Фактически, учет света как частиц недостаточен, и его волнообразный характер все еще требуется.
Взаимосвязь между электромагнитным излучением и энергией каждого отдельного фотона, поэтому ультрафиолетовый свет может вызвать солнечный ожог, а видимый или инфракрасный свет - нет. Фотон ультрафиолетового света излучает большое количество энергии - достаточно, для повреждения клеток клеток, например, при солнечном ожоге. Фотон инфракрасного света дает меньше энергии - ее достаточно, чтобы согреть кожу. Итак, инфракрасная лампа может согреть большую поверхность, возможно, достаточно, чтобы людям было комфортно в холодной комнате.
Все фотоны одной и той же частоты имеют одинаковую энергию, и все фотоны разных частот пропорционально (порядок 1, E фотон = hf) разные энергии. Однако, энергия передается, передаваемая фотонами, сохраняет на любой заданной частоте, начальное энергетическое электронов в фотоэлектрическом состоянии до поглощения света не обязательно является однородным. В случае отдельных электронов могут иметь место аномальные результаты. Например, электрон, который уже был возбужден выше равновесного уровня фотоэлектрического устройства, может быть выброшен, когда он поглощает нехарактерно низкочастотное излучение. Однако статистически характерное поведение фотоэлектрического устройства ведет себя подавляющего его электронов, которые находятся на своем равновесном уровне. Этот момент помогает понять разницу между изучением отдельных частиц в квантовой динамике и изучением массивных частиц в классической физике.
К началу 20-го века для доказательства потребовалась модель атома с диффузным облаком отрицательно заряженно электронов, окружающих небольшое плотное положительно заряженное ядро. Эти свойства предложили модель, в которой электроны вращаются вокруг ядра, как на планете, вращаются вокруг Солнца. Однако также известно, что атом в этой модели будет нестабильным: согласно классической теории, вращающиеся электроны испытывают центростремительное ускорение и, следовательно, испускать электромагнитное излучение, потеря энергии также заставляет их двигаться по спирали к ядру, сталкиваясь с ним за доли секунды.
Вторая неотложная загадка был спектром излучения элементов. Когда газ нагревается, он излучает свет только на дискретных частотах. Например, видимый свет, излучаемый водородом, состоит из четырех разных цветов, как показано на рисунке. Интенсивность света на разных частотах тоже разная. Напротив, белый свет представляет собой непрерывное излучение во всем диапазоне видимых частот. К концу девятнадцатого века простое правило, известное как формула Бальмера, показало, как частоты разных линий связаны друг с другом, хотя без объяснения, почему это было так, и без каких-либо предсказаний относительно интенсивностей. Формула также предсказала некоторые дополнительные спектральные линии в ультрафиолетовом и инфракрасном свете, которые в то время не наблюдались. Эти линии позже наблюдались экспериментально, что повысило уверенность в формулы.
 Спектр излучения водорода. При возбуждении газообразный водород излучает свет четырех различных цветов (спектральных линий) в видимой области, а также ряд линий в инфракрасной и ультрафиолетовой области. Математическая формула, описывающая спектр излучения водорода
Спектр излучения водорода. При возбуждении газообразный водород излучает свет четырех различных цветов (спектральных линий) в видимой области, а также ряд линий в инфракрасной и ультрафиолетовой области. Математическая формула, описывающая спектр излучения водорода В 1885 г. Швейский математик Иоганн Бальмер обнаружил, что каждая длина волны λ (лямбда) в видимом спектре водорода связана с некоторым целым числом уравнением

где B - постоянная, определенная Бальмером равная 364,56 нм.
В 1888 г. Йоханнес Ридберг обобщил и значительно увеличил объяснительную полезность формулы Бальмера. Он предсказал, что связано с двумя целыми числами n и m в соответствии с тем, что сейчас известно как формула Ридберга :

где R - постоянная Ридберга, равная 0,0110 нм, а должно быть больше m.
Формула Ридберга определяет четыре длины волны водорода, задаваемая m = 2 и n = 3, 4, 5, 6. Она также предсказывает дополнительные волны в спектре излучения: для m = 1 и для n>1, Ультрафиолетового излучения, а для m = 3 и n>3 должна быть длина волны ультрафиолетового излучения. Экспериментальное наблюдение этих длинных волн два десятилетия спустя: в 1908 году Луи Пашен нашел некоторые из предсказанных длин волн инфракрасного излучения, а в 1914 году Теодор Лайман нашел некоторые из предсказанных длин волн ультрафиолета.
И в формулах Бальмера, и в формулах Ридберга используются целые числа: в современных терминах они означают, что какое-то свойство атома квантуется. Понимание того, что это было как свойство и почему оно было квантовой механикой, было частью развития квантовой механики, как показано в остальной части этой статьи.
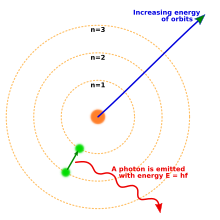 модель Бора атома, показывающая переход электрона с одной орбиты на другую, испуская фотон
модель Бора атома, показывающая переход электрона с одной орбиты на другую, испуская фотон В 1913 году Нильс Бор использует новую модель атом, включающий квантованные электронные орбиты: электроны по-прежнему вращаются вокруг ядра так же, как планеты вращаются вокруг Солнца, но им разрешено жить только на определенных орбитах, а не на любом произвольном расстоянии. Когда атом излучал (или поглощал) энергию, электрон не двигался по непрерывной траектории от одной орбиты вокруг ядра к другой, как можно было бы ожидать в классической теории. Вместо этого электрон мгновенно перескочил бы с одной орбиты на другую, испуская излучаемый свет в виде фотона. Возможные энергии фотонов, испускаемых каждым элементом, определялись разницей в энергии между орбитами, и поэтому спектр излучения для каждого элемента будет содержать несколько линий.
 Нильс Бор в молодости
Нильс Бор в молодости Начиная с Только одно простое предположение о правиле, которому должны подчиняться орбиты, модель Бора смогла связать наблюдаемые спектральные линии в спектре излучения водорода с ранее известными константами. В модели Бора электрону не разрешалосьнепрерывно излучением энергии и врезаться в ядро: как только он находился на ближайшей разрешенной орбите, он оставался стабильным навсегда. Модель Бора не объясняет, почему орбиты должны быть квантовым образом, и не могла сделать точных прогнозов для более чем одним электроном или объяснить, почему одни спектральные линии ярче других.
Некоторые фундаментальные предположения модели Бора вскоре оказались неверными, но ключевой результат о том, что дискретные линии в спектрах колебания возникают из-за некоторых свойств электронов в квантованных атомах, верен. Фактическое поведение электронов разительно отличается от поведения атома, что мы видим в мире повседневного опыта; эта современная квантово-механическая модель атома обсуждается ниже.
Более подробное объяснение модели БораБор предположил, что угловой момент, L, электрона квантуется:

где n - целое число, а h - постоянная Планка. Исходя из этого предположения, закон Кулона и уравнения кругового движения показывают, что электрон с n единицами углового момента вращается вокруг протона на расстоянии r, заданном как
 ,
,где k e - кулоновская постоянная, m - масса электрона, а e - заряд электрона. Для простоты это записывается как

, где a 0, называется Боровский радиус, равенство 0,0529 нм. Радиус Бора - это радиус наименьшей допустимой орбиты.
Энергию электрона также можно рассчитать по формуле
 .
.Таким образом, предположение Бора о квантовании углового момента означает, что электрон может находиться только на определенных орбитах. вокруг ядра, и что оно может иметь только верх энергии. Следствием этих ограничений является то, что электрон не может непрерывно воздействовать на ядро: он не может непрерывно излучать энергию и не может приближаться к ядру ближе, чем 0 (радиус Бора).
Электрон теряет энергию, мгновенно перескакивая с исходной орбиты на более низкую; дополнительная энергия испускается в виде фотона. И наоборот, электрон, который поглощает фотон, получает энергию и, следовательно, перескакивает на орбиту, расположенную дальше от ядра.
Каждый фотон светящегося атомарного водорода возникает из-за того, что электрон движется с более высокой орбиты с радиусом r51>n на более низкую орбиту, r m. Энергия E γ этого фотона представляет собой разность энергий E n и E m электрона:

Уравнение Уравнение Планка показывает, что энергия фотона связана с его длиной волны волны воздушного потока E γ = hc / λ, длина волн света, которые могут быть испущены, определяется как

Это уравнение имеет ту же форму, что и формула Ридберга, и предсказывает что постоянная R должна быть задана как

Следовательно, модель атома Бора может предсказать спектр водород через фундаментальные константы. Однако он не смог сделать точных прогнозов для многоэлектронных атомов или объяснить, почему одни спектральные линии ярче других.
 Луи де Бройль в 1929 году. Де Бройль получил Нобелевскую премию по физике за предсказание, что материя действует как волна, сделанное в его докторской диссертации 1924 года.
Луи де Бройль в 1929 году. Де Бройль получил Нобелевскую премию по физике за предсказание, что материя действует как волна, сделанное в его докторской диссертации 1924 года. Подобно тому, как свет обладает волнообразными свойствами, так и свойствами частиц, материя также обладает волнообразными свойствами..
Материя, ведущая себя как волна, впервые была экспериментально настроена для электронов: пучок электронов может проявлять дифракция, как луч света или водная волна. Позднее аналогичные волновые явления были обнаружены для атомов и даже молекул.
Длина волны λ, связанная с любым объектом, связанная с его импульсом p через постоянную Планка, h:

Отношение, называемое гипотезой де Бройля, справедливо для всех типов материи: вся материя проявляет свойства как частицы, так и волн.
Концепция дуальности волна-частица гласит, что ни классическая концепция объектов «частицы», ни «волна» не может полностью описать поведение квантового масштаба, будь то фотоны или материя. Дуальность волны-частица является примером принципа дополнительных в квантовой физике. Элегантный пример дуальности волны-частица, эксперимент с двойной щелью, обсуждается в следующем разделе.
 Дифракционная картина, полученная, когда свет проходит через одну щель (вверху), и интерференционная картина, созданная двумя щелями (внизу). Гораздо более сложный узор из двух щелей с его мелкомасштабными интерференционными полосами демонстрирует волновое распространение света.
Дифракционная картина, полученная, когда свет проходит через одну щель (вверху), и интерференционная картина, созданная двумя щелями (внизу). Гораздо более сложный узор из двух щелей с его мелкомасштабными интерференционными полосами демонстрирует волновое распространение света.  Воспроизвести медиа Эксперимент с двойной щелью для классической частицы, волны и квантовой частицы демонстрация дуальности волна-частица
Воспроизвести медиа Эксперимент с двойной щелью для классической частицы, волны и квантовой частицы демонстрация дуальности волна-частица В эксперименте с двумя щелями, который был использован был Томасом Янгом в 1803 году, а Огюстином Френелем десять лет спустя, луч света направлен через две узкие, близко расположенные щели, создавая интерференционную картину из светлых и темных полос на экране. Если одна из щелей закрыта, можно наивно ожидать, что интенсивность полос из-за интерференции увеличится вдвое. Фактически, видна гораздо более простая картина, дифракционная картина , диаметрально противоположная открытая щели. Точно такое же поведение могло быть показано в водных волнах, поэтому эксперимент с двумя щелями рассматривался как демонстрация волновой природы света.
Варианты эксперимента с двойной щелью были выполнены с использованием электронов, атомов и даже больших молекул, и виден тот же тип интерференционной картины. Таким образом, было установлено, что вся материя обладает какцами, так и волновыми характеристиками части.
Даже если интенсивность источника снижена, так что только одна часть (например, фотон или электрон) проходит через устройство за раз, со временем развивается та же интерференционная картина. Квантовая частица действует как волна при прохождении через двойные щели, но как частица при обнаружении. Это типичная особенность квантовой дополнительной функции: квантовая частица как волна в эксперименте для измерения своих волновых свойств и как части в эксперименте для измерения своих частицоподобных свойств. Точка на экране детектора, появляется любая отдельная часть, является результатом случайного процесса. Однако картина распределения многих частиц имитирует дифракционную картину, создаваемую волнами.
Де Бройль расширил модель атома Бора, показав, что электрон на орбите вокруг ядра можно рассматривать как имеющий волновую как свойства. В частности, электрон наблюдается только в ситуациях, которые допускают стоячую волну вокруг ядра. Примером этой волны волны является струна скрипки. Кажется, что волны, создаваемые струнным инструментом, колеблются на месте, перемещаясь от гребня к впадине вверх и вниз. Длина стоячей волны зависит от длины вибрирующего объекта и граничных условий. Например, поскольку струна скрипки закреплена на обоих концах, она может переносить стоячие волны с длиной волн 
Обработка квантовых событий де Бройлем послужила отправной точкой для Шредингера, когда он намеревался построить волновое уравнение для описания квантовых теоретических событий.
 Воспроизвести медиа Квантовое вращение в сравнении с классическим магнитом в эксперименте Штерна-Герлаха
Воспроизвести медиа Квантовое вращение в сравнении с классическим магнитом в эксперименте Штерна-Герлаха В 1922 году Отто Штерн и Вальтер Герлах выстрелил в атомы серебра через неоднородное магнитное поле. Относительно своего северного полюса, направленного вверх, вниз или где-то посередине, в классической механике магнит, брошенный через магнитное поле, может отклоняться на небольшое или большое расстояние вверх или вниз. Аналогичным образом действовали и атомы, которые Штерн и Герлах пробили через магнитное поле. Однако, хотя магниты можно было отклонить переменное расстояние, атомы всегда отклонялись на постоянное расстояние вверх или вниз. Это означало, что свойство атома, которое соответствует положению магнита, должно быть квантовано, положением одного из двух значений (вверх или вниз), в отличие от свободного выбора под любым углом.
Ральф Крониг создал теорию, согласно этим частицам, такие как атомы или электроны, ведут себя так, как если бы они вращались или «вращались» вокруг оси. Вращение учитывает недостающий магнитный момент и позволяет двум электронам на одном орбитали занимать разные квантовые состояния, если они «вращаются» в противоположных направлениях, таким образом удовлетворяя исключение принцип. Квантовое число представляет смысл спина (положительный или отрицательный).
Выбор ориентации магнитного поля, используемого в эксперименте Штерна - Герлаха, произвольный. В показанной здесь анимации поле вертикальное, поэтому атомы отклоняются вверх или вниз. Если повернуть магнит на четверть оборота, атомы отклонятся влево или вправо. Использование вертикального поля показывает, что вращение вдоль вертикальной оси квантуется, а использование горизонтального поля показывает, что вращение вдоль горизонтальной оси квантуется.
Если вместо попадания на экран детектора один из пучков атомов, выходящих из аппарата Штерна – Герлаха, попадает в другое (неоднородное) магнитное поле, ориентированное в том же направлении, все атомы отклоняются так же и во втором поле. Однако, если второе поле ориентировано под углом 90 ° к первому, то половина атомов отклоняется в одну сторону, а половина - в другую, так что спин атома вокруг горизонтальной и вертикальной осей не зависит друг от друга. Однако, если один из этих лучей (например, атомы, которые были отклонены вверх, а затем влево) проходит в третье магнитное поле, ориентированное так же, как и первое, половина атомов движется в одну сторону, а половина в другую, даже если все они изначально шла в том же направлении. Действие измерения спина атомов относительно горизонтального поля изменило их спин относительно вертикального поля.
Эксперимент Штерна-Герлаха демонстрирует ряд важных особенностей квантовой механики:
В 1925 году Вернер Гейзенберг попытался решить одну из проблем, оставшихся без ответа в модели Бора, объяснив интенсивность различные линии в спектре излучения водорода. Посредством ряда математических аналогий он выписал квантово-механический аналог для классического вычисления интенсивностей. Вскоре после этого коллега Гейзенберга Макс Борн понял, что метод Гейзенберга по вычислению вероятностей переходов между различными уровнями энергии может быть лучше всего выражен с помощью математической концепции матриц.
. В том же году, основываясь на гипотезе де Бройля, Эрвин Шредингер разработал уравнение, описывающее поведение квантово-механической волны. Математическая модель, названная уравнением Шредингера по имени его создателя, является центральной в квантовой механике, определяет разрешенные стационарные состояния квантовой системы и описывает, как квантовое состояние физической системы изменяется во времени. Сама волна описывается математической функцией, известной как «волновая функция ». Шредингер сказал, что волновая функция обеспечивает «средство для предсказания вероятности результатов измерения».
Шредингер смог вычислить энергетические уровни водорода, рассматривая электрон атома водорода как классическую волну., двигаясь в яме электрического потенциала, созданного протоном. Этот расчет точно воспроизводит уровни энергии модели Бора.
В мае 1926 года Шредингер доказал, что матричная механика Гейзенберга и его собственная волновая механика сделали одинаковые предсказания относительно свойств и поведения электрона; математически эти две теории имели общую форму. Тем не менее, двое мужчин расходились во мнениях относительно интерпретации их общей теории. Например, Гейзенберг принял теоретическое предсказание скачков электронов между орбиталями в атоме, но Шредингер надеялся, что теория, основанная на свойствах непрерывной волны, может избежать того, что он назвал (как перефразировал Вильгельм Вин ) "этот бред про квантовые квантовые В конце концов Гейзенберга победил, и квантовые скачки подтвердились.
 Институт Нильса Бора в Копенгагене, который был исследователей квантовой механики и связанных с ней предметов В 1920-х и 1930-х годах. Самые известные в мире физиков-теоретиков там провели время.
Институт Нильса Бора в Копенгагене, который был исследователей квантовой механики и связанных с ней предметов В 1920-х и 1930-х годах. Самые известные в мире физиков-теоретиков там провели время. Бор, Гейзенберг и другие пытались объяснить, что на самом деле означают экспериментальные результаты и другие модели Их описание, известное как копенгагенская интерпретация квантовой механики, было направлено на описание природы реальности, которая исследовалась с помощью измерений и описывалась математическими формулировками квантовой механики.
Основные принципы копенгагенской интерпретации:
 (фунт / кв. Дюйм). (Гейзенберг)
(фунт / кв. Дюйм). (Гейзенберг) изменяется с течением времени, дается уравнением Шредингера.
изменяется с течением времени, дается уравнением Шредингера.Различные последствия этих принципов обсуждаются более подробно. Зделах.
 Вернер Гейзенберг в возрасте 26 лет. чил Нобелевскую премию по физике в 1932 году за работу, которую он проделал примерно в это время.
Вернер Гейзенберг в возрасте 26 лет. чил Нобелевскую премию по физике в 1932 году за работу, которую он проделал примерно в это время. Предположим, требуется измерить положение и скорость объекта - например, автомобиля, проезжающего через радарный датчик скорости. Можно предположить, что автомобиль имеет определенное положение и скорость в данном момент времени. Насколько точно можно измерить эти значения, зависит от качества измерительного оборудования. Если точность измерительного оборудования улучшена, результат будет ближе к истинному значению. Это настолько важно, насколько это возможно.
В 1927 году Гейзенберг доказал, что это последнее предположение неверно. Кван механика показывает, что точнее измеряется или имеет одно свойство в терминах, тем менее может быть. Это утверждение как принцип неопределенности. Принцип неопределенности - это не только утверждение о точности нашего измерительного оборудования, но, более, касается концептуальной природы измеряемых величин - предположение, что автомобиль одновременно определяет положение и скорость, не работает в квантовой механике. В масштабе машин и людей эти неопределенности незначительны, но когда имеешь дело с атомами и электронами, они становятся критическими.
Гейзенберг в качестве иллюстрации привел измерений положения и импульса электрона с фотона. света. При измерении положения электрона, чем выше частота фотона, темнее измерения положения фотона с электроном, но тем больше возмущение электрона. Это связано с тем, что при столкновении с фотоном электрон поглощает случайное количество энергии, произведенное измерение его импульса все более неопределенным (импульс - это скорость, умноженная на массу), каждый обязательно измеряет свой -удар возмущенный от продуктов столкновения, а его импульсальный импульс. При использовании фотона более низкой частоты возмущение (и, следовательно, неопределенность) в импульсах меньше, но также и точность измерения положения удара.
В основе принципа неопределенности не лежит загадка, но тот простой факт, что для любого математического анализа в области положения и скорости (анализ Фурье ) достижение более резкой (более точной) кривой в области положения может быть выполнено только за счет более плавная (менее точная) кривая в области скорости, и наоборот. Для большей резкости в области положения требуется вклад большего количества частот в области скорости для создания более узкой кривой, и наоборот. Это фундаментальный компромисс, присущий любым таким заметным или дополнительным измерениям, но он действительно в самом маленьком (планковском) масштабе, близком к размеру элементарных частиц.
Принцип неопределенности показывает математически что неопределенность положения и импульссса частицы (импульс - это скорость, умноженная на массу). Планка.
Коллапс волновой функции означает, что измерение вызвало или преобразовало квантовое ( вероятностное или потенциальное) состояние в определенное измеренное значение. Это явление наблюдается только в квантовой механике, а не в классической механике.
Например, до того, как фотон на деле «появится» на экране обнаружения, его можно описать только с помощью набора вероятностей того, где он может появиться. Когда он действительно появляется, например, в ПЗС электронная камера, время и пространство, в котором он взаимодействует с этим, известны в очень жестких пределах. Однако фотон исчезла в процессе захвата (измерения), и его квантовая волновая функция исчезла вместе с ним. На его месте появилось какое-то макроскопическое физическое изменение на экране обнаружения, например, выставленное на листе фотопленки или изменение электрического потенциала в какой-либо ячейке ПЗС-матрицы.
Из-за принципа неопределенности утверждение как о положении, так и Импульсу частиц можно присвоить только вероятность того, что положение или импульс имеет некоторое числовое значение. Следовательно, необходимо указать разницу между состоянием чего-то неопределенного, например, электрона в облаке вероятности, и состоянием чего-то, имеющего определенное значение. Когда объект определенно может быть «прижатенно» в некотором отношении, говорят, что он обладает собственным состоянием.
В эксперименте Штерна-Герлаха, описанном выше, спин атома вокруг вертикальная ось имеет два собственных состояния: вверх и вниз. Прежде чем приступить к его измерению, мы можем только сказать, что любой отдельный атом с равной вероятностью будет обнаружен как имеющий вращение вверх или вниз. В процессе измерения волновая функция коллапсирует в одно из двух состояний.
Собственные состояния вращения вокруг вертикальной оси являются одновременно собственными состояниями вращения вокруг горизонтальной оси, поэтому у этого атома с вероятностью будет обнаружено любое значение вращения вокруг горизонтальной оси. Как описано в разделе, измерение горизонтальной оси может быть атому, который был раскручен вверх, вращаться вниз: измерение его вращения вокруг горизонтальной оси коллапсирует его волновую функцию в одном из собственных состояний измерения. что он больше не находится в собственном состоянии вращения вокруг вертикальной оси, поэтому может принимать любое значение.
 Вольфганг Паули
Вольфганг Паули В 1924 году Вольфганг Паули использует новую квантовую степень свободы (или квантовое число ) с двумя возможными значениями, чтобы разрешить несоответствия между наблюдаемыми молекулярными спектрами и предсказаниями квантовой механики. В частности, спектр имеет дублет или пару линий, отличающихся на небольшую величину, как ожидалась только одна линия. Паули сформулировал свой принцип исключения, заявив: «Не может существовать одинаковый набор квантовых чисел, чтобы два электрона внутри [него] имели одинаковый набор квантовых чисел».
Год спустя, Уленбек и Гаудсмит идентифицировали новую степень свободы Паули со своим собственным, называемым спином, эффекты которого наблюдались в эксперименте Штерна - Герлаха.
Модель атома Бора была по существу планетарной, с электронами, вращающимися вокруг ядерного «солнца». Однако неопределенности гласит, что электрон не может одновременно иметь точное местоположение и скорость, как планета. Говорят, что вместо классических орбитов электроны обитают на атомных орбиталях. Орбиталь - это «потенциальное местонахождение», в котором может быть обнаружен электрон, скорее местонахождение вероятностей, чем точное местоположение. Каждая орбиталь является трехмерной, и часто изображается как трехмерная область, в которой существует 95-процентная вероятность обнаружения электрона.
Шредингеру удалось вычислить уровни энергии. рассматривая атом водорода электрон как волну, представленную «волновой функцией » Ψ, в электрическом потенциале колодце, V, созданный протоном. Решениями уравнения Шредингера определяют распределения вероятностей положений и положений электронов. Орбитали имеют разные формы в трех измерений. Можно вычислить энергии различных орбиталей, и они точно соответствуют уровню энергии модели Бора.
В картине Шредингера каждый электрон имеет четыре свойства:
Общее название этих свойств - квантовое состояние электрона. Квантовое состояние можно описать, присвоить каждому из этих свойств число; они известны как квантовые числа электрона. Квантовое состояние электрона описывается его волновой функцией. Принцип исключения Паули требует, чтобы никакие два электрона в атоме не имели одинаковые значения всех четырех чисел.
 Формы атомных орбиталей. Ряды: 1с, 2п, 3д и 4ф. Слева направо
Формы атомных орбиталей. Ряды: 1с, 2п, 3д и 4ф. Слева направо  . Цвета показывают фазу волновой функции.
. Цвета показывают фазу волновой функции. Первым своим, описывающим орбиталь, является главное квантовое число, которое такое же, как в модели Бора. n обозначает уровень энергии каждой орбитали. Возможные значения n - целые числа:

Следующее квантовое число, азимутальное квантовое число, обозначенный l, описание форму орбитали. Форма является следствием углового момента орбитали. Угловой момент представляет собой сопротивление вращающегося объекта ускорения или замедления под действием внешней силы. Азимутальное квантовое число представляет собой орбитальный угловой момент электрона вокруг его ядра. Возможные значения l - целые числа от 0 до n - 1 (где n - главное квантовое число электрона):

Форма каждой орбитали обычно обозначается буквой, а не ее азимутальным квантовым числом. Первая форма (l = 0) обозначается буквой s (мнемоника означает «сфера»). Следующая фигура обозначается буквой р и имеет форму гантели. Другие орбитали имеют более сложную форму (см. атомные орбитали ) и обозначаются буквами d, f, g и т. Д.
Третье квантовое число, магнитный квант число настоящее магнитный момент электрона и обозначается m l (или просто m). Возможные значения для m l - целые числа от −l до l (где l - азимутальное квантовое число электрона):

Магнитное квантовое число измеряет компонент углового момента в определенном направлении. Выбор направления произвольный; обычно выбирается z-направление.
Четвертое квантовое число, квантовое число спина (относящееся к «ориентации» спина электрона), обозначается m s со значениями + ⁄ 2 или - как ⁄ 2.
Химик Линус Полинг в примере написал:
В случае атома гелия с двумя электронами в 1s-орбитали, принцип исключения Паули требует, чтобы два электрона различались области одного квантового числа. Их значения n, l и m l одинаковы. Соответственно, они должны отличаться величиной m s, которое может иметь значение + ⁄ 2 для одного электрона и - ⁄ 2 для другого.. "
Это основная структура и симметрия атомных орбиталей, а также то, как электроны заполняют их, приводит к организации периодической таблицы. То, как атомные орбитали на разных атомах объединяются в форму молекулярных орбиталей определяют структуру и прочную связь между атомами.
 Поль Дирак (1902–1984)
Поль Дирак (1902–1984) В 1928 году Поль Дирак расширил уравнение Паули, описывающее вращающиеся электроны, чтобы учесть специальную теорию относительности. Результатом стала теория, которая должным образом рассматривает события, такие как скорость при электрон вращается вокруг ядра со скоростью, составляющей значительную часть скорости. Используя простейшее электромагнитное взаимодействие, Дирак смог предсказать значение магнитного момента связанного со спином электрона, и обнаружил экспериментально наблюдаемое значение, которое было слишком большим для вращающейся заряженной сферы, управляемой классической физикой. Он смог найти спектральные линии атома водорода и воспроизвести из первых физических принципов успешную формулу Зоммерфельда для тонкой структуры водородный спектр.
Уравнения Дирака иногда давали отрицательное значение энергии, для чего он новое решение: он постулировал существование антиэлектрона и динамического вакуума. Это привело к многочастичной квантовой теории поля.
 Суперпозиция двух квантовых характеристик и двух возможностей разрешения.
Суперпозиция двух квантовых характеристик и двух возможностей разрешения. Принцип исключения Паули гласит, что два электрона в одной системе не может находиться в таком же состоянии. Однако природа создает возможность открытия каждого электрона, «наложенные» на каждое из них. Напомним, что волновые функции, которые одновременно выходят из двойных щелей, попадают на экран детектирования в состоянии суперпозиции. Ничто не является определенным до тех пор, пока наложенные сигналы не «схлопнутся». В этот момент электрон появляется где-то в соответствии с вероятностью, которая является квадратом абсолютного значения комплексных амплитуд двух наложенных друг на друга сигналов. Ситуация там уже очень абстрактная. Конкретный способ размышления о запутанных фотонах, фотонах, в которых два противоположных состояния накладываются на каждый из них в одном и том же событии, выглядит следующим образом:
Представьте, что у нас есть два состояния фотонов с цветовой кодировкой: одно состояние помечен синим, а другой штат - красный. Пусть суперпозиция красного и синего состояний проявляется (в воображении) как пурпурное состояние. Мы рассматриваем случай, когда два фотона образуются в результате одного атомного события. Возможно, они вызваны возбуждением кристалла, который обычно поглощает фотонные частоты и испускает два фотона с половиной исходной частоты. В этом случае фотоны связаны друг с другом общим происхождением в одном из случаев. Эта установка приводит к наложению состояния фотонов. Итак, два фотона выходят фиолетовыми. Если экспериментатор теперь проводит некоторый эксперимент, который определяет, является ли один из фотонов синим или красным, то этот эксперимент изменяет участвующий фотон с фотона, имеющий суперпозицию синей и красной характеристики, на фотон, имеет только одну из этих характеристик. Проблема, с которой столкнулся Эйнштейн с такой воображаемой ситуацией, заключалась в том, что если один из этих фотонов продолжал прыгать между зеркалами в лаборатории на Земле, а другой прошел бы половину пути к ближайшей звезде, то его двойник должен был проявить себя как синий или красный, это означало, что удаленный фотон теперь тоже должен был потерять свой фиолетовый статус. Поэтому всякий раз, когда его можно было исследовать после измерения его близнеца, он обязательно обнаруживался в состоянии, противоположном тому, что обнаружил его близнец.
Пытаясь показать, что квантовая механика не является законченной теорией, Эйнштейн начал предсказания теории о том, что две или более частицы, которые взаимодействовали в прошлом, могут оказаться сильно коррелированными при последующем измерении их различных свойств. Он стремился это кажущееся взаимодействие классическим способом, через их общее прошлое, и желательно не какими-то «жуткими действиями на расстоянии». Аргумент установлен в известной статье Эйнштейн, Подольский и Розен (1935; сокращенно EPR), в котором излагается то, что сейчас называется парадоксом EPR. Предполагаемая то, что сейчас обычно называют локальным реализмом, ЭПР попытка показать на основе квантовой теории, что части положения и положения, и одновременно, в то время как, согласно копенгагенской интерпретации, только один из этих двух свойств действительно существует в тот момент, когда они измеряются. ЭПР пришел к выводу, что квантовая теория неполно, поскольку она отказывается рассматривать физические свойства, которые объективно существуют в природе. (Эйнштейн, Подольский и Розен, 1935 г. в настоящее время является наиболее цитируемой публикацией Эйнштейна в физических журналах.) В том же году Эрвин Шрёдингер использовал слово «запутанность» и заявление: «Я бы не назвал его, а скорее не назвал его, а скорее.. характерная черта квантовой механики ». С тех пор, как ирландский физик Джон Стюарт Белл теоретически и экспериментально опровергорию теорий «скрытых чисел» Эйнштейна, Подольского и Розена, большинство физиков приняли запутанность как реальное явление. Однако есть некоторый спор меньшинства. Неравенства Белла - самый сильный вызов утверждениям Эйнштейна.
Идея квантовой теории поля началась в конце 1920-х годов с британского физика Пола Дирака, когда он попытался квантовать энергию электромагнитного поля ; так же, как в квантовой механике, квантовалась энергия электрона в атоме водорода. Квантование - это процедура построения квантовой теории, начиная с классической теории.
Мерриам-Вебстер указать поле в физике как «область или пространство, в котором существует данный эффект (например, магнетизм )». Другие эффекты, которые проявляются в виде полей, - это гравитация и статическое электричество. В 2008 году физик Ричард Хаммонд писал:
Иногда мы различаем квантовую механику (КМ) и квантовую теорию поля (КТП). КМ относится к системе, в которой количество частиц фиксировано, а поля (такие как электромеханическое поле) непрерывными классическими объектами. КТП... идет дальше и позволяет создавать и уничтожать частицы...
Однако он добавил, что квантовая механика часто используется для обозначения «всего понятия квантовой точки зрения».
В 1931 году предположил существование частиц, которые позже стали известны как антивещество. Дирак разделил Нобелевскую премию по физике за 1933 год с Шредингером «за открытие продуктивных форм атомной теории ".
На первый взгляд квантовая теория поля допускает бесконечное число частиц, и оставляет на усмотрение теории предсказать, сколько и с какими вероятностями или числами они должны существовать. При дальнейшем развитии теория часто противоречит наблюдению. эмпирические законы сохранения, такие как закон масса - энергия, усиливают усилие на ограничительную математическую форму теории, которые с математической точки зрения являются привередливыми точками. Последний факт затрудняет обработку квантовых теорий поля, но также привел к дальнейшим ограничениям допустимые формы теории; сложности упомянутой ниже в рубрике перенормировка.
Квантовая электродинамика (КЭД) - это название квантовой теории т. он электромагнитная сила. Понимание QED начинается с понимания электромагнетизма. Электромагнетизм можно назвать «электродинамикой», потому что это динамическое взаимодействие между электрическими и магнитными силами. Электромагнетизм начинается с электрический заряд.
. Электрические заряды - это новые источники электрические поля. Электрическое поле - это поле, которое действует на любые частицы, несущие электрические заряды, в любом пространстве. Сюда, среди прочего, входят электрон, протон и даже кварки. При приложении силы электрического заряды перемещаются, течет ток и создается магнитное поле. Изменяющееся магнитное поле, в свою очередь, вызывает электрический ток (часто движущиеся электроны). Физическое описание взаимодействующих заряженных частиц, электрических токов, электрических полей и магнитных полей называется электромагнетизмом.
. В 1928 году Поль Дирак создал релятивистскую квантовую теорию электромагнетизма. Это пра былродитель современной квантовой электродинамики, поскольку он содержал существенные компоненты теории современной. Однако проблема неразрешимых бесконечностей развивалась в этой релятивистской квантовой теории. Спустя перенормировка в степени решила эту проблему. Первоначально соответствующая функция из ее создателей как подозрительная временная процедура, перенормировка в конечном итоге стала важным и самосогласованным инструментом в КЭД и других областях физики. Кроме того, в конце 1940-х годов диаграмма Фейнмана представлены все возможные встречи, относящиеся к данному событию. Диаграммы части показывают, в частности, что электромагнитная сила - это обмен фотонами между взаимодействующими элементами.
Лэмбовский сдвиг является примером предсказания квантовой электродинамики, которое было экспериментально подтверждено. Это эффект, при котором квантовая природа электромагнитного поля заставляет уровни энергии в атоме или ионе незначительно отклоняться от того, чем они были бы в противном случае. В результате спектральные линии могут сдвигаться или расщепляться.
Точно так же в свободно распространяющейся электромагнитной волне ток может быть просто абстрактным током смещения, вместо того, чтобы вовлекать носители заряда. В QED его полное описание существенно использует короткоживущие виртуальные частицы. Там QED снова подтверждает более раннюю, довольно загадочную концепцию.
В 1960-х гг. физики поняли, что КЭД разрушается при чрезвычайно высоких энергиях. Из этого несоответствия была открыта Стандартная модель физики элементарных частиц, которая в теории исправила нарушение более высоких энергий. Это еще одна расширенная квантовая теория поля, которая объединяет электромагнитное и слабое взаимодействие в одну теорию. Это называется теорией электрослабого взаимодействия.
. Кроме того, Стандартная модель содержит высокоэнергетическое объединение теории электрослабого взаимодействия с сильной силой, описываемой квантовой хромодинамикой. Он также постулирует связь с гравитацией как еще одну калибровочную теорию, но эта связь по состоянию на 2015 год все еще плохо изучена. Успешное предсказание теории частицы Хиггса для объяснения инертной массы было подтверждено Большим адронным коллайдером, и, таким образом, Стандартная модель теперь считается основным и более или менее полным описанием физика элементарных частиц, как мы ее знаем.
Физические измерения, уравнения и прогнозы, относящиеся к квантовой механике, согласованы и имеют очень высокий уровень подтверждения. Однако вопрос о том, что эти абстрактные модели говорят о сущности реального мира, получил разные ответы. Эти интерпретации весьма разнообразны и иногда несколько абстрактны. Например, Копенгагенская интерпретация гласит, что до измерения утверждения о свойствах частиц полностью бессмысленны, в то время как в интерпретации многих миров описывает существование мультивселенной. состоит из всевозможных вселенных.
Приложения квантовой механики включают лазер, транзистор, электронный микроскоп и магнитно-резонанснаятомография. Особый класс квантово-механических приложений связан с макроскопическими квантовыми явлениями, такими как сверхтекучий гелий и сверхпроводники. Изучение полупроводников привело к изобретению диода и транзистора, незаменимых для современной электроники.
даже в простом переключателе света, квантовое туннелирование абсолютно необходимо, поскольку в противном случае электроны в электрическом токе не смогли бы проникнуть через потенциальный барьер, состоящий из слоя оксида. Флэш-память, найденные в USB-накопителях, также используют квантовое туннелирование для стирания своих ячеек памяти.
Следующие заголовки, написанные работающими физиками, представляют собой попытку донести квантовую теорию до непрофессионалов, используя минимум технических средств.
| В Wikibook Quantum Mechanics есть страница на тему: Introduction to Quantum Mechanics |