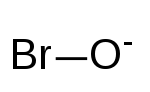 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК гипобромит | |
| Идентификаторы | |
| Количество CAS | |
| 3D модель ( JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| Ссылка на Гмелин | 1040 |
| PubChem CID | |
| Панель управления CompTox ( EPA) | |
ИнЧИ
| |
Улыбки
| |
| Характеристики | |
| Химическая формула | BrO - |
| Молярная масса | 95,904 г / моль |
| Конъюгированная кислота | Гипобромистая кислота |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| | |
| Ссылки на инфобоксы | |
Гипобромит ионы, называемые также щелочно - бром водой, является BrO -. Бром находится в степени окисления +1. Гипобромит - это соединение брома, аналогичное гипохлоритам, содержащимся в обычных отбеливателях и в иммунных клетках. Во многих отношениях гипобромит действует так же, как гипохлорит, а также используется в качестве гермицида и противопаразитарного средства как в промышленности, так и в иммунной системе.
Соли гипобромита образуются при обработке брома водной щелочью, такой как гидроксид натрия или калия. При 20 ° C реакция идет быстро.
В этой реакции бром диспропорционирует (часть подвергается восстановлению, а часть окислению) от степени окисления 0 (Br 2 ) до степени окисления -1 (Br -) и степени окисления +1 (BrO -). Гипобромит натрия можно выделить в виде твердого вещества оранжевого цвета.
Вторичная реакция, при которой гипобромит самопроизвольно диспропорционирует до бромида (степень окисления брома -1) и бромата (степень окисления брома +5), происходит быстро при 20 ° C и медленно при 0 ° C.
Следовательно, в реакции 2 образование и пропорции продуктов степени окисления брома -1, +1 и +5 можно регулировать температурой. Гипобромит не является термодинамически стабильным при любом pH (см. Диаграмму Пурбе для брома на http://www.eosremediation.com/download/Chemistry/Chemical%20Properties/Eh_pH_Diagrams.pdf ), но он кинетически заблокирован в направлении дальнейшего диспропорционирования на бромат и бромид выше pKa HBrO.
Эти реакции брома аналогичны реакциям хлора с образованием гипохлорита и хлората. Соответствующая реакция хлора 1 (с образованием ClO -) протекает быстро при 20 ° C, а реакция 2 (с образованием ClO - 3 ) происходит медленно при 20 ° C и быстро при 70 ° C.
Гипобромит - это соединение, содержащее этот анион. Примеры включают гипобромит натрия и гипобромит калия.
Бромид из рациона, естественно присутствующий в крови, используется эозинофилами, лейкоцитами класса гранулоцитов, специализирующимися на борьбе с многоклеточными паразитами. Эти клетки реагируют бромидом с пероксидом с образованием гипобромита под действием пероксидазы эозинофилов, фермента галопероксидазы, который предпочтительно использует для этой цели бромид, а не хлорид.
Простые бромидные соли (такие как бромид натрия) также иногда используются в горячих ваннах и спа в качестве мягких бактерицидных агентов, используя действие добавленного окислителя (такого как перекись водорода) для образования гипобромита in situ аналогично действию пероксидазы на бромид в эозинофилах.
Было высказано предположение, что гипобромит является реактивным промежуточным продуктом в перегруппировке Хофмана.
Другие анионы брома:
| Степень окисления брома | −1 | +1 | +3 | +5 | +7 |
|---|---|---|---|---|---|
| Имя | бромид | гипобромит | бромит | бромат | пербромат |
| Формула | Br - | BrO - | Братан - 2 | Братан - 3 | Братан - 4 |
| Состав |  | | | |  |