| Папилломавирусная инфекция | |
|---|---|
| Другие имена | Вирус папилломы человека |
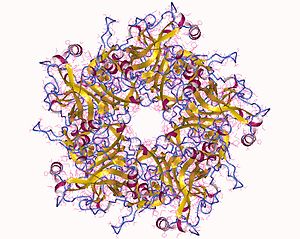 | |
| Главный капсидный белок L1 ВПЧ 11 | |
| Специальность | Инфекционные болезни, гинекология, онкология |
| Симптомы | Нет, бородавки |
| Осложнения | Рак шейки матки, вульвы, влагалища, полового члена, ануса, рта, миндалин или горла |
| Причины | Распространение вируса папилломы человека при прямом контакте |
| Факторы риска | половой контакт |
| Профилактика | Вакцины против ВПЧ, презервативы |
| Частота | Большинство людей в какой-то момент заражены |
Инфекция вируса папилломы человека ( инфекция ВПЧ) - это инфекция, вызываемая вирусом папилломы человека ( ВПЧ), ДНК-вирусом из семейства Papillomaviridae. Многие инфекции ВПЧ протекают бессимптомно, и 90% из них проходят спонтанно в течение двух лет. Однако в некоторых случаях инфекция ВПЧ сохраняется и приводит к появлению бородавок или предраковых поражений. Эти поражения, в зависимости от пораженного участка, увеличивают риск рака шейки матки, вульвы, влагалища, полового члена, заднего прохода, рта, миндалин или горла. Почти весь рак шейки матки возникает из-за ВПЧ; два штамма, HPV16 и HPV18, составляют 70% случаев. ВПЧ16 ответственен за почти 90% ВПЧ-положительных случаев рака ротоглотки. От 60% до 90% других видов рака, перечисленных выше, также связаны с ВПЧ. ВПЧ6 и ВПЧ11 являются частыми причинами остроконечных кондилом и папилломатоза гортани.
Инфекция ВПЧ вызывается вирусом папилломы человека, ДНК-вирусом из семейства папилломавирусов. Описано более 170 типов. Более 40 типов могут передаваться половым путем и инфицировать задний проход и гениталии. Факторы риска стойкой инфекции, передаваемой половым путем, включают ранний возраст первого полового акта, наличие нескольких половых партнеров, курение и слабую иммунную функцию. Эти типы обычно распространяются при постоянном прямом контакте кожа к коже, причем вагинальный и анальный секс являются наиболее распространенными методами. Кроме того, инфекция ВПЧ может передаваться от матери к ребенку во время беременности. Нет никаких доказательств того, что ВПЧ может передаваться через обычные предметы, такие как сиденья унитаза, но типы, вызывающие бородавки, могут распространяться через такие поверхности, как пол. Было обнаружено, что у пациентов с активным генитальным ВПЧ обнаружена ДНК ВПЧ на кончиках пальцев. Кроме того, ВПЧ не уничтожается обычными дезинфицирующими и дезинфицирующими средствами для рук, что увеличивает вероятность передачи вируса через фомиты. Человек может заразиться более чем одним типом ВПЧ. Известно, что ВПЧ поражает только людей.
Вакцины против ВПЧ могут предотвратить наиболее распространенные типы инфекций. Чтобы быть наиболее эффективным, прививка должна производиться до начала половой жизни и поэтому рекомендуется в возрасте от 9 до 13 лет. Скрининг на рак шейки матки, такой как тест Папаниколау («мазок Папаниколау») или обследование шейки матки после применения уксусной кислоты, может выявить как ранний рак, так и аномальные клетки, которые могут перерасти в рак. Скрининг позволяет начать лечение на ранней стадии, что приводит к лучшим результатам. Благодаря скринингу сократилось как количество случаев, так и количество смертей от рака шейки матки. Остроконечные кондиломы можно удалить замораживанием.
Почти каждый человек в какой-то момент своей жизни инфицирован ВПЧ. ВПЧ - самая распространенная инфекция, передающаяся половым путем (ИППП) во всем мире. По оценкам, в 2018 году во всем мире произошло 569000 новых случаев рака шейки матки, из которых 311000 умерли. Около 85% этих случаев рака шейки матки произошло в странах с низким и средним уровнем дохода. В Соединенных Штатах ежегодно происходит около 30 700 случаев рака, вызванного ВПЧ. Примерно у 1% сексуально активных взрослых есть остроконечные кондиломы. Случаи появления кожных бородавок были описаны со времен Древней Греции, а тот факт, что они вызваны вирусом, не был установлен до 1907 года.
Некоторые типы ВПЧ, такие как ВПЧ-5, могут вызывать инфекции, которые сохраняются на протяжении всей жизни человека, не проявляя никаких клинических симптомов. ВПЧ 1-го и 2-го типов могут вызывать у некоторых инфицированных людей обычные бородавки. ВПЧ 6 и 11 типов могут вызывать остроконечные кондиломы и папилломатоз гортани.
Многие типы ВПЧ канцерогены. В таблице ниже перечислены общие симптомы инфекции ВПЧ и связанных штаммов ВПЧ.
| Болезнь | Тип ВПЧ |
|---|---|
| Обычные бородавки | 2, 7, 22 |
| Подошвенные бородавки | 1, 2, 4, 63 |
| Плоские бородавки | 3, 10, 28 |
| Аногенитальные бородавки | 6, 11, 42, 44 и другие |
| Анальная дисплазия (высыпания) | 16, 18, 31, 53, 58 |
| Рак половых органов |
|
| Бородавчатая эпидермодисплазия | более 15 видов |
| Очаговая гиперплазия эпителия (рот) | 13, 32 |
| Папилломы во рту | 6, 7, 11, 16, 32 |
| Рак ротоглотки | 16 |
| Веррукозная киста | 60 |
| Папилломатоз гортани | 6, 11 |
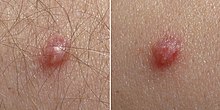 Папиллома
Папиллома  Образец отчета о тестировании ДНК на генотип ВПЧ из лаборатории
Образец отчета о тестировании ДНК на генотип ВПЧ из лаборатории Кожная инфекция (« кожная » инфекция) ВПЧ очень распространена. Кожные инфекции, вызванные ВПЧ, могут вызывать появление доброкачественных новообразований на коже, называемых бородавками ( бородавками ). Бородавки возникают из-за быстрого роста клеток на внешнем слое кожи. Хотя случаи бородавок были описаны еще со времен Древней Греции, их вирусная причина не была известна до 1907 года.
Кожные бородавки чаще всего возникают в детстве и обычно появляются и регрессируют спонтанно в течение недель или месяцев. Часто возникают рецидивирующие кожные бородавки. Считается, что все ВПЧ способны вызывать длительные «латентные» инфекции в небольшом количестве стволовых клеток, присутствующих в коже. Хотя эти скрытые инфекции невозможно полностью искоренить, считается, что иммунологический контроль блокирует появление таких симптомов, как бородавки. Иммунологический контроль зависит от типа ВПЧ, что означает, что человек может стать устойчивым к одному типу ВПЧ, оставаясь при этом восприимчивым к другим типам.
Типы бородавок включают:
Обычные, плоские и подошвенные бородавки гораздо реже передаются от человека к человеку.
ВПЧ-инфекция кожи в области гениталий является наиболее распространенной инфекцией, передаваемой половым путем. Такие инфекции связаны с генитальными или анальными бородавками (с медицинской точки зрения называемыми остроконечными кондиломами или венерическими бородавками), и эти бородавки являются наиболее легко распознаваемым признаком генитальной инфекции ВПЧ.
Штаммы ВПЧ, которые могут вызывать остроконечные кондиломы, обычно отличаются от штаммов, вызывающих бородавки на других частях тела, например, на руках или ногах или даже на внутренней поверхности бедер. Генитальные бородавки могут быть вызваны самыми разными типами ВПЧ, но на типы 6 и 11 вместе взятые приходится около 90% всех случаев. Однако в общей сложности более 40 типов ВПЧ передаются половым путем и могут инфицировать кожу заднего прохода и половых органов. Такие инфекции могут вызывать остроконечные кондиломы, хотя они также могут протекать бессимптомно.
Подавляющее большинство половых инфекций ВПЧ никогда не вызывают каких-либо явных симптомов и устраняются иммунной системой в течение нескольких месяцев. Более того, люди могут передавать вирус другим, даже если у них нет явных симптомов инфекции. Большинство людей заражаются генитальным ВПЧ в какой-то момент своей жизни, и в настоящее время инфицировано около 10% женщин. Значительное увеличение заболеваемости генитальной инфекцией ВПЧ происходит в том возрасте, когда люди начинают половую жизнь. Как и в случае с кожными ВПЧ, иммунитет к генитальному ВПЧ считается специфическим для определенного штамма ВПЧ.
Помимо остроконечных кондилом, инфекция, вызванная ВПЧ 6 и 11 типов, может вызвать редкое заболевание, известное как рецидивирующий папилломатоз гортани, при котором бородавки образуются на гортани или других участках дыхательных путей. Эти бородавки могут часто повторяться, могут мешать дыханию и в очень редких случаях могут прогрессировать до рака. По этим причинам может быть рекомендовано повторное хирургическое вмешательство по удалению бородавок.
 Рак, вызванный ВПЧ
Рак, вызванный ВПЧ Около дюжины типов ВПЧ (включая типы 16, 18, 31 и 45) называют типами «высокого риска», потому что стойкая инфекция связана с раком ротоглотки, гортани, вульвы, влагалища, шейки матки, полового члена и ануса. Все эти виды рака связаны с инфицированием ВПЧ, передаваемым половым путем, в многослойную эпителиальную ткань. Люди, инфицированные как ВПЧ, так и ВИЧ, имеют повышенный риск развития рака шейки матки или анального канала. ВПЧ 16 типа является штаммом, который с наибольшей вероятностью вызывает рак, и присутствует примерно в 47% всех случаев рака шейки матки, а также во многих случаях рака влагалища и вульвы, рака полового члена, рака анального канала и рака головы и шеи.
По оценкам, 561 200 новых случаев рака во всем мире (5,2% всех новых случаев рака) были связаны с ВПЧ в 2002 году, что делает ВПЧ одной из наиболее важных инфекционных причин рака. Рак, связанный с ВПЧ, составляет более 5% от общего числа диагностированных случаев рака во всем мире, и эта заболеваемость выше в развивающихся странах, где, по оценкам, ежегодно он вызывает почти полмиллиона случаев.
В Соединенных Штатах ежегодно происходит около 30 700 случаев рака, вызванного ВПЧ.
| Зона рака | Среднее годовое количество случаев | Приписываемый ВПЧ (оценка) | Приписываемый ВПЧ 16/18 (оценка) |
|---|---|---|---|
| Шейка матки | 11 771 | 10 700 | 7 800 |
| Глотка (мужчины) | 12 638 | 9 100 | 8 000 |
| Глотка (женщины) | 3 100 | 2 000 | 1,600 |
| Вульва | 3,554 | 2400 | 1,700 |
| Анус (женщины) | 3 260 | 3 000 | 2600 |
| Анус (мужчины) | 1,750 | 1,600 | 1,400 |
| Пенис | 1,168 | 700 | 600 |
| Влагалище | 802 | 600 | 400 |
| Прямая кишка (женщины) | 513 | 500 | 400 |
| Прямая кишка (мужчины) | 237 | 200 | 200 |
| Общий | 38 793 | 30 700 | 24 600 |
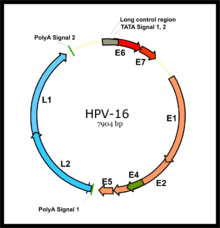 Организация генома вируса папилломы человека типа 16, одного из подтипов, вызывающих рак шейки матки (ранние гены E1-E7, поздние гены L1-L2: капсид)
Организация генома вируса папилломы человека типа 16, одного из подтипов, вызывающих рак шейки матки (ранние гены E1-E7, поздние гены L1-L2: капсид) У некоторых инфицированных людей их иммунная система может не контролировать ВПЧ. Затяжная инфекция типами ВПЧ высокого риска, такими как типы 16, 18, 31 и 45, может способствовать развитию рака. Сопутствующие факторы, такие как сигаретный дым, также могут повышать риск такого рака, связанного с ВПЧ.
Считается, что ВПЧ вызывает рак, интегрируя свой геном в ядерную ДНК. Некоторые из ранних генов, экспрессируемых HPV, такие как E6 и E7, действуют как онкогены, способствующие росту опухоли и злокачественной трансформации. Интеграция генома ВПЧ также может вызывать канцерогенез, способствуя нестабильности генома, связанной с изменениями числа копий ДНК.
E6 производит белок (также называемый E6), который связывается и инактивирует белок в клетке-хозяине, называемый p53. Обычно р53 предотвращает рост клеток и способствует их гибели при повреждении ДНК. p53 также активирует белок p21, который блокирует образование комплекса циклин D / Cdk4, тем самым предотвращая фосфорилирование RB и, в свою очередь, останавливая развитие клеточного цикла, предотвращая активацию E2F. Короче говоря, p53 - это белок-супрессор опухолей, который останавливает клеточный цикл и предотвращает рост и выживание клеток при повреждении ДНК. Таким образом, инактивация p53 с помощью E6 может способствовать нерегулируемому делению клеток, росту клеток и выживанию клеток - характеристикам рака.
E6 также имеет тесную связь с клеточным белком, связанным с E6 белком (E6-AP), который участвует в пути убиквитинлигазы, системе, которая действует для разложения белков. E6-AP связывает убиквитин с белком p53, тем самым сигнализируя его о протеосомной деградации.
Исследования также показали связь между широким спектром типов ВПЧ и плоскоклеточным раком кожи. В таких случаях исследования in vitro показывают, что белок E6 вируса ВПЧ может ингибировать апоптоз, вызванный ультрафиолетовым светом.
 Изображение художника о раке шейки матки, вызванном вирусом папилломы человека.
Изображение художника о раке шейки матки, вызванном вирусом папилломы человека. Почти все случаи рака шейки матки связаны с инфекцией ВПЧ, причем два типа, ВПЧ16 и ВПЧ18, присутствуют в 70% случаев. В 2012 году Международное агентство по изучению рака признало 12 типов ВПЧ канцерогенными для рака шейки матки: 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58 и 59. ВПЧ необходим для рак шейки матки. Стойкая инфекция ВПЧ увеличивает риск развития рака шейки матки. Лица, у которых наблюдается повышенная заболеваемость этими типами инфекций, - это женщины с ВИЧ / СПИДом, у которых риск рака шейки матки повышен в 22 раза.
Канцерогенные типы ВПЧ при раке шейки матки относятся к роду альфа-папилломавирусов и могут быть далее сгруппированы в клады ВПЧ. Два основных канцерогенные клады ВПЧ, alphapapillomavirus-9 (А9) и alphapapillomavirus-7 (А7), содержат HPV16 и HPV18, соответственно. Было показано, что эти две клады ВПЧ по-разному влияют на молекулярные характеристики опухоли и прогноз пациентов, при этом клада A7 связана с более агрессивными путями и худшим прогнозом.
В 2012 году во всем мире произошло около 528 000 новых случаев заболевания и 266 000 случаев смерти от рака шейки матки. Около 85% из них произошло в развивающихся странах.
Большинство инфекций шейки матки, вызванных ВПЧ, быстро устраняются иммунной системой и не прогрессируют до рака шейки матки (см. Ниже подраздел «Удаление» в вирусологии). Поскольку процесс преобразования нормальных клеток шейки матки в раковые происходит медленно, рак возникает у людей, инфицированных ВПЧ в течение длительного времени, обычно более десяти лет или более (стойкая инфекция). Более того, как инфекция ВПЧ, так и рак шейки матки вызывают метаболические модификации, которые могут быть коррелированы с аберрантной регуляцией ферментов, связанных с метаболическими путями.
Неевропейские (NE) варианты HPV16 значительно более канцерогены, чем европейские (E) варианты HPV16.
Исследования показывают связь между инфекцией ВПЧ и раком заднего прохода. ВПЧ, передающиеся половым путем, встречаются в большом проценте случаев рака анального канала. Более того, риск анального рака в 17–31 раз выше среди ВИЧ-положительных людей, которые были инфицированы ВПЧ высокого риска, и в 80 раз выше для особенно ВИЧ-положительных мужчин, имеющих половые контакты с мужчинами.
Скрининг анального мазка Папаниколау на рак анального канала может принести пользу некоторым субпопуляциям мужчин и женщин, занимающихся анальным сексом. Однако нет единого мнения о том, что такое обследование полезно и кому следует сдавать мазок Папаниколау из анального канала.
ВПЧ связан примерно с 50% случаев рака полового члена. В США на рак полового члена приходится около 0,5% всех случаев рака у мужчин. ВПЧ16 является наиболее часто обнаруживаемым типом. Риск рака полового члена увеличивается в 2-3 раза для людей, инфицированных как ВИЧ, так и ВПЧ.
Инфекция полости рта канцерогенными типами ВПЧ высокого риска (чаще всего ВПЧ 16) связана с увеличением числа случаев рака головы и шеи. Эта ассоциация не зависит от употребления табака и алкоголя.
На формы ВПЧ, передающиеся половым путем, приходится около 25% случаев рака ротовой полости и верхней части глотки (ротоглотки) во всем мире, но местный процент широко варьируется - от 70% в США до 4% в Бразилии. Вступление в анальный или оральный секс с партнером, инфицированным ВПЧ, может увеличить риск развития этих видов рака.
В Соединенных Штатах количество вновь диагностированных случаев рака головы и шеи, связанных с ВПЧ, превысило количество случаев рака шейки матки. Частота таких видов рака увеличилась с 0,8 случаев на 100 000 человек в 1988 году до 4,5 на 100 000 человек в 2012 году, а по состоянию на 2015 год этот показатель продолжал расти. Исследователи объясняют эти последние данные увеличением орального секса. Этот тип рака чаще встречается у мужчин, чем у женщин.
Сообщалось о мутационном профиле рака головы и шеи, положительного и отрицательного на ВПЧ, что дополнительно демонстрирует, что они являются фундаментально разными заболеваниями.
Некоторые данные связывают ВПЧ с доброкачественными и злокачественными опухолями верхних дыхательных путей. Международное агентство по изучению рака обнаружило, что у людей с раком легких значительно больше шансов иметь несколько форм антител к ВПЧ с высоким риском, чем у людей, не страдающих раком легких. Исследователи, которые искали ВПЧ среди 1633 пациентов с раком легких и 2729 человек без заболевания легких, обнаружили, что у людей с раком легких было больше типов ВПЧ, чем у пациентов без рака, а среди пациентов с раком легких шансы иметь восемь типов серьезного ВПЧ были значительно выше.. Кроме того, экспрессия структурных белков ВПЧ с помощью иммуногистохимии и исследований in vitro позволяет предположить наличие ВПЧ при раке бронхов и его предшественниках. Другое исследование обнаружило ВПЧ в EBC, бронхиальной чистке и опухолевой ткани легких в случаях, и обнаружило наличие инфекции ВПЧ у 16,4% субъектов, пораженных немелкоклеточным раком легкого, но ни у одного из контрольных. Сообщенные средние частоты HPV при раке легких составляли 17% и 15% в Европе и Америке, соответственно, а среднее количество HPV в образцах азиатского рака легкого составляло 35,7%, при значительной неоднородности между некоторыми странами и регионами.
В очень редких случаях ВПЧ может вызывать бородавчатую эпидермодисплазию (ЭВ) у людей с ослабленной иммунной системой. Вирус, не иммунной системы, приводит к перепроизводству кератина на клетки кожи, что приводит к патологическим изменениям, напоминающих бородавки или кожного рога, которые могут в конечном итоге превратить в рак кожи, но развитие не очень хорошо понял. Специфические типы ВПЧ, связанные с ЭВ, - это ВПЧ5, ВПЧ8 и ВПЧ14.
ВПЧ, передающийся половым путем, делится на две категории: ВПЧ низкого и высокого риска. ВПЧ низкого риска вызывают появление бородавок на гениталиях или вокруг них. Типы 6 и 11 вызывают 90% всех остроконечных кондилом и рецидивирующего респираторного папилломатоза, который вызывает доброкачественные опухоли в дыхательных путях. ВПЧ высокого риска вызывают рак и состоят примерно из дюжины идентифицированных типов. Типы 16 и 18 ответственны за большинство случаев рака, вызванного ВПЧ. Эти ВПЧ высокого риска вызывают 5% случаев рака в мире. В Соединенных Штатах ВПЧ высокого риска вызывают 3% всех случаев рака у женщин и 2% у мужчин.
Факторы риска стойких половых инфекций ВПЧ, повышающих риск развития рака, включают ранний возраст первого полового акта, наличие нескольких партнеров, курение и подавление иммунитета. Генитальный ВПЧ распространяется при постоянном прямом контакте кожа к коже, при этом наиболее распространенными методами являются вагинальный, анальный и оральный секс. Иногда он может передаваться от матери к ее ребенку во время беременности. ВПЧ трудно удалить с помощью стандартных методов дезинфекции в больницах, и он может передаваться в медицинских учреждениях через многоразовое гинекологическое оборудование, такое как вагинальные ультразвуковые датчики. Период передачи инфекции все еще неизвестен, но, вероятно, по крайней мере до тех пор, пока сохраняются видимые поражения ВПЧ. ВПЧ может передаваться даже после лечения поражений, которые больше не видны и не присутствуют.
Хотя генитальные типы ВПЧ могут передаваться от матери к ребенку во время родов, заболевания, связанные с генитальным ВПЧ, у новорожденных возникают редко. Однако отсутствие внешнего вида не исключает наличия бессимптомной скрытой инфекции, поскольку вирус доказал свою способность скрываться на протяжении десятилетий. Перинатальная передача ВПЧ 6 и 11 типов может привести к развитию рецидивирующего респираторного папилломатоза с ювенильным началом (JORRP). JORRP встречается очень редко, с частотой около 2 случаев на 100 000 детей в Соединенных Штатах. Хотя показатели JORRP значительно выше, если у женщины появляются остроконечные кондиломы во время родов, риск JORRP в таких случаях все же составляет менее 1%.
Генитальные инфекции ВПЧ передаются в первую очередь при контакте с гениталиями, анусом или ртом инфицированного полового партнера.
Из 120 известных вирусов папилломы человека 51 вид и три подтипа поражают слизистую оболочку половых органов. Пятнадцать классифицируются как типы высокого риска (16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 68, 73 и 82), три как вероятные группы высокого риска (26, 53 и 66), а двенадцать - с низким уровнем риска (6, 11, 40, 42, 43, 44, 54, 61, 70, 72, 81 и 89).
Презервативы не полностью защищают от вируса, потому что области вокруг гениталий, включая внутреннюю поверхность бедра, не покрыты, таким образом подвергая эти области коже инфицированного человека.
Исследования показали, что ВПЧ передается между руками и гениталиями одного и того же человека и половых партнеров. Эрнандес проверял гениталии и доминирующую руку каждого человека в двадцати пяти гетеросексуальных парах каждые два месяца в среднем в течение семи месяцев. Она нашла две пары, в которых гениталии мужчины заразили руку женщины ВПЧ с высоким риском, две - где ее рука инфицировала его гениталии, одну - где ее гениталии - его руку, две - в каждой, где он заразил свою руку, и она заразила свою руку. Руки не были основным источником передачи инфекции в этих двадцати пяти парах, но они имели большое значение.
Партридж сообщает, что кончики пальцев мужчин становились положительными на ВПЧ высокого риска более чем в половине случаев (26% за два года), чем их гениталии (48%). Винер сообщает, что 14% образцов кончиков пальцев у сексуально активных женщин были положительными.
Несексуальный контакт рук, кажется, играет незначительную роль или не играет никакой роли в передаче ВПЧ. В начале исследования Винер обнаружила, что все четырнадцать образцов пальцев девственницы отрицательны. В отдельном отчете о генитальной инфекции ВПЧ 1% девственниц (1 из 76), не имевших половых контактов, дали положительный результат на ВПЧ, в то время как 10% девственниц, сообщивших о непроникающих сексуальных контактах, были положительными (7 из 72).
Совместное использование возможно зараженных предметов, например бритв, может передавать ВПЧ. Хотя это возможно, передача вируса папилломы человека другими путями, кроме полового акта, менее распространена для инфекции ВПЧ женских половых органов. Контакт между пальцами и гениталиями - возможный путь передачи, но вряд ли он будет значительным источником.
Хотя традиционно считалось, что ВПЧ не передается через кровь - поскольку считается, что он инфицирует только кожные и слизистые ткани, - недавние исследования поставили это понятие под сомнение. Исторически ДНК ВПЧ обнаруживалась в крови больных раком шейки матки. В 2005 году группа сообщила, что в образцах замороженной крови 57 педиатрических пациентов, ранее не имевших сексуального опыта, у которых была вертикальная или трансфузионная ВИЧ-инфекция, 8 (14,0%) из этих образцов также дали положительный результат на ВПЧ-16. Это, по-видимому, указывает на возможность передачи ВПЧ при переливании крови. Однако, поскольку передача ВПЧ другим путем не половым путем - не редкость, это не может быть окончательно доказано. В 2009 году группа исследователей проверила образцы крови Австралийского Красного Креста 180 здоровых мужчин-доноров на ВПЧ и впоследствии обнаружила ДНК одного или нескольких штаммов вируса в 15 (8,3%) образцов. Однако важно отметить, что обнаружение наличия ДНК ВПЧ в крови - это не то же самое, что обнаружение самого вируса в крови, и остается неизвестным, может ли сам вирус находиться в крови инфицированных людей или нет. Таким образом, еще предстоит определить, может ли ВПЧ передаваться через кровь. Это вызывает беспокойство, поскольку донорская кровь в настоящее время не проверяется на ВПЧ, и, по крайней мере, некоторые организации, такие как Американский Красный Крест и другие общества Красного Креста, в настоящее время, похоже, не запрещают ВПЧ-положительным людям сдавать кровь.
Передача ВПЧ в больницу, особенно хирургическому персоналу, была документально подтверждена. Хирурги, в том числе урологи и / или кто-либо из находящихся в палате, могут инфицироваться ВПЧ в результате вдыхания вредных вирусных частиц во время электрокаутеризации или лазерной абляции кондиломы (бородавки). Был случай, когда лазерный хирург развил обширный папилломатоз гортани после проведения лазерной абляции пациентам с аногенитальными кондиломами.
 Структура капсидного белка вируса папилломы человека типа 16, полученная методом криоэлектронной микроскопии. Вынесено из PDB : 5KEQ
Структура капсидного белка вируса папилломы человека типа 16, полученная методом криоэлектронной микроскопии. Вынесено из PDB : 5KEQ ВПЧ - инфекция ограничена базальные клетки из многослойного эпителия, только ткани, в которой они реплицировать. Вирус не может связываться с живой тканью; вместо этого он заражает эпителиальные ткани через микро-ссадины или другие эпителиальные травмы, обнажающие сегменты базальной мембраны. Инфекционный процесс протекает медленно, для инициации транскрипции требуется 12–24 часа. Считается, что вовлеченные антитела играют главную нейтрализующую роль, в то время как вирионы все еще находятся на базальной мембране и поверхностях клеток.
Считается, что поражения ВПЧ возникают в результате пролиферации инфицированных базальных кератиноцитов. Инфекция обычно происходит, когда базальные клетки хозяина подвергаются воздействию инфекционного вируса через нарушенный эпителиальный барьер, как это могло бы произойти во время полового акта или после незначительных ссадин кожи. ВПЧ - инфекция не была показана цитолитическими ; скорее, вирусные частицы высвобождаются в результате дегенерации слущивающихся клеток. ВПЧ может выжить в течение многих месяцев и при низких температурах без хозяина; Следовательно, человек с подошвенными бородавками может распространять вирус, ходя босиком.
ВПЧ представляет собой небольшой двухцепочечный кольцевой ДНК-вирус с геномом примерно из 8000 пар оснований. Жизненный цикл ВПЧ строго следует программе дифференциации кератиноцитов хозяина. Считается, что ВПЧ вириона заражает эпителиальной ткани через микро-ссадины, когда вириона ассоциируется с предполагаемыми рецепторами, такими как альфа - интегринов, ламининов и аннексина A2, ведущих к входу в вирионов в базальных эпителиальных клеток через клатрин - опосредованного эндоцитоза и / или кавеолин- опосредованный эндоцитоз в зависимости от типа ВПЧ. На этом этапе вирусный геном транспортируется в ядро неизвестными механизмами и устанавливается с числом копий 10-200 вирусных геномов на клетку. Затем происходит сложный транскрипционный каскад, когда кератиноциты хозяина начинают делиться и становиться все более дифференцированными в верхних слоях эпителия.
Филогения различных штаммов ВПЧ обычно отражает модели миграции Homo sapiens и предполагает, что ВПЧ, возможно, диверсифицировался вместе с человеческой популяцией. Исследования показывают, что ВПЧ эволюционировал по пяти основным ветвям, которые отражают этническую принадлежность человека-хозяина, и диверсифицировались вместе с человеческой популяцией. Исследователи определили два основных варианта HPV16: европейский (HPV16-E) и неевропейский (HPV16-NE).
 Показанная на рентгеновской кристаллографии структура онкобелка E6 HPV типа 16 (фиолетовый), связанный с пептидным мотивом LxxLL человеческого белка UBE3A (голубой). Отрисовано из PDB : 4GIZ.
Показанная на рентгеновской кристаллографии структура онкобелка E6 HPV типа 16 (фиолетовый), связанный с пептидным мотивом LxxLL человеческого белка UBE3A (голубой). Отрисовано из PDB : 4GIZ. Двумя основными онкобелками типов ВПЧ высокого риска являются E6 и E7. Обозначение «E» указывает на то, что эти два белка являются ранними белками (экспрессируются на ранней стадии жизненного цикла ВПЧ), тогда как обозначение «L» указывает на то, что они являются поздними белками (поздняя экспрессия). Геном HPV состоит из шести ранних (E1, E2, E4, E5, E6 и E7) открытых рамок считывания (ORF), двух поздних (L1 и L2) ORF и некодирующей длинной контрольной области (LCR). После инфицирования клетки-хозяина активируется ранний вирусный промотор и транскрибируется полицистронная первичная РНК, содержащая все шесть ранних открытых рамок считывания. Затем эта полицистронная РНК подвергается активному сплайсингу РНК с образованием множества изоформ мРНК. Одна из сплайсированных изоформ РНК, E6 * I, служит мРНК E7 для трансляции белка E7. Однако ранняя транскрипция вируса подвергается вирусной регуляции E2, и высокие уровни E2 репрессируют транскрипцию. Геномы HPV интегрируются в геном хозяина за счет разрушения ORF E2, предотвращая репрессию E2 на E6 и E7. Таким образом, интеграция вирусного генома в геном ДНК хозяина увеличивает экспрессию E6 и E7, способствуя пролиферации клеток и вероятности злокачественных новообразований. Степень экспрессии E6 и E7 коррелирует с типом поражения шейки матки, которое в конечном итоге может развиться.
Белки E6 / E7 инактивируют два белка-супрессора опухолей, p53 (инактивированный E6) и pRb (инактивированный E7). Считается, что вирусные онкогены E6 и E7 модифицируют клеточный цикл таким образом, чтобы поддерживать дифференцирующийся кератиноцит хозяина в состоянии, благоприятном для усиления репликации вирусного генома и, как следствие, поздней экспрессии генов. E6 в сочетании с E6-ассоциированным белком хозяина, который обладает активностью убиквитинлигазы, действует, чтобы убиквитинат p53, что приводит к его протеосомной деградации. Е7 (в онкогенных ВПЧ) действует как первичный трансформирующий белок. E7 конкурирует за связывание с белком ретинобластомы (pRb), освобождая фактор транскрипции E2F для трансактивации его мишеней, тем самым продвигая клеточный цикл вперед. Все ВПЧ могут вызывать временную пролиферацию, но только штаммы 16 и 18 могут иммортализовать клеточные линии in vitro. Также было показано, что ВПЧ 16 и 18 не могут увековечивать только первичные клетки крысы ; необходима активация онкогена ras. В верхних слоях эпителия хозяина поздние гены L1 и L2 транскрибируются / транслируются и служат в качестве структурных белков, которые инкапсидируют амплифицированные вирусные геномы. Как только геном инкапсидируется, капсид, по-видимому, подвергается окислительно-восстановительному процессу сборки / созревания, который связан с естественным окислительно-восстановительным градиентом, который охватывает как надбазальные, так и ороговевшие слои эпителиальной ткани. Это событие сборки / созревания стабилизирует вирионы и увеличивает их специфическую инфекционность. Затем вирионы могут быть отделены от мертвых чешуек эпителия хозяина, и жизненный цикл вируса продолжается. Исследование 2010 года показало, что E6 и E7 участвуют в накоплении бета-катенина в ядре и активации передачи сигналов Wnt при HPV-индуцированном раке.
Как только вирион ВПЧ проникает в клетку, происходит активная инфекция, и вирус может передаваться. Может пройти от нескольких месяцев до лет, прежде чем плоскоклеточные интраэпителиальные поражения (SIL) разовьются и могут быть обнаружены клинически. Время от активной инфекции до клинически обнаруживаемого заболевания может затруднить для эпидемиологов определение того, какой партнер был источником инфекции.
Большинство людей излечиваются от ВПЧ без каких-либо медицинских действий или последствий. В таблице представлены данные для типов высокого риска (т. Е. Типов, обнаруженных при раке).
| Месяцы после первоначального положительного теста | 8 месяцев | 12 месяцев | 18 месяцев |
|---|---|---|---|
| % мужчин дали отрицательный результат | 70% | 80% | 100% |
Устранение инфекции не всегда создает иммунитет при появлении нового или продолжающегося источника инфекции. В исследовании Hernandez 2005-6, проведенном с участием 25 пар, сообщается: «В ряде случаев была указана очевидная реинфекция [от партнера] после избавления от вируса».
 Известные типы ВПЧ и связанные с ними заболевания
Известные типы ВПЧ и связанные с ними заболевания Выявлено более 170 типов ВПЧ, обозначенных цифрами. Их можно разделить на типы «низкого риска» и «высокого риска». Типы низкого риска вызывают бородавки, а типы высокого риска могут вызывать поражения или рак.
В рекомендациях Американского онкологического общества рекомендуются различные стратегии скрининга рака шейки матки в зависимости от возраста женщины, истории обследования, факторов риска и выбора тестов. Из-за связи между ВПЧ и раком шейки матки ACS в настоящее время рекомендует раннее выявление рака шейки матки у бессимптомных взрослых со средним риском, в первую очередь, с помощью цитологического исследования шейки матки с помощью мазка Папаниколау, независимо от статуса вакцинации против ВПЧ. Женщин в возрасте 30–65 лет желательно сдавать каждые 5 лет как с помощью теста на ВПЧ, так и с помощью мазка Папаниколау. В других возрастных группах одного теста Папаниколау может быть достаточно, если у них не диагностированы атипичные плоскоклеточные клетки неопределенного значения (ASC-US). Рекомендуется совместное тестирование с Пап-тестом и тестом на ВПЧ, поскольку это снижает количество ложноотрицательных результатов. По данным Национального института рака: «Самый распространенный тест выявляет ДНК нескольких типов ВПЧ высокого риска, но не может определить присутствующие типы. Другой тест специфичен для ДНК ВПЧ типов 16 и 18, двух типов, вызывающих Большинство раковых заболеваний, связанных с ВПЧ. Третий тест может выявить ДНК нескольких типов ВПЧ высокого риска и указать, присутствует ли ВПЧ-16 или ВПЧ-18. Четвертый тест выявляет РНК из наиболее распространенных типов ВПЧ высокого риска. Эти тесты может обнаружить инфекции ВПЧ до того, как станут очевидными клеточные аномалии.
«Теоретически тесты ДНК и РНК ВПЧ могут быть использованы для выявления инфекций ВПЧ в клетках, взятых из любой части тела. Однако эти тесты одобрены FDA только для двух показаний: для последующего тестирования женщин, которые, по всей видимости, имеют ненормальные результаты мазка Папаниколау и для скрининга рака шейки матки в сочетании с тестом Папаниколау среди женщин старше 30 лет ».
Рекомендации по скринингу на рак ротоглотки, разработанные Целевой группой профилактических услуг и Американской стоматологической ассоциацией в США, предлагают традиционный визуальный осмотр, но поскольку некоторые части ротоглотки трудно увидеть, этот рак часто обнаруживается только на более поздних стадиях.
Диагноз рака ротоглотки ставится при биопсии слущенных клеток или тканей. National Comprehensive Cancer Network и Колледж американских патологов рекомендуют тестирование на ВПЧ рака ротоглотки. Тем не менее, хотя тестирование рекомендуется, не существует определенного типа теста, используемого для обнаружения ВПЧ в опухолях полости рта, который в настоящее время рекомендован FDA в Соединенных Штатах. Поскольку ВПЧ типа 16 является наиболее распространенным типом рака ротоглотки, иммуногистохимия p16 - это один из вариантов теста, используемый для определения наличия ВПЧ, который может помочь определить курс лечения, поскольку опухоли, отрицательные по p16, имеют лучшие результаты. Другой вариант, который появился как надежный вариант, - это гибридизация ДНК ВПЧ in situ (ISH), которая позволяет визуализировать ВПЧ.
Несмотря на то, что ВПЧ является обычным явлением, не существует большого количества доступных тестов; в большинстве исследований ВПЧ использовались инструменты и специальные анализы, недоступные широкой публике. Клиницисты часто полагаются на вакцину среди молодых людей и высокие показатели клиренса (см. Подраздел «Клиренс» в вирусологии), чтобы снизить риск заболевания и смертности и лечить раковые заболевания, когда они появляются. Другие считают, что снижение инфекции ВПЧ у большего числа мужчин и женщин, даже при отсутствии симптомов, важно (коллективный иммунитет) для предотвращения большего числа раковых заболеваний, а не просто для их лечения. Если используются тесты, отрицательные результаты тестов показывают безопасность от передачи, а положительные результаты тестов показывают, где необходима защита (презервативы, перчатки) для предотвращения передачи, пока инфекция не исчезнет.
Исследования проверили и обнаружили ВПЧ у мужчин, включая типы высокого риска (то есть типы, обнаруживаемые при раке), на пальцах, рту, слюне, анусе, уретре, моче, сперме, крови, мошонке и половом члене.
Набор Qiagen / Digene, упомянутый в предыдущем разделе, был успешно использован не по прямому назначению для тестирования полового члена, мошонки и ануса мужчин, состоящих в длительных отношениях с женщинами, которые были положительными на ВПЧ высокого риска. Было обнаружено, что 60% из них являются переносчиками вируса, в первую очередь, на половом члене. В других исследованиях использовались цитощетки и индивидуальный анализ.
В одном исследовании исследователи взяли образцы уретры, мошонки и полового члена. Образцы, взятые из уретры, добавляли менее 1% к уровню HPV. Подобные исследования побудили Джулиано рекомендовать забор образцов головки, вала и складки между ними, а также мошонки, поскольку забор образцов уретры или ануса очень мало помогал в диагностике. Данн рекомендует головку, стержень, их складку и крайнюю плоть.
В одном исследовании испытуемых просили не мыть половые органы в течение 12 часов перед взятием образцов, включая уретру, а также мошонку и половой член. В других исследованиях ничего не говорится о мытье - особом пробеле в исследованиях рук.
В одном небольшом исследовании использовались влажные цитощетки, а не кожа. Было обнаружено, что более высокая доля мужчин была ВПЧ-положительной, когда кожу протирали наждачной бумагой с зернистостью 600 перед тем, как протирать щеткой, а не протирать тампоном без подготовки. Неясно, собирала ли вирионы наждачная бумага или просто разрыхляла их для сбора тампоном.
Исследования показали, что самостоятельный забор (с помощью наждачной бумаги и дакроновых тампонов) столь же эффективен, как и сбор, проводимый клиницистом, а иногда даже более эффективен, поскольку пациенты были более склонны, чем клиницист, энергично выскабливать. Женщины добились аналогичных успехов при самостоятельном взятии проб с использованием тампонов, тампонов, цитобисток и лаважа.
В нескольких исследованиях использовались цитощетки для взятия образцов с кончиков пальцев и под ногтями, не смачивая область или кисть.
В других исследованиях анализировалась моча, сперма и кровь, и было обнаружено различное количество ВПЧ, но пока нет общедоступного теста для них.
Хотя можно проверить ДНК ВПЧ при других видах инфекций, в Соединенных Штатах нет утвержденных FDA тестов для общего скрининга или тестов, одобренных канадским правительством, поскольку тестирование неубедительно и считается ненужным с медицинской точки зрения.
Остроконечные кондиломы являются единственным видимым признаком генитального ВПЧ низкого риска и могут быть идентифицированы при визуальном осмотре. Однако эти видимые наросты являются результатом неканцерогенных типов ВПЧ. Пятипроцентная уксусная кислота (уксус) используется для выявления как бородавок, так и плоскоклеточных очагов интраэпителиальной неоплазии (SIL) с ограниченным успехом, вызывая белый цвет аномальной ткани, но большинство врачей сочли этот метод полезным только на влажных участках, таких как женские гениталии. тракт. В настоящее время тесты на ВПЧ для мужчин используются только в исследовательских целях.
Были проведены исследования по тестированию на ВПЧ по наличию антител. Подход ищет иммунный ответ в крови, который будет содержать антитела к ВПЧ, если пациент является ВПЧ-положительным. Надежность таких тестов не была доказана, поскольку по состоянию на август 2018 года не было одобренного FDA продукта; анализ крови был бы менее инвазивным тестом для скрининговых целей.
В вакцины против ВПЧ может предотвратить наиболее распространенные типы инфекции. Чтобы они были эффективными, их необходимо использовать до того, как возникнет инфекция, и поэтому они рекомендуются в возрасте от девяти до тринадцати лет. Скрининг на рак шейки матки, например, с помощью теста Папаниколау (pap) или осмотра шейки матки после использования уксусной кислоты, может обнаружить ранний рак или аномальные клетки, которые могут перерасти в рак. Это позволяет начать лечение на ранней стадии, что приводит к лучшим результатам. Скрининг снизил как количество, так и смертность от рака шейки матки в развитых странах. Бородавки можно удалить замораживанием.
Для предотвращения заражения некоторыми типами ВПЧ доступны три вакцины: Гардасил, Гардасил 9 и Церварикс ; все три защищают от первоначального заражения типами ВПЧ 16 и 18, которые вызывают большинство случаев рака, ассоциированного с ВПЧ. Гардасил также защищает от ВПЧ 6 и 11 типов, которые вызывают 90% остроконечных кондилом. Гардасил - это рекомбинантная четырехвалентная вакцина, тогда как Церварикс - двухвалентная вакцина, которую получают из вирусоподобных частиц (VLP) капсидного белка L1. Гардасил 9 не является валентным, он способен предотвращать около 90% случаев рака шейки матки, вульвы, влагалища и анального канала. Он может защитить от ВПЧ типов 6, 11, 16, 18, 31, 33, 45, 52 и 58; последние пять вызывают до 20% случаев рака шейки матки, которые ранее не покрывались.
Вакцины приносят мало пользы женщинам, уже инфицированным ВПЧ типов 16 и 18. По этой причине вакцина рекомендуется в первую очередь тем женщинам, которые еще не контактировали с ВПЧ во время полового акта. В документе с изложением позиции Всемирной организации здравоохранения по вакцинации против ВПЧ четко изложены соответствующие экономически эффективные стратегии использования вакцины против ВПЧ в программах государственного сектора.
Имеются достоверные доказательства того, что вакцины против ВПЧ защищают от предраковых поражений шейки матки у молодых женщин, особенно вакцинированных в возрасте от 15 до 26 лет. Вакцины против ВПЧ не повышают риск серьезных побочных эффектов. Для мониторинга воздействия вакцин против ВПЧ на рак шейки матки необходимо более длительное наблюдение.
CDC рекомендует вводить вакцину двумя прививками с интервалом не менее 6 месяцев для детей в возрасте 11–12 лет и тремя дозами для лиц 13 лет и старше. В большинстве стран они финансируются только для использования женщинами, но во многих странах разрешены для использования мужчинами, а в Австралии они финансируются для мальчиков-подростков. Вакцина не оказывает терапевтического действия на существующие инфекции ВПЧ или поражения шейки матки. В 2010 году 49% девочек-подростков в США получили вакцину против ВПЧ.
После исследований, показывающих, что вакцина более эффективна для девочек младшего возраста, чем для подростков старшего возраста, в 2014 году в Великобритании, Швейцарии, Мексике, Нидерландах и Квебеке вакцина была введена в виде двухдозовой схемы для девочек в возрасте до 15 лет.
Рекомендации по скринингу на рак шейки матки для женщин, получающих вакцину против ВПЧ, не изменились. Женщинам по-прежнему рекомендуется продолжать скрининг шейки матки, например мазок Папаниколау, даже после вакцинации, поскольку он не предотвращает все типы рака шейки матки.
И мужчины, и женщины являются носителями ВПЧ. Вакцина Гардасил также защищает мужчин от рака заднего прохода, бородавок и остроконечных кондилом.
Продолжительность действия обеих вакцин наблюдалась с момента их первой разработки, и ожидается, что она будет длительной.
В декабре 2014 года FDA одобрило девятивалентную вакцину на основе гардасила, Гардасил 9, для защиты от заражения четырьмя штаммами ВПЧ, покрываемыми гардасилом первого поколения, а также пятью другими штаммами, ответственными за 20% случаев рака шейки матки ( ВПЧ-31, ВПЧ-33, ВПЧ-45, ВПЧ-52 и ВПЧ-58).
В Центрах по контролю и профилактике заболеваний говорят, что мужчина « Презерватив использование может снизить риск для полового вируса папилломы человека (ВПЧ) инфекции», но обеспечивает меньшую степень защиты по сравнению с другими венерическими заболеваниями «, поскольку ВПЧ также может быть передано под воздействием областей (например, инфицированная кожа или поверхности слизистых оболочек), которые не закрыты или не защищены презервативом ».
Вирус необычайно устойчив и невосприимчив к большинству дезинфицирующих средств. Это первый вирус, устойчивый к инактивации глутаральдегидом, который является одним из наиболее распространенных сильнодействующих дезинфицирующих средств, используемых в больницах. Разбавленный отбеливатель гипохлорита натрия эффективен, но не может использоваться на некоторых типах многоразового оборудования, например, ультразвуковых преобразователях. В результате этих трудностей растет беспокойство по поводу возможности передачи вируса через медицинское оборудование, особенно многоразовое гинекологическое оборудование, которое нельзя автоклавировать. Для такого оборудования некоторые органы здравоохранения рекомендуют использовать УФ-дезинфекцию или негипохлоритные «дезинфицирующие средства высокого уровня [отбеливатель] на окислительной основе с указанием на этикетке вирусов без оболочки», например, концентрированный раствор перекиси водорода или салфетки из диоксида хлора. Ожидается, что такие методы дезинфекции будут относительно эффективными против ВПЧ.
В настоящее время не существует специального лечения инфекции ВПЧ. Однако вирусная инфекция обычно устраняется иммунной системой до неопределяемого уровня. По данным Центров по контролю и профилактике заболеваний, иммунная система организма избавляется от ВПЧ естественным путем в течение двух лет в 90% случаев (более подробную информацию см. В подразделе «Очистка» в вирусологии). Однако эксперты не согласны с тем, полностью ли уничтожен вирус или снижен до неопределяемого уровня, и трудно определить, когда он заразен.
Последующее наблюдение обычно рекомендуется и практикуется во многих клиниках. Последующее наблюдение иногда бывает безуспешным, потому что часть пролеченных не возвращается для оценки. В дополнение к обычным методам телефонных звонков и почты, текстовые сообщения и электронная почта могут увеличить количество людей, которые возвращаются за медицинской помощью. По состоянию на 2015 г. неясно, каков наилучший метод наблюдения после лечения интраэпителиальной неоплазии шейки матки.
Во всем мире 12% женщин имеют положительный результат на ДНК ВПЧ, причем показатели варьируются в зависимости от возраста и страны. Самые высокие показатели ВПЧ наблюдаются у молодых женщин, с показателем 24% у женщин в возрасте до 25 лет. Ставки снижаются в старших возрастных группах в Европе и Америке, но в меньшей степени в Африке и Азии. Эти показатели наиболее высоки в Африке к югу от Сахары (24%) и Восточной Европе (21%), а самые низкие - в Северной Америке (5%) и Западной Азии (2%).
Наиболее распространенными типами ВПЧ во всем мире являются ВПЧ16 (3,2%), ВПЧ18 (1,4%), ВПЧ52 (0,9%), ВПЧ31 (0,8%) и ВПЧ58 (0,7%). Типы ВПЧ высокого риска также распределены неравномерно: уровень ВПЧ16 составляет около 13% в Африке и 30% в Западной и Центральной Азии.
Подобно многим заболеваниям, ВПЧ непропорционально поражает страны с низким уровнем дохода и бедными ресурсами. Например, более высокие уровни ВПЧ в Африке к югу от Сахары могут быть связаны с высоким уровнем воздействия вируса иммунодефицита человека (ВИЧ) в этом регионе. Другими факторами, влияющими на глобальное распространение болезней, являются сексуальное поведение, включая возраст начала половой жизни, количество половых партнеров и легкость доступа к барьерным противозачаточным средствам, которые варьируются в глобальном масштабе.
| Возраст (лет) | Распространенность (%) |
|---|---|
| С 14 до 19 | 24,5% |
| 20–24 | 44,8% |
| 25–29 | 27,4% |
| От 30 до 39 | 27,5% |
| От 40 до 49 | 25,2% |
| От 50 до 59 | 19,6% |
| 14–59 | 26,8% |
ВПЧ считается наиболее распространенной инфекцией, передаваемой половым путем в Соединенных Штатах. Большинство сексуально активных мужчин и женщин, вероятно, в какой-то момент своей жизни заразятся генитальным ВПЧ. По оценкам Американской ассоциации социального здоровья, около 75–80% сексуально активных американцев будут инфицированы ВПЧ в какой-то момент своей жизни. К 50 годам более 80% американских женщин заразятся хотя бы одним штаммом генитального ВПЧ. Было подсчитано, что в 2000 г. было около 6,2 миллиона новых случаев инфицирования ВПЧ среди американцев в возрасте 15–44 лет; из них, по оценкам, 74% приходятся на людей в возрасте от 15 до 24 лет. Из изученных ЗППП генитальный ВПЧ был наиболее распространенным. В Соединенных Штатах, по оценкам, 10% населения имеют активную инфекцию ВПЧ, 4% имеют инфекцию, вызвавшую цитологические аномалии, и еще 1% имеют инфекцию, вызывающую генитальные бородавки.
Оценки распространенности ВПЧ варьируются от 14% до более 90%. Одна из причин такого различия заключается в том, что в некоторых исследованиях сообщается о женщинах, у которых в настоящее время обнаруживается инфекция, в то время как в других исследованиях сообщается о женщинах, у которых когда-либо была обнаруживаемая инфекция. Другая причина несоответствия - разница в штаммах, на которые проводилось тестирование.
Одно исследование показало, что в течение 2003–2004 годов в любой момент времени 26,8% женщин в возрасте от 14 до 59 были инфицированы по крайней мере одним типом ВПЧ. Это было выше, чем предыдущие оценки; 15,2% были инфицированы одним или несколькими типами высокого риска, которые могут вызвать рак.
Распространенность типов высокого и низкого риска примерно одинакова с течением времени.
Вирус папилломы человека не входит в число заболеваний, которые обычно передаются в CDC с 2011 года.
В период с 2010 по 2014 год в Ирландии ежегодно диагностировалось в среднем 538 случаев рака, связанных с ВПЧ. Рак шейки матки был наиболее частым раком, связанным с ВПЧ, и в среднем составлял 292 случая в год (74% от общего числа женщин и 54% от общего количества раковых заболеваний, связанных с ВПЧ). Изучение 996 образцов цитологии шейки матки у городской женщины ирландского происхождения, прошедшей оппортунистический скрининг, показало, что общая распространенность ВПЧ составляет 19,8%, ВПЧ 16 - 20% и ВПЧ 18 - 12% - наиболее частые выявленные типы высокого риска. В Европе типы 16 и 18 вызывают более 70% случаев рака шейки матки. Общие показатели инвазивного рака, связанного с ВПЧ, могут увеличиваться. В период с 1994 по 2014 год частота инвазивных раковых заболеваний, связанных с ВПЧ, увеличивалась на 2% в год для обоих полов в Ирландии.
Поскольку известно, что ВПЧ связан с аногенитальными бородавками, они подлежат уведомлению в Центр наблюдения за охраной здоровья (HPSC). Остроконечные кондиломы - вторая по распространенности ИППП в Ирландии. В 2017 году было зарегистрировано 1281 случай аногенитальных бородавок, что меньше 1593 случая 2016 года. Самый высокий повозрастной коэффициент как для мужчин, так и для женщин был в возрастном диапазоне 25-29 лет, 53% случаев были среди мужчин.
В Шри-Ланке распространенность ВПЧ составляет 15,5% независимо от их цитологических аномалий.
В 1972 году Стефания Яблоньска из Польши предложила ассоциацию вирусов папилломы человека с раком кожи при бородавчатой эпидермодисплазии. В 1978 году Яблоньска и Жерар Орт из Института Пастера обнаружили ВПЧ-5 при раке кожи. В 1976 году Харальд цур Хаузен опубликовал гипотезу о том, что вирус папилломы человека играет важную роль в возникновении рака шейки матки. В 1983 и 1984 годах Цур Хаузен и его сотрудники идентифицировали HPV16 и HPV18 при раке шейки матки.
HeLa линия клеток содержит дополнительную ДНК в своем геноме, которые произошли от типа ВПЧ 18.
Ludwig-McGill ВПЧ когорта является одним из крупнейших в мире продольных исследований естественной истории папилломы человека (ВПЧ) и рак шейки матки риска. Он был основан в 1993 году отделом исследования рака Людвига и Университетом Макгилла в Монреале, Канада.
| Классификация | D |
|---|---|
| Внешние ресурсы |