| Гемодиализ | |
|---|---|
 Аппарат для гемодиализа Аппарат для гемодиализа | |
| Другие названия | диализ почек |
| Специальность | нефрология |
| [редактировать в Викиданных ] | |
Гемодиализ, также пишется гемодиализ или просто диализ, это процесс очищения крови человека, почки которого не работают нормально. Этот тип диализа обеспечивает экстракорпоральное удаление продуктов жизнедеятельности, таких как креатинин и мочевина, и свободной воды из крови, когда почки в состоянии почечная недостаточность. Гемодиализ является одним из трех методов заместительной почечной терапии (два других - трансплантация почки и перитонеальный диализ ). Альтернативным методом экстракорпорального разделения компонентов крови, таких как плазма или клетки, является аферез.
Гемодиализ может быть амбулаторным или стационарным лечением. Регулярный гемодиализ проводится в амбулаторном отделении диализа, либо в специально построенном помещении в больнице, либо в отдельной отдельной клинике. Реже гемодиализ проводят в на дому. Процедуры диализа в клинике инициируются и управляются специализированным персоналом, состоящим из медсестер и техников; Лечение диализа в домашних условиях можно инициировать самостоятельно и управлять им или проводить совместно с помощью обученного помощника, который обычно является членом семьи.
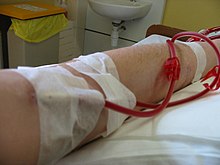 Гемодиализ в прогресс
Гемодиализ в прогресс Гемодиализ i s выбор заместительной почечной терапии для пациентов, остро нуждающихся в диализе, и для многих пациентов в качестве поддерживающей терапии. Он обеспечивает отличное и быстрое выведение растворенных веществ.
A нефролог (медицинский специалист по почкам) решает, когда необходим гемодиализ и различные параметры диализного лечения. К ним относятся частота (количество процедур в неделю), продолжительность каждой процедуры, скорость потока крови и диализного раствора, а также размер диализатора. Состав диализного раствора также иногда корректируется с точки зрения содержания в нем натрия, калия и бикарбоната. В целом, чем больше размер тела человека, тем больше ему потребуется диализа. В Северной Америке и Великобритании типично 3–4-часовой курс лечения (иногда до 5 часов для более крупных пациентов), проводимый 3 раза в неделю. Сеансы два раза в неделю предназначены только для пациентов со значительной остаточной функцией почек. Четыре сеанса в неделю часто назначают более крупным пациентам, а также пациентам, имеющим проблемы с перегрузкой жидкостью. Наконец, растет интерес к короткому ежедневному домашнему гемодиализу, который представляет собой 1,5–4-часовые сеансы, проводимые 5–7 раз в неделю, обычно дома. Также представляет интерес ночной диализ, который включает диализ пациента, обычно дома, в течение 8–10 часов в сутки, 3–6 ночей в неделю. Ночной диализ в центре, 3–4 раза в неделю, также предлагается в нескольких отделениях диализа в США.
Гемодиализ часто включает удаление жидкости (посредством ультрафильтрации ), поскольку большинство пациентов с почечной недостаточностью выделяют мало мочи или не выделяют ее совсем. Побочные эффекты, вызванные удалением слишком большого количества жидкости и / или слишком быстрым удалением жидкости, включают низкое кровяное давление, усталость, боли в груди, судороги ног, тошноту и головные боли. Эти симптомы могут возникать во время лечения и могут сохраняться после лечения; их иногда все вместе называют диализным похмельем или диализным смывом. Выраженность этих симптомов обычно пропорциональна количеству и скорости удаления жидкости. Однако влияние данного количества или скорости удаления жидкости может сильно варьироваться от человека к человеку и изо дня в день. Этих побочных эффектов можно избежать и / или уменьшить их тяжесть, ограничив потребление жидкости между курсами лечения или увеличив дозу диализа, например диализ чаще или дольше на курс лечения, чем стандартный, три раза в неделю, 3–4 часа на график лечения.
Поскольку для гемодиализа требуется доступ к системе кровообращения, пациенты, проходящие гемодиализ, могут подвергать свою кровеносную систему воздействию микробов, что может привести к бактериемии, инфекция, поражающая сердечные клапаны (эндокардит ) или инфекция, поражающая кости (остеомиелит ). Риск заражения зависит от типа используемого доступа (см. Ниже). Также может произойти кровотечение, риск опять же зависит от типа используемого доступа. Инфекции можно свести к минимуму, строго придерживаясь инфекционного контроля передовых методов.
Смещение венозной иглы (VND) является потенциально смертельным осложнением гемодиализа, когда пациент страдает быстрой кровопотерей из-за неустойчивого прикрепления иглы к точке венозного доступа.
Нефракционированный гепарин (УВЧ) является наиболее часто используемым антикоагулянтом при гемодиализе, поскольку он обычно хорошо переносится и его можно быстро восстановить с помощью сульфата протамина. Низкомолекулярный гепарин (НМГ), однако, становится все более популярным и в настоящее время является нормой в Западной Европе. По сравнению с УВЧ, НМГ имеет преимущество в более простом способе введения и уменьшении кровотечений, но этот эффект нельзя легко обратить. Гепарин нечасто может вызывать снижение количества тромбоцитов из-за реакции, называемой гепарин-индуцированной тромбоцитопенией (HIT). У таких пациентов могут использоваться альтернативные антикоагулянты. Риск ГИТ ниже при НМГ по сравнению с УВЧ. Несмотря на то, что HIT вызывает низкое количество тромбоцитов, это парадоксальным образом может предрасполагать к тромбозу. У пациентов с высоким риском кровотечения диализ можно проводить без антикоагулянтов.
Синдром первого применения - редкая, но тяжелая анафилактическая реакция на искусственная почка. Его симптомы включают чихание, хрипы, одышку, боль в спине, боль в груди или внезапную смерть. Это может быть вызвано остаточным стерилизующим веществом в искусственной почке или материалом самой мембраны. В последние годы частота возникновения синдрома первого применения снизилась благодаря более широкому использованию гамма-облучения, стерилизации паром или электронно-лучевого излучения вместо химических стерилизаторов, а также разработки новых полупроницаемых мембран из более высокая биосовместимость. Всегда необходимо учитывать новые методы обработки ранее приемлемых компонентов диализа. Например, в 2008 году из-за заражения гепарина в процессе производства гиперсульфатированным хондроитинсульфатом.
долгосрочные осложнения гемодиализа произошла серия реакций первого типа, включая смертельные случаи. гемодиализ-связанный амилоидоз, невропатия и различные формы болезни сердца. Было показано, что увеличение частоты и продолжительности лечения уменьшает перегрузку жидкостью и увеличение сердца, что обычно наблюдается у таких пациентов. Из-за этих осложнений дополнительная и альтернативная медицина распространена среди пациентов, находящихся на гемодиализе.
Дефицит фолиевой кислоты может возникать у некоторых пациентов, находящихся на гемодиализе.
 Полупроницаемая мембрана
Полупроницаемая мембрана Принцип гемодиализа такой же, как и у других методов диализа ; он включает диффузию растворенных веществ через полупроницаемую мембрану. Гемодиализ использует противоточный поток, где диализат течет в направлении, противоположном кровотоку в экстракорпоральном контуре. Противоточный поток поддерживает максимальный градиент концентрации на мембране и увеличивает эффективность диализа.
Удаление жидкости (ультрафильтрация ) достигается путем изменения гидростатического давления камеры диализата, в результате чего свободная вода и некоторые растворенные вещества перемещаются через мембрану вдоль созданного градиент давления.
Используемый диализный раствор может быть стерилизованным раствором минеральных ионов. Мочевина и другие отходы, калий и фосфат диффундируют в диализный раствор. Однако концентрации натрия и хлорида аналогичны концентрациям в нормальной плазме, чтобы предотвратить потерю. Бикарбонат натрия добавляется в более высокой концентрации, чем плазма, для коррекции кислотности крови. Также обычно используется небольшое количество глюкозы.
Обратите внимание, что это другой процесс, чем связанный метод гемофильтрации.
Для получения доступа к крови для гемодиализа используются три основных метода: внутривенный катетер, артериовенозный свищ (AV) и синтетический трансплантат. На тип доступа влияют такие факторы, как ожидаемое время почечной недостаточности пациента и состояние его сосудистой сети. Пациентам могут быть назначены процедуры множественного доступа, обычно из-за созревания атриовентрикулярного свища или трансплантата, а катетер все еще используется. Катетер обычно устанавливается под легким седативным действием, тогда как при свищах и трансплантатах требуется операция.
 Permacath для диализа
Permacath для диализа Существует три типа гемодиализа: обычный гемодиализ, ежедневный гемодиализ и ночной гемодиализ. Ниже приводится адаптация и краткое изложение брошюры Оттавской больницы.
Обычный гемодиализ обычно проводится три раза в неделю, примерно по три-четыре часа для каждой процедуры (иногда по пять часов для более крупных пациентов), в течение которых у пациента берется кровь через трубку со скоростью 200–400 мл / мин. Трубка подсоединяется к игле калибра 15, 16 или 17, вставленной в диализный свищ или трансплантат, или подсоединяется к одному порту диализного катетера. Затем кровь прокачивается через диализатор, а затем обработанная кровь закачивается обратно в кровоток пациента через другую трубку (подключенную ко второй игле или порту). Во время процедуры тщательно контролируется артериальное давление пациента, и если оно становится низким или у пациента появляются какие-либо другие признаки низкого объема крови, такие как тошнота, специалист по диализу может ввести дополнительную жидкость через аппарат. Во время лечения весь объем крови пациента (около 5000 см3) циркулирует через аппарат каждые 15 минут. Во время этого процесса диализный пациент получает недельный объем воды для обычного человека.
Ежедневный гемодиализ обычно используется теми пациентами, которые проводят диализ самостоятельно дома. Он менее стрессовый (более щадящий), но требует более частого доступа. Это просто с катетерами, но более проблематично со свищами или трансплантатами. «Техника петли» может использоваться при свищах, требующих частого доступа. Ежедневный гемодиализ обычно проводится по 2 часа шесть дней в неделю.
Процедура ночного гемодиализа аналогична обычному гемодиализу, за исключением того, что он проводится от трех до шести ночей в неделю и от шести до десяти часов за сеанс, пока пациент спит.
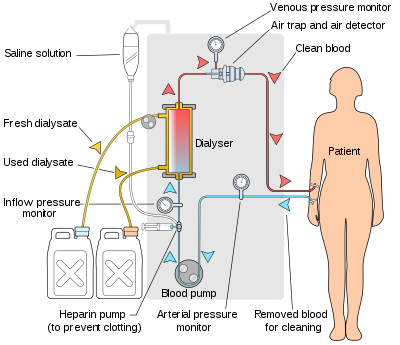 Схема гемодиализного контура
Схема гемодиализного контура Гемодиализный аппарат перекачивает кровь пациента и диализат через диализатор. Новейшие аппараты для диализа на рынке полностью компьютеризированы и непрерывно контролируют ряд критически важных для безопасности параметров, включая скорость потока крови и диализата; проводимость диализирующего раствора, температура и pH; и анализ диализата на предмет утечки крови или наличия воздуха. Любое показание, выходящее за пределы нормального диапазона, вызывает звуковой сигнал, чтобы предупредить техника по уходу за пациентом, который наблюдает за пациентом. Производителями диализных аппаратов являются такие компании, как Nipro, Fresenius, Gambro, Baxter, B. Браун, NxStage и Bellco.
 Емкости для диализатного раствора гемодиализного блока
Емкости для диализатного раствора гемодиализного блока Расширенная система очистки воды абсолютно необходима для гемодиализа. Поскольку пациенты на диализе подвергаются воздействию огромного количества воды, которая смешивается с концентратом диализата для образования диализата, даже следовые минеральные примеси или бактериальные эндотоксины могут проникать в кровь пациента. Поскольку поврежденные почки не могут выполнять предназначенную для них функцию удаления примесей, ионы, попавшие в кровоток через воду, могут накапливаться до опасного уровня, вызывая многочисленные симптомы или смерть. Алюминий, хлорамин, фторид, медь и цинк, а также бактериальные фрагменты и эндотоксины - все это вызывает проблемы в этом отношении.
По этой причине вода, используемая для гемодиализа, перед использованием тщательно очищается. Сначала его фильтруют, регулируют температуру и корректируют pH, добавляя кислоту или основание. Затем он размягчается. Затем вода проходит через резервуар, содержащий активированный уголь, для адсорбции органических загрязнителей. Затем осуществляется первичная очистка путем пропускания воды через мембрану с очень маленькими порами, так называемую мембрану обратного осмоса. Это позволяет воде проходить, но задерживает даже очень мелкие растворенные вещества, такие как электролиты. Окончательное удаление остатков электролитов осуществляется путем пропускания воды через резервуар с ионообменными смолами, которые удаляют любые оставшиеся анионы или катионы и заменяют их ионами гидроксила и водорода, соответственно, оставляя сверхчистую воду.
Даже такой степени очистки воды может быть недостаточно. В последнее время наблюдается тенденция пропускания этой очищенной воды (после смешивания с концентратом диализата) через мембрану диализатора. Это обеспечивает еще один уровень защиты за счет удаления примесей, особенно бактериального происхождения, которые могли накопиться в воде после ее прохождения через исходную систему очистки воды.
После смешивания очищенной воды с концентратом диализата ее проводимость увеличивается, поскольку вода, содержащая заряженные ионы, проводит электричество. Во время диализа проводимость диализирующего раствора постоянно контролируется, чтобы гарантировать, что вода и концентрат диализата смешиваются в надлежащих пропорциях. Как чрезмерно концентрированный диализный раствор, так и чрезмерно разбавленный раствор могут вызвать серьезные клинические проблемы.
Диализатор - это часть оборудования, которая фактически фильтрует кровь. Почти все используемые сегодня диализаторы изготовлены из полых волокон. Цилиндрический пучок полых волокон, стенки которых состоят из полупроницаемой мембраны, закреплен на каждом конце в заливочном компаунде (разновидность клея). Затем этот узел помещается в прозрачный пластиковый цилиндрический корпус с четырьмя отверстиями. Одно отверстие или отверстие для крови на каждом конце цилиндра сообщается с каждым концом пучка полых волокон. Это образует «кровяной отсек» диализатора. Два других порта прорезаны в боковой части цилиндра. Они сообщаются с пространством вокруг полых волокон, «отсеком для диализата». Кровь прокачивается через порты для крови через этот пучок очень тонких капиллярных -подобных трубок, а диализат прокачивается через пространство, окружающее волокна. При необходимости для перемещения жидкости из крови в отделение диализата применяются градиенты давления.
Мембраны диализатора бывают с разными размерами пор. Поры с меньшим размером пор называются «низкофлюсовыми», а частицы с большими размерами пор - «высокопоточными». Некоторые более крупные молекулы, такие как бета-2-микроглобулин, вообще не удаляются диализаторами с низким потоком; В последнее время появилась тенденция к использованию диализаторов с высокой плотностью потока. Однако для таких диализаторов требуются более новые диализные аппараты и высококачественный диализный раствор для надлежащего контроля скорости удаления жидкости и предотвращения обратного потока примесей диализирующего раствора в пациента через мембрану.
Мембраны диализатора раньше делались в основном из целлюлозы (полученной из хлопкового линта). Поверхность таких мембран не была очень биосовместимой, потому что открытые гидроксильные группы будут активировать комплемент в крови, проходящей через мембрану. Поэтому была модифицирована основная, «незамещенная» целлюлозная мембрана. Одно изменение заключалось в том, чтобы покрыть эти гидроксильные группы ацетатными группами (ацетат целлюлозы); другой - добавление некоторых соединений, которые ингибируют активацию комплемента на поверхности мембраны (модифицированная целлюлоза). Первоначальные мембраны из «незамещенной целлюлозы» больше не широко используются, тогда как диализаторы из ацетата целлюлозы и модифицированной целлюлозы все еще используются. Целлюлозные мембраны могут быть выполнены в конфигурации с низким или высоким потоком, в зависимости от размера их пор.
Другая группа мембран изготовлена из синтетических материалов с использованием полимеров, таких как полиарилэфирсульфон, полиамид, поливинилпирролидон, поликарбонат и полиакрилонитрил. Эти синтетические мембраны активируют комплемент в меньшей степени, чем незамещенные целлюлозные мембраны. Однако в целом они более гидрофобны, что приводит к усилению адсорбции белков на поверхности мембраны, что, в свою очередь, может привести к активации системы комплемента. Синтетические мембраны могут быть выполнены в конфигурации с низким или высоким потоком, но большинство из них обладают высокой проницаемостью.
Нанотехнология используется в некоторых из самых последних высокопроницаемых мембран для создания пор одинакового размера. Цель высокопроницаемых мембран - пропускать относительно большие молекулы, такие как бета-2-микроглобулин (молекулярная масса 11 600 дальтон), но не пропускать альбумин (молекулярная масса ~ 66 400 дальтон). Каждая мембрана имеет поры разного размера. По мере увеличения размера пор некоторые диализаторы с высоким потоком пропускают альбумин из крови в диализат. Это считается нежелательным, хотя одна школа мысли считает, что удаление некоторого количества альбумина может быть полезным с точки зрения удаления связанных с белками уремических токсинов.
Вопрос о том, улучшает ли использование диализатора с высоким потоком исходы для пациентов, является спорным, но несколько важных исследований показали, что он имеет клинические преимущества. В исследовании HEMO, финансируемом NIH, сравнивали выживаемость и госпитализацию пациентов, рандомизированных для диализа с мембранами с низким или высоким потоком. Хотя первичный результат (смертность от всех причин) не достиг статистической значимости в группе, рандомизированной для использования мембран с высокой проницаемостью, несколько вторичных результатов были лучше в группе с высокой проницаемостью. Недавний Кокрановский анализ показал, что польза выбора мембраны для исходов еще не продемонстрирована. Совместное рандомизированное исследование из Европы, исследование MPO (Membrane Permeabilities Outcomes), сравнивающее смертность пациентов, только начинающих диализ с использованием мембран с высокой или низкой проницаемостью, обнаружило незначительную тенденцию к повышению выживаемости у пациентов, использующих мембраны с высокой проницаемостью, и улучшение выживаемости у пациентов с более низким уровнем сывороточного альбумина или у диабетиков.
Диализные мембраны с высокой пропускной способностью и / или периодическая гемодиафильтрация в режиме онлайн (IHDF) также могут быть полезны для уменьшения осложнений, связанных с бета-2-микроглобулином накопление. Поскольку бета-2-микроглобулин представляет собой большую молекулу с молекулярной массой около 11 600 дальтон, он вообще не проходит через диализные мембраны с низким потоком. Бета-2-М удаляется диализом с высокой интенсивностью потока, но еще более эффективно удаляется с помощью IHDF. Спустя несколько лет (обычно не менее 5-7 лет) у пациентов, находящихся на гемодиализе, начинают развиваться осложнения, связанные с накоплением бета-2-М, включая синдром запястного канала, костные кисты и отложения этого амилоида в суставах и других тканях. Бета-2-М амилоидоз может вызывать очень серьезные осложнения, включая спондилоартропатию, и часто связан с проблемами плечевого сустава. Наблюдательные исследования, проведенные в Европе и Японии, показали, что использование мембран с высокой проницаемостью в режиме диализа, или IHDF, снижает осложнения с бета-2-М по сравнению с обычным диализом с использованием мембраны с низким потоком.
Диализаторы бывают разных размеров. Диализатор большего размера с большей площадью мембраны (A) обычно удаляет больше растворенных веществ, чем диализатор меньшего размера, особенно при высокой скорости кровотока. Это также зависит от коэффициента проницаемости мембраны K 0 для рассматриваемого растворенного вещества. Таким образом, эффективность диализатора обычно выражается как K 0 A - произведение коэффициента проницаемости и площади. Большинство диализаторов имеют площадь поверхности мембраны от 0,8 до 2,2 квадратных метров и значения K 0 A в диапазоне примерно от 500 до 1500 мл / мин. K 0 A, выраженный в мл / мин, можно рассматривать как максимальный клиренс диализатора при очень высоких расходах крови и диализата.
Диализатор можно либо выбросить после каждой обработки, либо использовать повторно. Повторное использование требует обширной процедуры дезинфекции высокого уровня. Повторно используемые диализаторы не используются совместно пациентами. Вначале возникли разногласия по поводу того, ухудшает ли повторное использование диализаторов результаты лечения пациентов. Сегодня единодушное мнение заключается в том, что повторное использование диализаторов, если оно выполняется осторожно и правильно, дает результаты, аналогичные одноразовому использованию диализаторов.
Повторное использование диализаторов - это практика, которая существует с момента изобретения продукта. Эта практика включает очистку бывшего в употреблении диализатора для многократного использования одним и тем же пациентом. Диализные клиники повторно используют диализаторы, чтобы стать более экономичными и снизить высокие затраты на «одноразовый» диализ, который может быть чрезвычайно дорогим и расточительным. Одноразовые диализаторы запускаются только один раз, а затем выбрасываются, образуя большое количество био- медицинских отходов, без какой-либо экономии средств. Если все сделано правильно, повторное использование диализатора может быть очень безопасным для диализных пациентов.
Есть два способа повторного использования диализаторов: ручной и автоматический. Ручное повторное использование подразумевает ручную очистку диализатора. Диализатор частично разбирается, затем несколько раз промывается перед ополаскиванием водой. Затем его хранят с жидким дезинфицирующим средством (PAA) в течение 18+ часов до следующего использования. Хотя многие клиники за пределами США используют этот метод, некоторые клиники переходят на более автоматизированный / рационализированный процесс по мере развития практики диализа. Новый метод автоматического повторного использования достигается с помощью медицинского устройства, которое появилось в начале 1980-х годов. Эти устройства полезны для диализных клиник, которые практикуют повторное использование, особенно для крупных диализных клинических учреждений, потому что они позволяют выполнять несколько циклов в день. Диализатор сначала предварительно очищается техническим специалистом, затем автоматически очищается машиной с помощью пошагового процесса, пока он в конечном итоге не будет заполнен жидким дезинфицирующим средством для хранения. Хотя автоматическое повторное использование более эффективно, чем повторное использование вручную, новые технологии позволили еще больше продвинуться в процессе повторного использования. При повторном использовании более 15 раз с текущей методологией диализатор может потерять B2m, клиренс средних молекул и целостность структуры пор волокна, что может снизить эффективность сеанса диализа пациента. В настоящее время, по состоянию на 2010 год, более новая, более совершенная технология переработки доказала способность полностью исключить ручной процесс предварительной очистки в целом, а также доказала способность регенерировать (полностью восстанавливать) все функции диализатора до уровней, которые приблизительно эквивалентны одноразового использования более 40 циклов. Поскольку ставки медицинского возмещения начинают еще больше падать, многие диализные клиники продолжают эффективно работать с программами повторного использования, тем более что этот процесс стал проще и оптимальнее, чем раньше.
Гемодиализ был одной из наиболее распространенных процедур, выполняемых в больницах США в 2011 году, при этом было совершено 909 000 госпитализаций (показатель 29 посещений на 10 000 населения). Это на 68 процентов больше, чем в 1997 году, когда было 473 000 остановок. Это пятая по частоте процедура для пациентов в возрасте 45–64 лет.
Многие сыграли роль в разработке диализа как практического метода лечения почечной недостаточности, начиная с Thomas Грэхем из Глазго, который впервые представил принципы транспорта растворенных веществ через полупроницаемую мембрану в 1854 году. Искусственная почка была впервые разработана Абелем, Раунтри и Тернером в 1913 году. первый гемодиализ для человека был проведен Хассом (28 февраля 1924 г.), а искусственная почка была разработана в клинически полезный аппарат Колффом в 1943-1945 гг. Это исследование показало, что жизнь могла быть продлена у пациентов, умирающих от почечной недостаточности.
Виллем Колфф был первым, кто сконструировал рабочий диализатор в 1943 году. Первым успешно пролеченным пациентом была 67-летняя женщина с уремией. кома, который пришел в сознание после 11 часов гемодиализа с диализатором Колффа в 1945 году. На момент его создания целью Колффа было для жизнеобеспечения во время восстановления после острой почечной недостаточности. После окончания Второй мировой войны Колфф пожертвовал пять сделанных им диализаторов больницам по всему миру, в том числе больницу Маунт-Синай, Нью-Йорк. Колфф передал комплект чертежей своего аппарата для гемодиализа Джорджу Торну в больницу Питера Бента Бригама в Бостоне. Это привело к производству диализатора Колффа следующего поколения, диализного аппарата Колффа-Бригама из нержавеющей стали .
Согласно Маккеллару (1999), значительный вклад в почечную терапию внес канадский хирург Гордон Мюррей с помощью двух врачей, студента-химика и научного персонала. Работа Мюррея проводилась одновременно и независимо от работы Колффа. Работа Мюррея привела к созданию первой успешной искусственной почки, построенной в Северной Америке в 1945–46 годах, которую успешно использовали для лечения 26-летней женщины из уремической комы в Торонто. Менее примитивный, более компактный диализатор второго поколения «Мюррей-Рошлау» был изобретен в 1952–53, конструкции которого были украдены немецким иммигрантом Эрвином Хальструпом и выданы как его собственные («Искусственная почка Хальструпа-Баумана»)..
К 1950-м годам изобретение Виллема Колффа диализатора использовалось для лечения острой почечной недостаточности, но не рассматривалось как эффективное лечение пациентов с хронической болезнью почек 5 стадии (ХБП).. В то время врачи считали, что пациенты не могут находиться на диализе бесконечно по двум причинам. Во-первых, они думали, что никакое искусственное устройство не сможет надолго заменить функцию почек. Кроме того, у пациента, находящегося на диализе, были повреждены вены и артерии, так что после нескольких сеансов лечения стало трудно найти сосуд для доступа к крови пациента.
Исходная почка Колффа не была очень полезной в клинической практике, потому что не позволяла удалять лишнюю жидкость. Шведский профессор Нильс Алвалл поместил модифицированную версию этой почки в контейнер из нержавеющей стали, к которому можно было приложить отрицательное давление, таким образом осуществив первое по-настоящему практическое применение гемодиализа, которое было осуществлено в 1946 г. Лундский университет. Алвалл также, возможно, был изобретателем артериовенозного шунта для диализа. Он впервые сообщил об этом в 1948 году, когда применил такой артериовенозный шунт у кроликов. Впоследствии он использовал такие шунты, сделанные из стекла, а также свой диализатор в контейнере, чтобы вылечить 1500 пациентов с почечной недостаточностью в период с 1946 по 1960 год, как было сообщено на Первом международном конгрессе нефрологов, состоявшемся в Эвиане в сентябре 1960 года. назначен на недавно созданную кафедру нефрологии в Лундском университете в 1957 году. Впоследствии он сотрудничал со шведским бизнесменом Хольгером Крафордом, чтобы основать одну из ключевых компаний, которая будет производить оборудование для диализа за последние 50 лет, Гамбро. Ранняя история диализа была рассмотрена Стэнли Шалдоном.
Белдинг Х. Скрибнер, работая с инженером-биомехаником Уэйном Куинтоном, модифицировал стеклянные шунты, используемые Элваллом, сделав их из Тефлон. Еще одним ключевым усовершенствованием было соединение их с коротким отрезком трубки из силиконового эластомера. Это легло в основу так называемого шунта Скрибнера, который, возможно, более правильно называть шунтом Куинтона-Скрибнера. После лечения доступ кровообращения будет оставаться открытым путем соединения двух трубок за пределами тела с помощью небольшой тефлоновой трубки U-образной формы, которая шунтирует кровь из трубки в артерии обратно в трубку в вене.
В 1962 году Скрибнер основал первое в мире амбулаторное диализное учреждение - Сиэтлский центр искусственной почек, позднее переименованный в Северо-западные центры почек. Сразу же возникла проблема, кому проводить диализ, поскольку спрос намного превышал возможности шести диализных аппаратов в центре. Скрибнер решил, что он не будет принимать решение о том, кто будет получать диализ, а кто нет. Вместо этого выбор будет сделан анонимным комитетом, который можно рассматривать как один из первых комитетов по биоэтике.
Подробную историю успешных и неудачных попыток диализа, в том числе таких пионеров, как Абель и Раундтри, Хаас и Нехелес, см. В обзоре Кьельстранда.
| Wikimedia Commons has media related to Hemodialysis. |