| Белок Hsp70 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
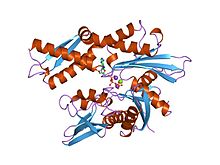 Структура фрагмента АТФазы 70К родственного белка теплового шока. Структура фрагмента АТФазы 70К родственного белка теплового шока. | |||||||||
| Идентификаторы | |||||||||
| Условное обозначение | HSP70 | ||||||||
| Pfam | PF00012 | ||||||||
| Клан пфам | CL0108 | ||||||||
| ИнтерПро | IPR013126 | ||||||||
| ПРОФИЛЬ | PDOC00269 | ||||||||
| SCOP2 | 3hsc / SCOPe / SUPFAM | ||||||||
| |||||||||
В 70 килодальтон белки теплового шока ( Hsp70 с или DnaK) представляют собой семейство из консервативных Повсеместно выраженных белков теплового шока. Белки с похожей структурой существуют практически во всех живых организмах. Внутриклеточно локализованные Hsp70 являются важной частью клеточного механизма сворачивания белков, выполнения функций шаперонирования и помощи в защите клеток от неблагоприятных эффектов физиологических стрессов. Кроме того, мембраносвязанные Hsp70 были идентифицированы как потенциальная мишень для лечения рака, а их внеклеточно локализованные аналоги были идентифицированы как имеющие как мембраносвязанные, так и безмембранные структуры.
Члены семейства Hsp70 очень сильно повышалась от теплового стресса и токсичных химических веществ, в частности, тяжелые металлы, такие как мышьяк, кадмий, медь, ртуть и т.д. Тепловой шок был первоначально обнаружен Ферруччо Ritossa в 1960 - е годы, когда работник лаборатории случайно увеличил инкубации температура дрозофилы (плодовых мушек). Изучая хромосомы, Ритосса обнаружил «паттерн вздутия», который указывал на повышенную транскрипцию гена неизвестного белка. Позже это было описано как «реакция теплового шока», а белки были названы «белками теплового шока» (Hsps).
 (а) Схематические домены Hsp70s. Hsp70s состоят из двух высококонсервативных функциональных доменов, включая NBD и C-концевой субстрат-связывающий домен (SBD), также мотив EEVD на C-конце. NBD содержит карман ATP / ADP, который связывается, а SBD содержит карман для связывания субстрата, который взаимодействует с протяженными полипептидами в качестве субстрата, α-спиральный субдомен с C-концевой стороны SBD образует гибкую крышку. EEVD-мотив участвует в связывании с ко-шаперонами и другими HSP. (b) полная аминокислотная последовательность человеческого Hsp70 (идентификатор UniProtKB: P0DMV8) как основного стресс-индуцируемого члена семейства Hsp70. (c) Вторичные структуры Hsp70 виртуализированы с помощью программного обеспечения VMD 1.9.1. Hsp70, белок теплового шока 70 кДа; NBD, N-концевой нуклеотид-связывающий домен; SBD, субстрат-связывающий домен на С-конце.
(а) Схематические домены Hsp70s. Hsp70s состоят из двух высококонсервативных функциональных доменов, включая NBD и C-концевой субстрат-связывающий домен (SBD), также мотив EEVD на C-конце. NBD содержит карман ATP / ADP, который связывается, а SBD содержит карман для связывания субстрата, который взаимодействует с протяженными полипептидами в качестве субстрата, α-спиральный субдомен с C-концевой стороны SBD образует гибкую крышку. EEVD-мотив участвует в связывании с ко-шаперонами и другими HSP. (b) полная аминокислотная последовательность человеческого Hsp70 (идентификатор UniProtKB: P0DMV8) как основного стресс-индуцируемого члена семейства Hsp70. (c) Вторичные структуры Hsp70 виртуализированы с помощью программного обеспечения VMD 1.9.1. Hsp70, белок теплового шока 70 кДа; NBD, N-концевой нуклеотид-связывающий домен; SBD, субстрат-связывающий домен на С-конце. Белки Hsp70 имеют три основных функциональных домена :
 Фосфорилирование изолированного серинового остатка протеинкиназой.
Фосфорилирование изолированного серинового остатка протеинкиназой. Фосфорилирование белка, посттрансляционная модификация, помогает регулировать функцию белка и включает фосфорилирование аминокислот с гидроксильными группами в их боковых цепях (у эукариот). Аминокислоты серина, треонина и тирозина являются обычными мишенями фосфорилирования. Фосфорилирование Hsp70 стало предметом более пристального изучения в научной литературе относительно недавно. Публикация 2020 года предполагает, что фосфорилирование серинового остатка между NBD и субстрат-связывающим доменом в дрожжевых Hsp70s приводит к резкому снижению нормального ответа на тепловой шок Hsp70. Эта дезактивация посредством фосфорилирования белка является обычным мотивом в регуляции белка и демонстрирует, как относительно небольшие изменения в структуре белка могут иметь биологически значимое влияние на функцию белка.
Система Hsp70 взаимодействует с протяженными пептидными сегментами белков, а также с частично свернутыми белками, вызывая агрегацию белков в ключевых путях для подавления активности. Когда Hsp70 не взаимодействует с пептидом-субстратом, он обычно находится в связанном с АТФ состоянии. Сам по себе Hsp70 характеризуется очень слабой АТФазной активностью, так что спонтанный гидролиз не происходит в течение многих минут. Когда вновь синтезированные белки выходят из рибосом, субстрат-связывающий домен Hsp70 распознает последовательности гидрофобных аминокислотных остатков и взаимодействует с ними. Это спонтанное взаимодействие обратимо, и в связанном с АТФ состоянии Hsp70 может относительно свободно связываться и высвобождать пептиды. Однако присутствие пептида в связывающем домене стимулирует АТФазную активность Hsp70, увеличивая его обычно медленную скорость гидролиза АТФ. Когда АТФ гидролизуется до АДФ, связывающий карман Hsp70 закрывается, прочно связывая теперь захваченную пептидную цепь. Еще больше ускоряют гидролиз АТФ так называемые коапероны J-домена: в первую очередь Hsp40 у эукариот и DnaJ у прокариот. Эти коапероны резко увеличивают АТФазную активность Hsp70 в присутствии взаимодействующих пептидов.
 Функция Hsp70 как в (ре) фолдинге, так и в деградации неправильно свернутого клиентского белка. (а) Схема цикла АТФ-АДФ Hsp70 для (ре) фолдинга клиентского белка, который вызывает конформационное изменение шаперона, гидролиз и обмен АТФ. (b) Комплекс Hsp70-CHIP, который способствует убиквитинизации клиентского белка и протеасомной деградации. CHIP взаимодействует с TPR-доменом Hsp70 и действует как убиквитин-лигаза для клиентов. ЧИП - иммунопреципитация хроматина; Hsp70, белок теплового шока 70 кДа; TPR, домен с повторением тетратрикопептида
Функция Hsp70 как в (ре) фолдинге, так и в деградации неправильно свернутого клиентского белка. (а) Схема цикла АТФ-АДФ Hsp70 для (ре) фолдинга клиентского белка, который вызывает конформационное изменение шаперона, гидролиз и обмен АТФ. (b) Комплекс Hsp70-CHIP, который способствует убиквитинизации клиентского белка и протеасомной деградации. CHIP взаимодействует с TPR-доменом Hsp70 и действует как убиквитин-лигаза для клиентов. ЧИП - иммунопреципитация хроматина; Hsp70, белок теплового шока 70 кДа; TPR, домен с повторением тетратрикопептида Путем связывания с частично синтезированными пептидными последовательностями (неполными белками) Hsp70 предотвращает их агрегацию и превращение в нефункциональные. Как только весь белок синтезируется, фактор обмена нуклеотидов ( среди идентифицированных прокариотических GrpE, эукариотических BAG1 и HspBP1 ) стимулирует высвобождение АДФ и связывание свежего АТФ, открывая карман связывания. Затем белок может сворачиваться самостоятельно или передаваться другим шаперонам для дальнейшей обработки. ХОП (The H SP70 / Hsp90 О rganizing Р rotein) может связываться с Hsp70 как и Hsp90 в то же время, и опосредует передачу пептидов из Hsp70 на Hsp90.
Hsp70 также помогает в трансмембранном транспорте белков, стабилизируя их в частично свернутом состоянии. Также известно, что он фосфорилируется, что регулирует несколько его функций.
Белки Hsp70 могут защищать клетки от теплового или окислительного стресса. Эти стрессы обычно приводят к повреждению белков, вызывая частичное разворачивание и возможную агрегацию. Временно связываясь с гидрофобными остатками, подверженными стрессу, Hsp70 предотвращает агрегацию этих частично денатурированных белков и препятствует их повторной укладке. Низкий уровень АТФ характерен для теплового шока, а устойчивое связывание рассматривается как подавление агрегации, в то время как восстановление после теплового шока включает связывание субстрата и цикл нуклеотидов. У термофильных анаэробов ( Thermotoga maritima) Hsp70 демонстрирует окислительно-восстановительное связывание с модельными пептидами, что указывает на второй способ регуляции связывания, основанный на окислительном стрессе.
Hsp70, по-видимому, может участвовать в удалении поврежденных или дефектных белков. Взаимодействие с CHIP ( C arboxyl-концом Н SP70 Я nteracting Р rotein) -an Е3 убиквитин лигазы -Позволяет Hsp70, чтобы передать белки в клеточном убиквитинировании и протеолиз пути.
Наконец, помимо улучшения общей целостности белка, Hsp70 непосредственно ингибирует апоптоз. Одним из отличительных признаков апоптоза является высвобождение цитохрома c, который затем рекрутирует Apaf-1 и dATP / ATP в комплекс апоптосом. Затем этот комплекс расщепляет прокаспазу-9, активируя каспазу-9 и в конечном итоге индуцируя апоптоз через активацию каспазы 3. Hsp70 ингибирует этот процесс, блокируя рекрутирование прокаспазы-9 в апоптосомный комплекс Apaf-1 / dATP / цитохром c. Он не связывается напрямую с сайтом связывания прокаспазы-9, но, вероятно, вызывает конформационные изменения, которые делают связывание прокаспазы-9 менее благоприятным. Показано, что Hsp70 взаимодействует с белком-сенсором стресса эндоплазматического ретикулума IRE1alpha, тем самым защищая клетки от апоптоза, вызванного стрессом ЭР. Это взаимодействие продлевает сплайсинг мРНК XBP-1, тем самым вызывая активацию транскрипции мишеней сплайсированного XBP-1, таких как EDEM1, ERdj4 и P58IPK, спасая клетки от апоптоза. Другие исследования предполагают, что Hsp70 может играть антиапоптотическую роль на других стадиях, но не участвует в апоптозе, опосредованном Fas-лигандом (хотя Hsp 27 участвует). Следовательно, Hsp70 не только сохраняет важные компоненты клетки (белки), но и напрямую спасает клетку в целом. Принимая во внимание, что белки стрессовой реакции (такие как Hsp70) эволюционировали до апоптотического аппарата, прямая роль Hsp70 в ингибировании апоптоза дает интересную эволюционную картину того, как более поздний (апоптотический) аппарат приспособился к предыдущему аппарату (Hsps), таким образом согласовывая улучшенную целостность клеточных белков. с повышенными шансами на выживание этой конкретной клетки.
Hsp70 сверхэкспрессируется при злокачественной меланоме и недоэкспрессируется при почечно-клеточном раке. В клеточной линии рака молочной железы (MCF7) было обнаружено, что не только Hsp90 взаимодействовал с рецептором эстрогена альфа (ERα), но также Hsp70-1 и Hsc70 также взаимодействовали с ERα.
Учитывая роль белков теплового шока как древней защитной системы для стабилизации клеток и устранения старых и поврежденных клеток, эта система была задействована раковыми клетками для стимулирования их роста. В частности, было показано, что повышенный Hsp70 ингибирует апоптоз раковых клеток, а повышенный Hsp70, как было показано, связан или непосредственно вызывает рак эндометрия, легких, толстой кишки, простаты и груди, а также лейкоз. Hsp70 в раковых клетках может быть ответственным за туморогенез и прогрессирование опухоли, обеспечивая устойчивость к химиотерапии. Было показано, что ингибирование Hsp70 уменьшает размер опухолей и может вызывать их полную регрессию. Hsp70 / Hsp90 является особенно привлекательной мишенью для терапевтов, потому что он регулируется путем ингибирования его АТФазной активности, в то время как другие HSP регулируются нуклеотидами. Для Hsp70 было разработано несколько ингибиторов, которые в настоящее время проходят клинические испытания, хотя на данный момент ингибиторы HSP90 оказались более успешными. Кроме того, было показано, что Hsp70 является регулятором иммунной системы, активируя иммунную систему как антиген. Таким образом, Hsp70, полученный из опухоли, был предложен в качестве потенциальной вакцины или средства нацеливания на иммунотерапию. Учитывая повышенную экспрессию Hsp70 при раке, он был предложен в качестве биомаркера для прогнозов рака, при этом высокие уровни предвещают плохой прогноз.
Было показано, что как Hsp70, так и HSP47 экспрессируются в дерме и эпидермисе после лазерного облучения, а пространственные и временные изменения в паттернах экспрессии HSP определяют зону термического повреждения, вызванную лазером, и процесс заживления в тканях. Hsp70 может биохимически определять зону термического повреждения, в которой клетки нацелены на разрушение, а HSP47 может иллюстрировать процесс восстановления после термического повреждения.
Ингибирование Hsp90 приводит к активации Hsp70 и Hsp40, что может направлять неправильно свернутый белок для деградации протеасом, что потенциально может ингибировать прогрессирование нейродегенеративных заболеваний. Например, сверхэкспрессия Hsp70 в клетках нейроглиомы человека, трансфицированных мутантным альфа-синуклеином, привела к уменьшению на 50% олигомерных видов альфа-синуклеина, указывая на возможность того, что увеличение его экспрессии может уменьшить распространение болезни Паркинсона. Точно так же сверхэкспрессия Hsp70 подавляла поли-Q-зависимую агрегацию и нейродегенерацию в клеточных культурах, на моделях дрожжей, мух и мышей, а делеция hsp70 увеличивала размер телец включения polyQ, предполагая, что увеличение его экспрессии может помочь предотвратить болезнь Хантингтона. Точно так же снижение Hsp70 было показано на моделях БАС у трансгенных мышей и у пациентов со спорадическим БАС. Наконец, повышенная экспрессия или активность Hsp70 была предложена в качестве метода предотвращения прогрессирования болезни Альцгеймера, потому что нокаут Hsp70 способствовал токсичности A-бета, и было показано, что Hsp70 способствует стабильности тау, в то время как уровни Hsp70 снижаются при таупатиях, таких как Болезнь Альцгеймера. Учитывая сложное взаимодействие между различными белками-шаперонами, терапевтические разработки в этой области нацелены на изучение того, как можно манипулировать сетью шаперонов в целом, и влияние этой манипуляции на прогрессирование нейродегенеративного заболевания, но баланс уровней Hsp70 и Hsp90 по-видимому, занимает центральное место в этой патофизиологии.
Прокариоты экспрессируют три белка Hsp70: DnaK, HscA (Hsc66) и HscC (Hsc62).
Эукариотические организмы экспрессируют несколько немного разных белков Hsp70. Все они имеют общую доменную структуру, но каждый имеет уникальный паттерн экспрессии или субклеточной локализации. Это, среди прочего:
Ниже приводится список генов Hsp70 человека и соответствующих им белков:
| ген | белок | синонимы | субклеточное расположение |
|---|---|---|---|
| HSPA1A | Hsp70 | HSP70-1, Hsp72 | Nuc / Cyto |
| HSPA1B | Hsp70 | HSP70-2 | Nuc / Cyto |
| HSPA1L | Hsp70 | ? | |
| HSPA2 | Hsp70-2 | ? | |
| HSPA5 | Hsp70-5 | BiP / Grp78 | ER |
| HSPA6 | Hsp70-6 | ? | |
| HSPA7 | Hsp70-7 | ? | |
| HSPA8 | Hsp70-8 | Hsc70 | Nuc / Cyto |
| HSPA9 | Hsp70-9 | Grp75 / mtHsp70 | Мито |
| HSPA12A | Hsp70-12a | ? | |
| HSPA14 | Hsp70-14 | ? |

Hsp90 необходимы для ремоделирования белков, как и белки Hsp70, и играют особенно важную роль у эукариот, где было высказано предположение, что Hsp90 взаимодействует с системой DnaK (состоящей из DnaK, GrpE и либо DnaJ, либо CbpA), чтобы облегчить этот процесс. ремоделирования белков. В E. coli Hsp90 работают совместно с Hsp70, облегчая ремоделирование и активацию белков. Hsp90Ec и DnaK являются шаперонами Hsp90 и Hsp70 соответственно. DnaK сначала связывает и стабилизирует неправильно свернутый белок, прежде чем работать совместно с Hsp90Ec, чтобы повторно свернуть этот субстрат и вызвать его активацию. Было обнаружено, что в условиях избытка DnaK этот шаперон ингибирует ремоделирование белков. Однако присутствие Hsp90Ec может смягчить этот эффект и сделать возможным ремоделирование белка, несмотря на условия избытка DnaK.
Суперсемейство Hsp70 также включает семейство белков Hsp110 / Grp170 ( Sse), которые являются более крупными белками, родственными Hsp70. Семейство белков Hsp110 имеет разные функции: дрожжевой Sse1p имеет небольшую активность АТФазы, но сам по себе является шапероном, а также фактором обмена нуклеотидов для Hsp70, тогда как близкородственный Sse2p имеет небольшую разворачивающую активность.
Ниже приводится список названных в настоящее время генов HSP110 человека. HSPH2-4 - это предлагаемые имена, и текущее имя связано:
| ген | синонимы | субклеточное расположение |
|---|---|---|
| HSPH1 | HSP105 | Цито |
| HSPH2 | HSPA4 ; АПГ-2; HSP110 | Цито |
| HSPH3 | HSPA4L ; АПГ-1 | Nuc |
| HSPH4 | HYOU1 / Grp170; ORP150; HSP12A | ER |