| Гранулоцитарно-макрофагальный колониестимулирующий фактор | |||||||||
|---|---|---|---|---|---|---|---|---|---|
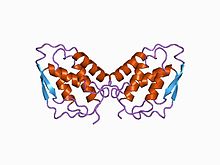 трехмерная структура рекомбинантный колониестимулирующий фактор гранулоцитов-макрофагов человека (rhGM_CSF) трехмерная структура рекомбинантный колониестимулирующий фактор гранулоцитов-макрофагов человека (rhGM_CSF) | |||||||||
| Идентификаторы | |||||||||
| Символ | GM_CSF | ||||||||
| Pfam | PF01109 | ||||||||
| Pfam клан | CL0053 | ||||||||
| InterPro | IPR000773 | ||||||||
| PROSITE | PDOC00584 | ||||||||
| SCOPe | 2gmf / SUPFAM | ||||||||
| |||||||||
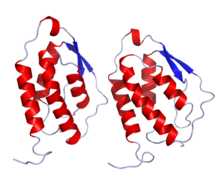 | |
| Клинические данные | |
|---|---|
| Код ATC | |
| Идентификаторы | |
Название IUPAC
| |
| Номер CAS | |
| DrugBank | |
| ChemSpider |
|
| Химические и физические данные | |
| Формула | C639 H 1006 N 168 O 196 S8 |
| Молярная масса | 14434,54 г · моль |
| (что это ?) | |
Гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF ), также известный как колониестимулирующий фактор 2 (CSF2), представляет собой мономерный гликопротеин, секретируемый макрофагами, Т-клетками, тучными клетками, естественными клетками-киллерами, эндотелиальные клетки и фибробласты, которые функционируют как цитокин. фармацевтические аналоги встречающегося в природе GM-CSF называются сарграмостим и молграмостим.
В отличие от колония гранулоцитов - стимулирующий фактор, который специфически способствует пролиферации и созреванию нейтрофилов, GM-CSF влияет на большее количество типов клеток, особенно на макрофаги и эозинофилы.
GM-CSF - это мономерный гликопротеин, который функционирует как цитокин - это лейкоцит фактор роста. GM-CSF стимулирует стволовые клетки к производству гранулоцитов (нейтрофилов, эозинофилов и базофилов ) и моноциты. Моноциты выходят из кровотока и мигрируют в ткань, после чего они созревают в макрофаги и дендритные клетки. Таким образом, он является частью иммунного /воспалительного каскада, посредством которого активация небольшого количества макрофагов может быстро привести к увеличению их количества, a Процесс, важный для борьбы с инфекцией.
GM-CSF также оказывает некоторое влияние на зрелые клетки иммунной системы. К ним относятся, например, усиление миграции нейтрофилов и изменение рецепторов, экспрессируемых на поверхности клеток.
сигналы GM-CSF через преобразователь сигналов и активатор транскрипции, STAT5. В макрофагах также было показано, что он передает сигнал через STAT3. Цитокин активирует макрофаги, препятствуя выживанию грибов. Он вызывает депривацию внутриклеточного свободного цинка и увеличивает производство активных форм кислорода, что приводит к грибковому голоданию и токсичности цинка. Таким образом, GM-CSF способствует развитию иммунной системы и способствует защите от инфекций.
GM-CSF также играет роль в эмбриональном развитии, действуя как эмбриокин, продуцируемый репродуктивным трактом.
Человеческий ген был локализован в непосредственной близости от гена интерлейкина 3 в кластере генов Т-хелперов ассоциированных цитокинов типа 2 в области 5q31 хромосомы, которая, как известно, связана с интерстициальными делециями в 5q- синдром и острый миелолейкоз. GM-CSF и IL-3 разделены изолирующим элементом и, таким образом, регулируются независимо. Другие гены в кластере включают гены, кодирующие интерлейкины 4, 5 и 13.
Колониестимулирующий фактор гранулоцитов-макрофагов человека гликозилирован в его зрелой форме.
GM-CSF был впервые клонирован в 1985 году, и вскоре после этого с использованием технологии рекомбинантной ДНК были изготовлены три потенциальных лекарственных продукта: молграмостим был произведен в Escherichia coli и не гликозилирован, сарграмостим был произведен в дрожжах, имеет лейцин вместо пролина в положении 23 и в некоторой степени гликозилирован, и был произведен в клетках яичника китайского хомячка (СНО) и имеет больше гликозилирование, чем сарграмостим. Степень гликозилирования влияет на то, как организм взаимодействует с лекарством и как лекарство взаимодействует с организмом.
В то время Институт генетики, Inc. работал над молграмостимом, Иммунекс работал над сарграмостимом (лейкин), а Сандоз работал над реграмостимом.
Молграмостим в конечном итоге был разработан и продан совместно компаниями Novartis и Schering-Plough под торговой маркой Leucomax для использования в восстановлении уровня белых кровяных клеток после химиотерапии, а в 2002 году Novartis продала свои права компании Schering-Plough.
Сарграмостим был одобрен FDA США в 1991 году для ускорения белого восстановление клеток крови после аутологичной трансплантации костного мозга под торговым названием Leukine, которое прошло через несколько рук, в результате получился Genzyme, который впоследствии был приобретен Sanofi. Leukine в настоящее время принадлежит компании Partner Therapeutics (PTx).
Imlygic был одобрен FDA США в октябре 2015 года, а в декабре 2015 года EMA как онколитическая виротерапия, коммерциализированная Amgen Inc. Этот вирус онколитического герпеса, названный Талимоген laherparepvec был генетически сконструирован для экспрессии человеческого GM-CSF с использованием аппарата опухолевых клеток.
GM-CSF обнаружен в высоких уровнях в суставах с ревматоидный артрит и блокирование GM-CSF как биологической мишени может уменьшить воспаление или повреждение. Некоторые препараты (например, отилимаб ) разрабатываются для блокирования GM-CSF. У тяжелобольных пациентов GM-CSF был испытан в качестве терапии для иммуносупрессии критического заболевания и показал многообещающее восстановление функции моноцитов и нейтрофилов, хотя влияние на исходы пациентов в настоящее время неясно и ожидает более крупных исследований.