 | |
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Золото (III) трихлорид | |
| Другие названия Хлорид ауриновой кислоты. Трихлорид золота | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.033.280 |
| PubChem CID | |
| номер RTECS |
|
| UNII | |
| Панель управления CompTox (EPA ) | |
InChI
| |
УЛЫБКИ
| |
| Свойства | |
| Химическая формула | AuCl 3. (существует как Au 2Cl6) |
| Молярная масса | 606,6511 г / моль |
| Внешний вид | Красные кристаллы (безводные); золотистые, желтые кристаллы (моногидрат) |
| Плотность | 4,7 г / см |
| Температура плавления | 254 ° C (489 ° F, 527 K) (разлагается) |
| Растворимость в воде | 68 г / 100 мл (холод) |
| Растворимость | растворим в эфире, мало растворим в жидкости аммиак |
| Магнитный восприимчивость (χ) | -112 · 10 см / моль |
| Структура | |
| Кристаллическая структура | моноклинная |
| Координационная геометрия | Квадратная плоская |
| Опасности | |
| Основная опасности | Раздражающий |
| Паспорт безопасности | См.: страница данных |
| Пиктограммы GHS |  |
| Сигнальное слово GHS | Предупреждение |
| Краткая характеристика опасности GHS | H315, H319, H335 |
| Меры предосторожности GHS | P261, P305 + 351 + 338 |
| Родственные соединения | |
| Другие анионы | Фторид золота (III). Бромид золота (III) |
| Прочие катионы | Хлорид золота (I). Хлорид серебра (I). Хлорид платины (II). Ртуть (II) хлорид |
| Страница дополнительных данных | |
| Структура и. свойства | Показатель преломления (n),. Диэлектрическая проницаемость (εr) и т. Д. |
| Термодинамика. данные | Фазовое поведение. твердое тело – жидкость – газ |
| Спектры l данные | UV, IR, ЯМР, MS |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
Хлорид золота (III), традиционно называемый хлорид ауриновой кислоты, представляет собой химическое соединение из золото и хлор. В молекулярной формуле Au 2Cl 6название трихлорид золота является упрощением, относящимся к эмпирической формуле AuCl 3. Римские цифры в названии указывают на то, что золото имеет степень окисления +3, что является обычным для соединений золота. Существует также другой родственный хлорид золота, хлорид золота (I) (AuCl). Хлористоводородная кислота, HAuCl 4, продукт, образующийся при растворении золота в царской водке, иногда называют «хлоридом золота» или «кислотным трихлоридом золота». Хлорид золота (III) очень гигроскопичен и хорошо растворяется в воде, а также в этаноле. Разлагается при температуре выше 160 ° C или на свету.
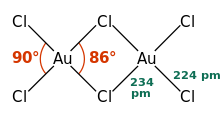
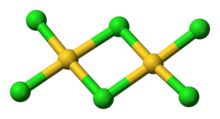
AuCl 3 существует в виде хлормостикового димера как в твердом, так и в парообразном состоянии, по крайней мере, при низких температурах. Бромид золота (III) ведет себя аналогичным образом. Структура подобна структуре хлорида йода (III).
В хлориде золота (III) каждый центр золота имеет плоскую квадратную форму, что типично для металлического комплекса с числом электронов d. Связь в AuCl 3 считается несколько ковалентной.
Хлорид золота (III) чаще всего получают пропусканием газообразного хлора над золотым порошком при 180 ° C:
Другой метод получения - это взаимодействие частиц Au с хлоридом с образованием тетрахлораурата. Затем его кислота, хлористоводородная кислота, нагревается для удаления газообразного хлористого водорода. Взаимодействие с царской водкой дает хлорид золота (III):

При контакте с водой AuCl. 3образует кислые гидраты и конъюгат основания [AuCl. 3(OH)].. Его можно уменьшить, Fe. вызывая осаждение элементарного золота из раствора.
Безводный AuCl 3 начинает разлагаться до AuCl примерно при 160 ° C; однако это, в свою очередь, подвергается диспропорционированию при более высоких температурах с образованием металлического золота и AuCl 3.
AuCl 3 является кислотой Льюиса и легко образует комплексы. Например, он реагирует с соляной кислотой с образованием хлористоводородной кислоты (HAuCl. 4):
Другие источники хлорида, такие как KCl, также преобразуют AuCl 3 в AuCl. 4. Водные растворы AuCl 3 реагируют с водным основанием, таким как гидроксид натрия, с образованием осадка Au (OH) 3, который будет растворяют в избытке NaOH с образованием аурата натрия (NaAuO 2). При осторожном нагревании Au (OH) 3 разлагается до оксида золота (III), Au 2O3, а затем до металлического золота.
Золото (III) хлорид является отправной точкой для синтеза многих других соединений золота. Например, реакция с цианидом калия дает водорастворимый комплекс, K [Au (CN) 4 ]:
AuCl 3 вызвало интерес химиков-органиков как слабокислый катализатор для различные реакции, хотя никакие преобразования не были коммерциализированы. Соли золота (III) , особенно Na [AuCl 4 ] (полученные из AuCl 3+ NaCl ), являются альтернативой ртути (II) солей в качестве катализаторов реакций с участием алкинов. Иллюстративной реакцией является гидратация концевых алкинов с образованием ацетил соединений.

Некоторые алкины подвергаются аминированию в присутствии катализаторов на основе золота (III). Золото катализирует алкилирование определенных ароматических колец и превращение фуранов в фенолы. Например, смесь ацетонитрила и хлорида золота (III) катализирует алкилирование 2-метилфурана с помощью метилвинилкетона в 5-положении:

Эффективность этой реакции с органическим золотом заслуживает внимания, потому что и фуран, и кетон чувствительны к побочным реакциям, таким как полимеризация в кислых условиях. В некоторых случаях, когда присутствуют алкины, иногда образуются фенолы (Ts = тозил ):
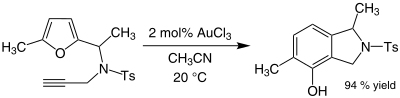
Эта реакция включает перегруппировку, которая дает новое ароматическое кольцо.
В качестве стехиометрического реагента, хлорид ауриновой кислоты реагирует с бензолом (и рядом других аренов) в чрезвычайно мягких условиях (минуты при комнатной температуре) с образованием димерного дихлорида фенилзолота (III):
PhH + ½ Au 2Cl6→ ½ [PhAuCl 2]2+ HCl